Clear Sky Science · zh
神经炎症与神经HIV:理解HIV-1相关因子在小胶质细胞激活中的作用
为何HIV仍困扰大脑
在发现HIV数十年后,许多感染者仍然面临记忆问题、思维迟缓、情绪改变和运动困难。这些问题被统称为“神经HIV”,即使在强效抗逆转录病毒药物时代仍然存在。本文综述探讨了大脑为何仍易受损,重点关注小胶质细胞——大脑内的常驻免疫细胞——以及持续存在的HIV相关分子如何使它们维持一种慢性且有害的激活状态。
看守者却反噬自身
小胶质细胞在正常情况下充当大脑的清道夫与哨兵,清除碎屑、塑造神经元之间的连接,并在感染或损伤时迅速响应。由于小胶质细胞天然表达HIV进入细胞所需的受体且寿命可达多年,它们就成为中枢神经系统中病毒的长期庇护所。即便抗逆转录病毒治疗在血液中抑制了主动病毒复制,受感染的小胶质细胞仍可保留HIV的遗传物质并产生病毒蛋白和RNA。这些残留的病毒产物,以及小的调控RNA和称为细胞外囊泡的微小膜性囊包,能将小胶质细胞从有益的守护者推动为长期的麻烦制造者。
病毒片段如何助长持续的脑部炎症
文章描述了特定HIV成分——尤其是Tat、gp120、Vpr、Nef蛋白及各种病毒RNA——如何反复将小胶质细胞推入炎性状态。来自受感染细胞释放的Tat和gp120能与小胶质细胞表面的受体结合,扰乱钙稳态、线粒体功能和细胞自噬回收系统,从而触发细胞内的危险感知器,导致释放可能损伤邻近神经元的化学信使。即便不引发完整的病毒复制,病毒RNA片段也会在小胶质细胞内被识别为警报信号,激活固有免疫通路和炎症小体复合体,这些复合体像分子式的触发器,最终引发炎性分子的爆发,有时引发一种剧烈的细胞死亡形式,进一步加剧局部损伤。
小胶质细胞内的细胞应激、铁和衰老
除简单的“开—关”免疫激活外,综述还强调了使小胶质细胞随时间变得更具毒性的更深层次细胞改变。Tat能将小胶质细胞驱向类似衰老的衰老样状态:这些细胞分裂减少、氧化损伤积累,并分泌更多炎性因子。Tat还促进一种依赖铁并由脂质受损失控引发的特殊细胞死亡形式——铁死亡(ferroptosis),这一机制与神经退行性疾病的关联日益受到关注。与此同时,Tat扰乱线粒体选择性清除(选择性自噬,mitophagy)和更广泛的自噬清除过程。当这些清理机制失效时,受损的线粒体和脂质堆积,反应性分子增多,关键的炎症通路如NF-κB和NLRP3炎症小体更容易被激活,从而将小胶质细胞锁定在自我维持的有害循环中。
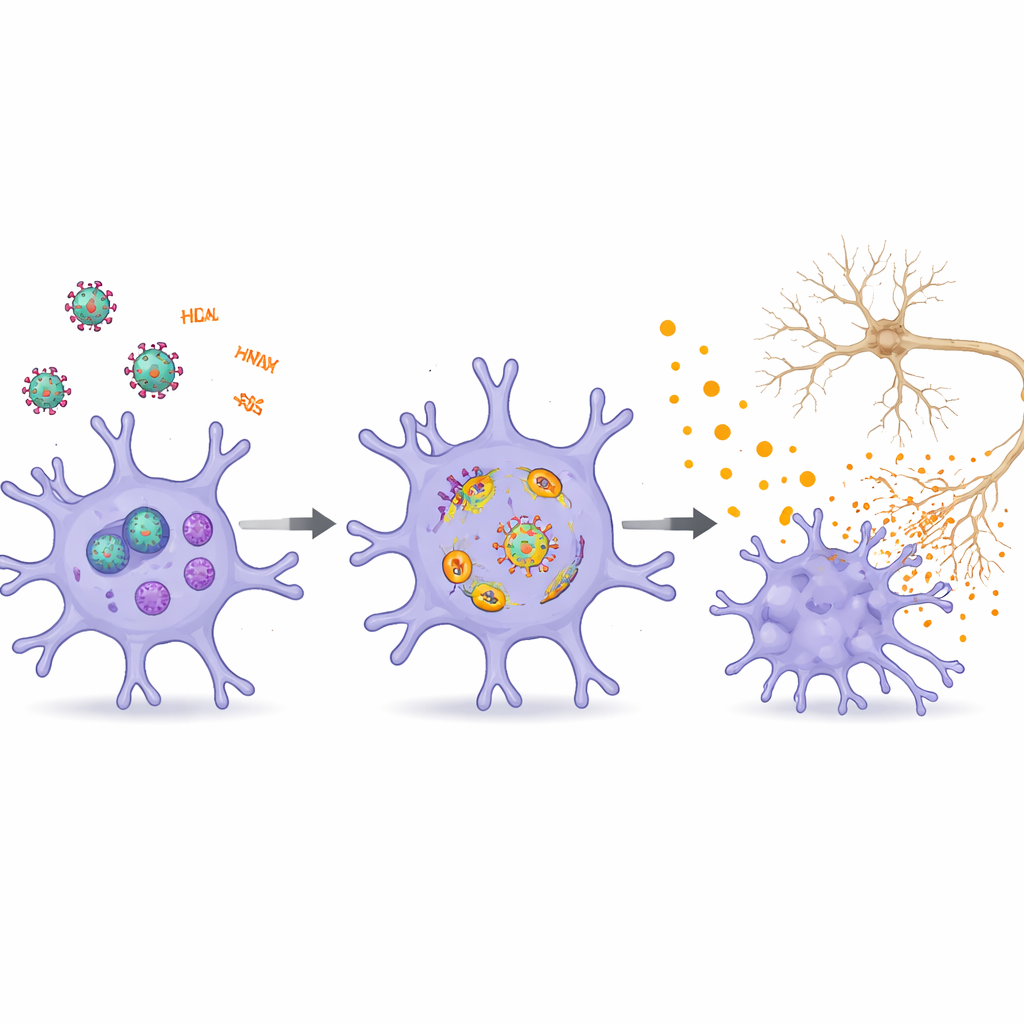
脑细胞间的串扰扩散损害
综述将小胶质细胞置于受HIV影响的更大脑细胞网络中进行考察。病毒蛋白和RNA通过扰乱能量产生、内体溶酶体运输和支撑突触的纤细树突直接损伤神经元,导致记忆与学习问题。它们削弱血脑屏障,使更多免疫细胞和有害信号进入脑内。支持神经元并维持白质的星形胶质细胞和少突胶质细胞也会对HIV因子作出反应,表现为炎症、衰老样或易于细胞死亡。细胞外囊泡在这些细胞类型间运送病毒蛋白和调控RNA,放大应激信号并强化神经炎症与网络功能障碍的循环。
趋向更平静大脑的新途径
对外行而言,核心信息是神经HIV并非仅由活跃病毒增殖引起,而是由来自HIV的持续“分子噪声”使小胶质细胞和其他脑细胞多年处于高度警戒状态。这种慢性、潜燃的炎症逐步侵蚀大脑健康。通过描绘主要分子枢纽——如炎症小体成分、NF-κB信号、受损的细胞回收、自身铁驱动的损伤和特定microRNA——作者勾画出超越常规抗逆转录病毒药物的有前景治疗靶点。这类治疗旨在抑制脑内储库中的病毒活性、恢复小胶质细胞的健康行为并打断炎症的恶性反馈回路,为保护感染者的认知功能与生活质量带来希望。
引用: Zhao, J., Bu, F., Wu, H. et al. Neuroinflammation and NeuroHIV: understanding the role of HIV-1 related factors in microglial activation. Transl Psychiatry 16, 194 (2026). https://doi.org/10.1038/s41398-026-03941-7
关键词: 神经HIV, 小胶质细胞, 神经炎症, HIV脑部并发症, HIV储库