Clear Sky Science · sv
Neuroinflammation och NeuroHIV: förstå rollen för HIV-1-relaterade faktorer i mikrogliaaktivering
Varför HIV fortfarande plågar hjärnan
Decennier efter upptäckten av HIV har många som lever med viruset fortfarande problem med minnet, långsammare tänkande, humörförändringar och rörelsesvårigheter. Dessa problem, samlade under begreppet ”NeuroHIV”, kvarstår även i epoken med effektiva antiretrovirala läkemedel. Denna översiktsartikel undersöker varför hjärnan förblir sårbar, med fokus på mikroglia — hjärnans egna immunceller — och hur kvarvarande HIV-relaterade molekyler kan hålla dem i ett kroniskt, skadligt aktiverat tillstånd.
Hjärnans väktare vända mot den
Mikroglia fungerar normalt som hjärnans städare och vakthållare. De rensar bort skräp, formar förbindelser mellan nervceller och svarar snabbt på infektion eller skada. Eftersom mikroglia naturligt uttrycker de receptorer som HIV använder för att tränga in i celler och kan leva i många år blir de långtidsfästen för viruset i centrala nervsystemet. Även när antiretroviral behandling undertrycker aktiv virusspridning i blodet kan infekterade mikroglia fortsätta att hysa HIV:s genetiska material och producera virusproteiner och RNA. Dessa kvarvarande virusprodukter, tillsammans med små regulatoriska RNA och små membranblåsor kallade extracellulära vesiklar, kan knuffa mikroglia från hjälpsamma väktare till kroniska bovar.
Hur virala fragment eldar på pågående hjärninflammation
Författarna beskriver hur specifika HIV-komponenter — särskilt proteinerna Tat, gp120, Vpr, Nef och olika virala RNA — upprepade gånger driver mikroglia in i ett inflammatoriskt läge. Tat och gp120, som frigörs från infekterade celler, binder till receptorer på mikroglia och rubbar kalciumbalansen, mitokondriernas hälsa och cellens återvinningssystem. Detta sätter igång interna dangersensorer som triggar frisättning av kemiska budbärare som kan skada intilliggande neuroner. Virala RNA-fragment, även när de inte leder till full viral replikation, upptäcks som larmssignaler inne i mikroglia. De aktiverar medfödda immunsignaler och inflammasomkomplex som uppträder som molekylära snubbeltrådar, vilket kulminerar i utbrott av inflammatoriska molekyler och ibland en brandliknande form av celldöd som ytterligare eldar på lokal skada.
Cellstress, järn och åldrande i mikroglia
Bortom enkel "på–av"-immunaktivering lyfter översikten fram djupare cellulära förändringar som gör mikroglia mer toxiska över tid. Tat kan driva mikroglia in i ett senescensliknande tillstånd som liknar accelererat åldrande: dessa celler delar sig mindre, ackumulerar oxidativ skada och utsöndrar högre nivåer av inflammatoriska faktorer. Tat främjar också en specialiserad form av celldöd kallad ferroptos, som är beroende av järn och okontrollerad lipidskada och i ökande grad kopplas till neurodegenerativa sjukdomar. Samtidigt stör Tat mitofagi — selektiv borttagning av uttjänta mitokondrier — och bredare autofagi, cellens avfallshanteringssystem. När dessa städrutiner fallerar byggs skadade mitokondrier och lipider upp, reaktiva molekyler ökar och centrala inflammatoriska vägar som NF-κB och NLRP3-inflammasomet blir lättare att aktivera, vilket låser mikroglia i en självförstärkande skadlig loop.
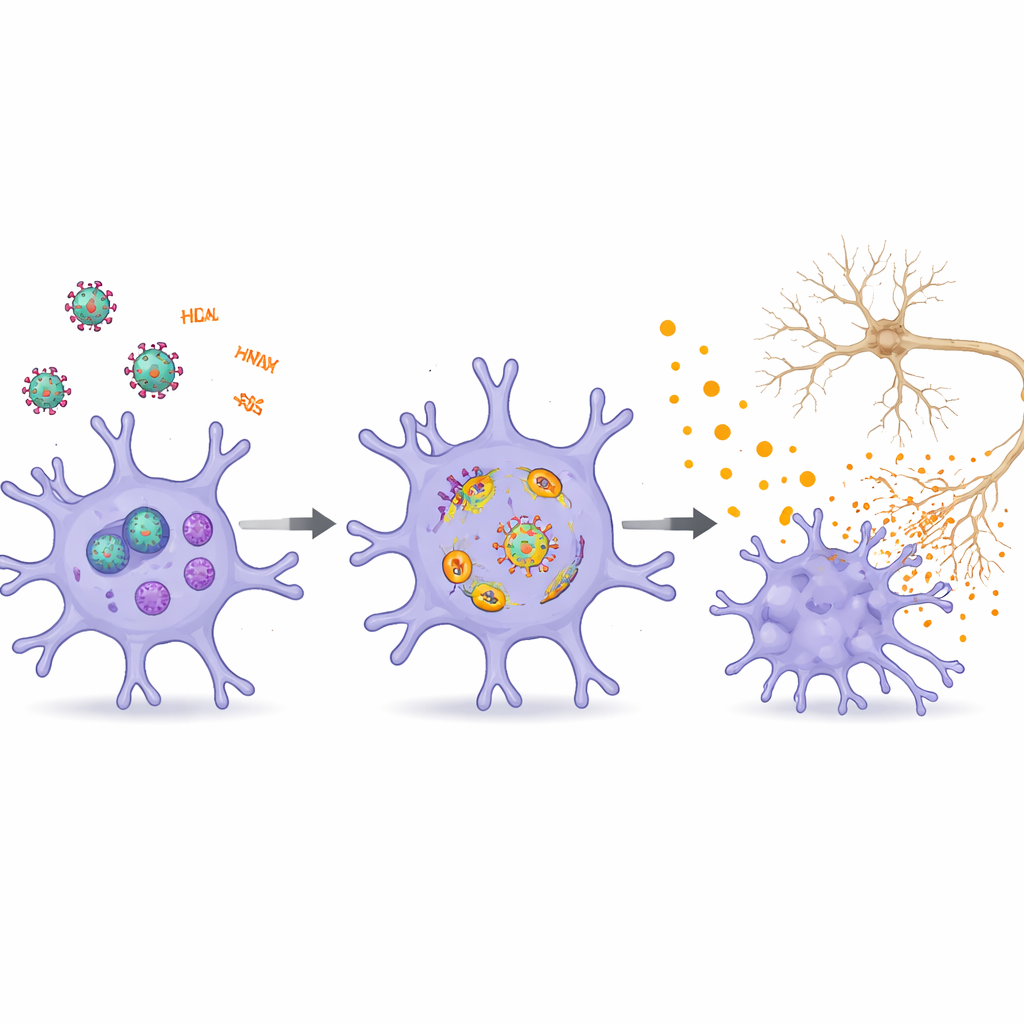
Kommunikation mellan hjärnceller sprider skadan
Översikten placerar mikroglia inom ett större nätverk av hjärnceller som påverkas av HIV. Virusproteiner och RNA skadar neuroner direkt genom att rubba energiproduktion, endolysosomal transport och de känsliga förgreningar som stödjer synapser, vilket bidrar till problem med minne och inlärning. De försvagar blod–hjärnbarriären och tillåter fler immunceller och toxiska signaler att komma in i hjärnan. Astrocyter och oligodendrocyter, som stödjer neuroner och upprätthåller vit substans, reagerar också på HIV-faktorer genom att bli inflammerade, senescenta eller benägna att genomgå celldöd. Extracellulära vesiklar transporterar virusproteiner och regulatoriska RNA mellan dessa celltyper, förstärker nödsignaler och befäster cykler av neuroinflammation och nätverksdysfunktion.
Nya vägar mot lugnare hjärnor
För en lekman är huvudbudskapet att NeuroHIV inte enbart orsakas av aktiv virusmultiplikation, utan av ett kvarvarande "molekylärt brus" från HIV som håller mikroglia och andra hjärnceller på hög beredskap under åratal. Denna kroniska, pyrande inflammation urholkar gradvis hjärnhälsan. Genom att kartlägga de viktigaste molekylära knutpunkterna — såsom inflammasomkomponenter, NF-κB-signalering, defekt cellulär återvinning, järndriven skada och specifika mikroRNA — skisserar författarna lovande mål för framtida terapier som går bortom standard antiretrovirala läkemedel. Sådana behandlingar skulle syfta till att tysta viral aktivitet i hjärnans reservoarer, återställa mikroglians hälsosamma beteende och bryta de onda cirklarna av inflammation, vilket erbjuder hopp om att bevara kognition och livskvalitet hos personer som lever med HIV.
Citering: Zhao, J., Bu, F., Wu, H. et al. Neuroinflammation and NeuroHIV: understanding the role of HIV-1 related factors in microglial activation. Transl Psychiatry 16, 194 (2026). https://doi.org/10.1038/s41398-026-03941-7
Nyckelord: NeuroHIV, mikroglia, neuroinflammation, HIV-hjärnkomplikationer, HIV-reservoarer