Clear Sky Science · es
Neuroinflamación y NeuroHIV: comprendiendo el papel de los factores relacionados con el VIH-1 en la activación microglial
Por qué el VIH sigue afectando al cerebro
Décadas después del descubrimiento del VIH, muchas personas que viven con el virus siguen padeciendo problemas de memoria, lentitud del pensamiento, cambios del ánimo y dificultades de movimiento. Estos problemas, agrupados bajo el término “NeuroHIV”, persisten incluso en la era de potentes fármacos antirretrovirales. Este artículo de revisión examina por qué el cerebro sigue siendo vulnerable, con un enfoque en la microglía —las células inmunitarias residentes del cerebro— y en cómo moléculas relacionadas con el VIH que perduran pueden mantenerlas en un estado crónico y dañino de activación.
Los guardianes del cerebro que se vuelven en su contra
La microglía normalmente actúa como conserje y centinela del cerebro. Elimina desechos, modela las conexiones entre neuronas y responde con rapidez a infecciones o lesiones. Dado que la microglía expresa de forma natural los receptores que utiliza el VIH para entrar en las células y puede vivir durante años, se convierte en un santuario a largo plazo para el virus dentro del sistema nervioso central. Incluso cuando la terapia antirretroviral suprime la replicación viral activa en la sangre, las microglías infectadas pueden seguir albergando material genético del VIH y producir proteínas y ARN virales. Estos productos virales persistentes, junto con pequeños ARN reguladores y diminutos paquetes de membrana llamados vesículas extracelulares, pueden empujar a la microglía de ser guardianes útiles a convertirse en generadores crónicos de daño.
Cómo los fragmentos virales alimentan la inflamación cerebral continua
Los autores describen cómo componentes específicos del VIH —especialmente las proteínas Tat, gp120, Vpr, Nef y diversos ARN virales— empujan repetidamente a la microglía hacia un modo inflamatorio. Tat y gp120, liberados por células infectadas, se unen a receptores en la microglía y alteran el equilibrio del calcio, la salud mitocondrial y los sistemas de reciclaje celular. Esto dispara sensores de peligro internos que desencadenan la liberación de mensajeros químicos capaces de dañar las neuronas vecinas. Fragmentos de ARN viral, incluso cuando no conducen a una replicación viral completa, son detectados como señales de alarma dentro de la microglía. Activan vías inmunitarias innatas y complejos de inflamasoma que actúan como cables trampa moleculares, culminando en ráfagas de moléculas inflamatorias y, a veces, en una forma explosiva de muerte celular que alimenta aún más el daño local.
Estrés celular, hierro y envejecimiento dentro de la microglía
Más allá de una simple activación inmunitaria “encendido–apagado”, la revisión destaca cambios celulares más profundos que hacen que la microglía sea más tóxica con el tiempo. Tat puede conducir a la microglía a un estado parecido a la senescencia que recuerda a un envejecimiento acelerado: estas células se dividen menos, acumulan daño oxidativo y secretan niveles elevados de factores inflamatorios. Tat también promueve una forma especializada de muerte celular llamada ferroptosis, que depende del hierro y del daño lipídico descontrolado y que está cada vez más vinculada a enfermedades neurodegenerativas. Al mismo tiempo, Tat interfiere con la mitofagia —la eliminación selectiva de mitocondrias deterioradas— y con la autofagia en general, el sistema de eliminación de residuos de la célula. Cuando estos procesos de limpieza fallan, las mitocondrias dañadas y los lípidos se acumulan, aumentan las especies reactivas y vías inflamatorias clave como NF-κB y el inflamasoma NLRP3 son más fáciles de activar, encerrando a la microglía en un bucle dañino y autosostenido.
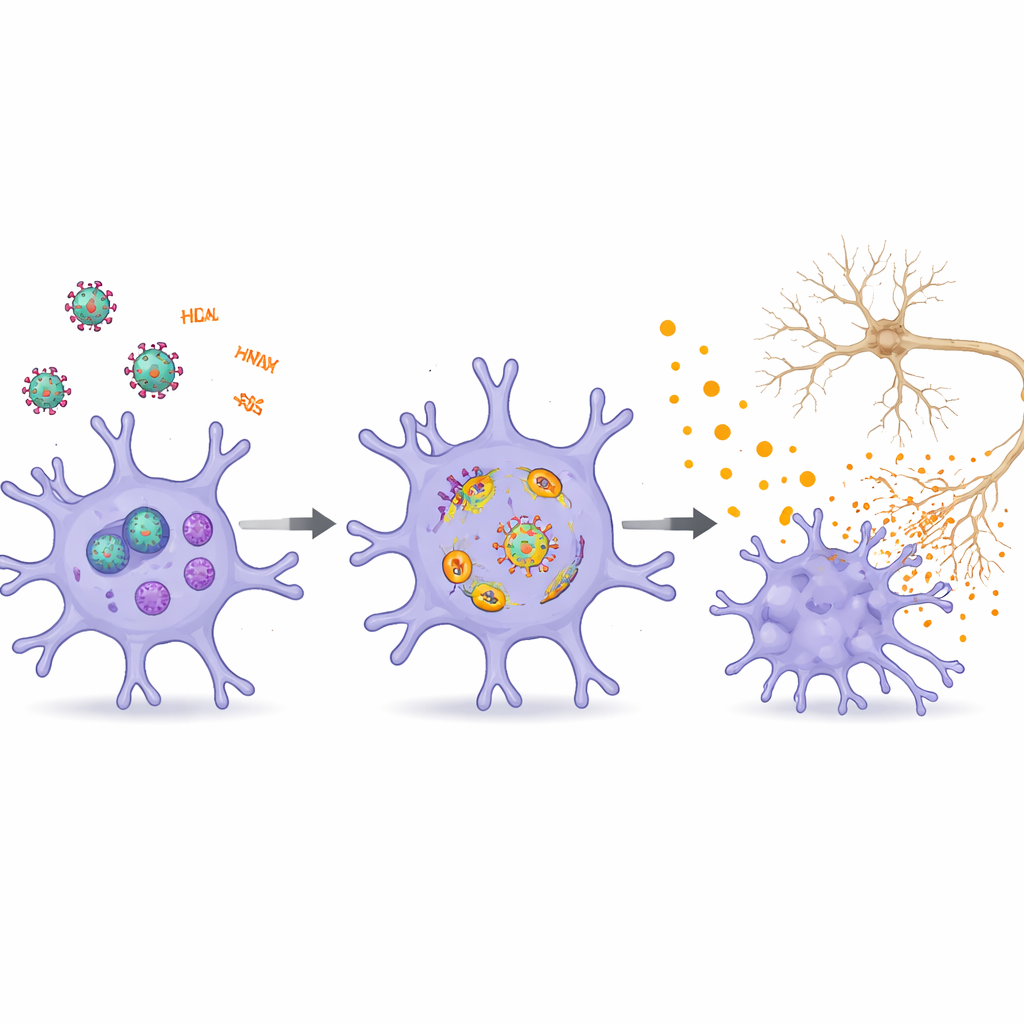
Comunicación entre células cerebrales que propaga el daño
La revisión sitúa a la microglía dentro de una red mayor de células cerebrales influida por el VIH. Las proteínas y los ARN virales dañan directamente a las neuronas al alterar la producción de energía, el tráfico endolisosomal y las delicadas ramas que sostienen las sinapsis, contribuyendo a problemas de memoria y aprendizaje. Debilitan la barrera hematoencefálica, permitiendo la entrada al cerebro de más células inmunitarias y señales tóxicas. Astroglía y oligodendrocitos, que apoyan a las neuronas y mantienen la materia blanca, también responden a los factores del VIH volviéndose inflamados, senescentes o proclives a morir. Las vesículas extracelulares transportan proteínas virales y ARN regulador entre estos tipos celulares, amplificando las señales de angustia y reforzando ciclos de neuroinflamación y disfunción de las redes neuronales.
Nuevas vías hacia cerebros más tranquilos
Para un lector no especializado, el mensaje clave es que la NeuroHIV no se debe simplemente al crecimiento viral activo, sino a un “ruido molecular” persistente del VIH que mantiene a la microglía y otras células cerebrales en alerta máxima durante años. Esta inflamación crónica y latente erosiona gradualmente la salud cerebral. Al cartografiar los principales nodos moleculares —como componentes del inflamasoma, la señalización NF-κB, el reciclaje celular defectuoso, el daño impulsado por el hierro y microARN específicos— los autores delinean objetivos prometedores para futuras terapias que vayan más allá de los fármacos antirretrovirales estándar. Tales tratamientos buscarían silenciar la actividad viral dentro de los reservorios cerebrales, restaurar el comportamiento saludable de la microglía e interrumpir los círculos viciosos de inflamación, ofreciendo esperanza para preservar la cognición y la calidad de vida de las personas que viven con VIH.
Cita: Zhao, J., Bu, F., Wu, H. et al. Neuroinflammation and NeuroHIV: understanding the role of HIV-1 related factors in microglial activation. Transl Psychiatry 16, 194 (2026). https://doi.org/10.1038/s41398-026-03941-7
Palabras clave: NeuroHIV, microglía, neuroinflamación, complicaciones cerebrales por VIH, reservorios del VIH