Clear Sky Science · nl
Neuroinflammatie en NeuroHIV: het begrijpen van de rol van HIV‑1‑gerelateerde factoren bij microgliale activatie
Waarom HIV de hersenen nog steeds lastigvalt
Decennia na de ontdekking van HIV hebben veel mensen die met het virus leven nog steeds moeite met geheugen, vertraagd denken, stemmingsveranderingen en bewegingsproblemen. Deze klachten, samengevat onder de term “NeuroHIV,” blijven bestaan zelfs in het tijdperk van krachtige antiretrovirale medicijnen. Dit overzichtsartikel onderzoekt waarom de hersenen kwetsbaar blijven, met de nadruk op microglia—de residentiële immuuncellen van de hersenen—en hoe aanhoudende HIV‑gerelateerde moleculen ze in een chronische, schadelijke activatiestatus kunnen houden.
De waakhonden van de hersenen keren zich tegen de hersenen
Microglia functioneren normaal als de schoonmakers en wachters van de hersenen. Ze ruimen afval op, vormen verbindingen tussen zenuwcellen en reageren snel op infectie of letsel. Omdat microglia van nature de receptoren tot expressie brengen die HIV gebruikt om cellen binnen te dringen en omdat ze jarenlang kunnen leven, vormen ze langetermijnschuilplaatsen voor het virus binnen het centrale zenuwstelsel. Zelfs wanneer antiretrovirale therapie actieve virale replicatie in het bloed onderdrukt, kunnen geïnfecteerde microglia HIV‑genetisch materiaal blijven herbergen en virale eiwitten en RNA produceren. Deze aanhoudende virale producten, samen met kleine regulerende RNA’s en kleine membraanpakketjes die extracellulaire vesikels worden genoemd, kunnen microglia verschuiven van nuttige beschermer naar chronische probleemmaker.
Hoe virale fragmenten aanhoudende hersenontsteking aanwakkeren
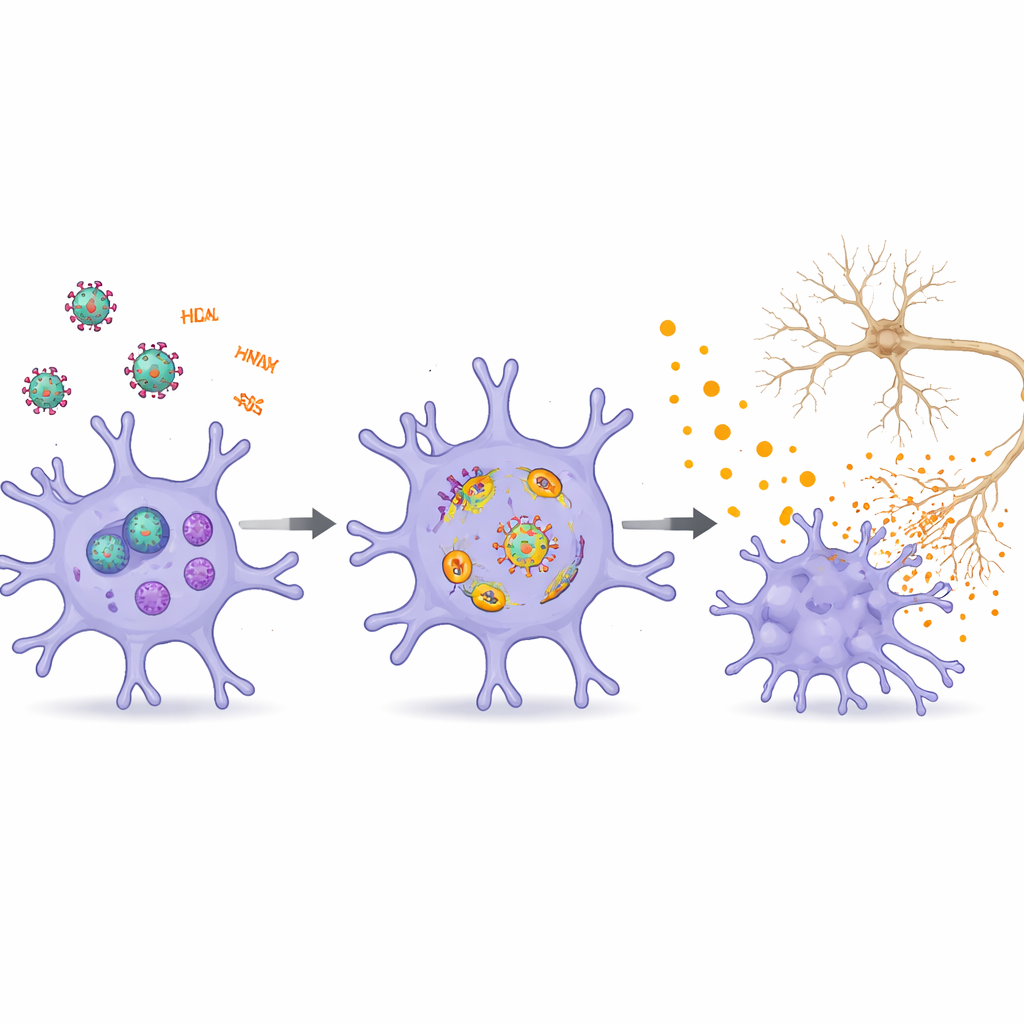
De auteurs beschrijven hoe specifieke HIV‑componenten—vooral de eiwitten Tat, gp120, Vpr, Nef en diverse virale RNA’s—herhaaldelijk microglia in een inflammatoire stand zetten. Tat en gp120, die vrijkomen uit geïnfecteerde cellen, binden aan receptoren op microglia en verstoren de calciumbalans, de mitochondriale gezondheid en de cellulaire recyclingmechanismen. Dit activeert interne gevaarsensoren die de afgifte van chemische boodschappers uitlokken die naburige neuronen kunnen beschadigen. Virale RNA‑fragmenten, zelfs wanneer ze niet tot volledige virusreplicatie leiden, worden binnen microglia als alarmeringssignalen herkend. Ze activeren aangeboren immuunroutes en inflammasoomcomplexen die als moleculaire strijkbomen functioneren, culminerend in uitbarstingen van ontstekingsmediatoren en soms een hevige vorm van celdood die de lokale schade verder aanwakkert.
Celstress, ijzer en veroudering binnen microglia
Buiten eenvoudige “aan‑of‑uit” immuunactivatie belicht het overzicht diepere cellulaire veranderingen die microglia na verloop van tijd toxischer maken. Tat kan microglia in een senescentie‑achtige staat duwen die op versnelde veroudering lijkt: deze cellen delen minder, hopen oxidatieve schade op en scheiden hogere niveaus van ontstekingsfactoren uit. Tat bevordert ook een gespecialiseerde vorm van celdood genaamd ferroptose, die afhankelijk is van ijzer en ongecontroleerde lipidenbeschadiging en steeds vaker wordt gekoppeld aan neurodegeneratieve aandoeningen. Tegelijk verstoort Tat mitofagie—de selectieve verwijdering van versleten mitochondriën—en bredere autofagie, het afvalverwerkingssysteem van de cel. Wanneer deze opruimprocessen falen, hopen beschadigde mitochondriën en lipiden zich op, stijgt het aantal reactieve moleculen en zijn sleutelontstekingsroutes zoals NF‑κB en het NLRP3‑inflammasoom gemakkelijker te activeren, waardoor microglia in een zichzelf in stand houdende schadelijke lus worden vastgezet.
Wederzijdse communicatie tussen hersencellen verspreidt de schade
Het overzicht plaatst microglia binnen een groter netwerk van hersencellen dat door HIV wordt beïnvloed. Virale eiwitten en RNA beschadigen neuronen direct door energielevering, endolysosomale trafficking en de delicate vertakkingen die synapsen ondersteunen te verstoren, wat bijdraagt aan geheugen‑ en leerproblemen. Ze verzwakken de bloed‑hersenbarrière, waardoor meer immuuncellen en toxische signalen de hersenen kunnen binnendringen. Astrocyten en oligodendrocyten, die neuronen ondersteunen en het witte stof onderhoudt, reageren ook op HIV‑factoren door ontstoken, senescent of vatbaar voor celdood te worden. Extracellulaire vesikels vervoeren virale eiwitten en regulerende RNA’s tussen deze celtypen, versterken stresssignalen en bestendigen cycli van neuroinflammatie en netwerkdysfunctie.
Nieuwe wegen naar rustiger hersenen
Voor een niet‑specialist is de kernboodschap dat NeuroHIV niet louter wordt veroorzaakt door actieve virale vermenigvuldiging, maar door aanhoudende “moleculaire ruis” van HIV die microglia en andere hersencellen langdurig op scherp zet. Deze chronische, smeulende ontsteking tast geleidelijk de hersengezondheid aan. Door de belangrijkste moleculaire knooppunten in kaart te brengen—zoals inflammasoomcomponenten, NF‑κB‑signaalgeving, defecte cellulaire recycling, ijzergedreven schade en specifieke microRNA’s—schetsen de auteurs veelbelovende doelen voor toekomstige therapieën die verder gaan dan standaard antiretrovirale middelen. Dergelijke behandelingen zouden gericht zijn op het tot zwijgen brengen van virale activiteit binnen hersenreservoirs, het herstel van gezond microgliaal gedrag en het doorbreken van vicieuze feedbacklussen van ontsteking, wat hoop biedt op behoud van cognitie en levenskwaliteit bij mensen die met HIV leven.
Bronvermelding: Zhao, J., Bu, F., Wu, H. et al. Neuroinflammation and NeuroHIV: understanding the role of HIV-1 related factors in microglial activation. Transl Psychiatry 16, 194 (2026). https://doi.org/10.1038/s41398-026-03941-7
Trefwoorden: NeuroHIV, microglia, neuroinflammatie, HIV‑complicaties in de hersenen, HIV‑reservoirs