Clear Sky Science · pl
Neurozapalanie i NeuroHIV: zrozumienie roli czynników związanych z HIV-1 w aktywacji mikrogleju
Dlaczego HIV wciąż zagraża mózgowi
Dziesięciolecia po odkryciu HIV wiele osób żyjących z wirusem nadal boryka się z problemami pamięci, spowolnieniem myślenia, zmianami nastroju i zaburzeniami ruchowymi. Te objawy, zgrupowane pod terminem „NeuroHIV”, utrzymują się nawet w erze skutecznej terapii przeciwretrowirusowej. Niniejszy artykuł przeglądowy analizuje, dlaczego mózg pozostaje podatny, koncentrując się na mikrogleju — komórkach odpornościowych mózgu — oraz na tym, jak utrzymujące się cząsteczki związane z HIV mogą utrzymywać je w przewlekłym, szkodliwym stanie aktywacji.
Stróże mózgu obróceni przeciw niemu
Mikroglej zazwyczaj działa jak sprzątacz i strażnik mózgu. Usuwa resztki, modeluje połączenia między komórkami nerwowymi i szybko reaguje na infekcję lub uszkodzenie. Ponieważ mikroglej naturalnie wyraża receptory, których HIV używa do wnikania do komórek, i może przetrwać przez lata, staje się długoterminowym sanktuarium dla wirusa w ośrodkowym układzie nerwowym. Nawet gdy terapia przeciwretrowirusowa tłumi aktywną replikację wirusa we krwi, zakażone komórki mikrogleju mogą nadal przechowywać materiał genetyczny HIV i wytwarzać białka wirusowe oraz RNA. Te utrzymujące się produkty wirusowe, wraz z małymi regulatorowymi RNA i maleńkimi pęcherzykami błonowymi zwanymi zewnątrzkomórkowymi pęcherzykami, mogą przesunąć mikroglej z roli pomocnych strażników do chronicznych sprawców szkód.
Jak fragmenty wirusa podtrzymują zapalenie mózgu
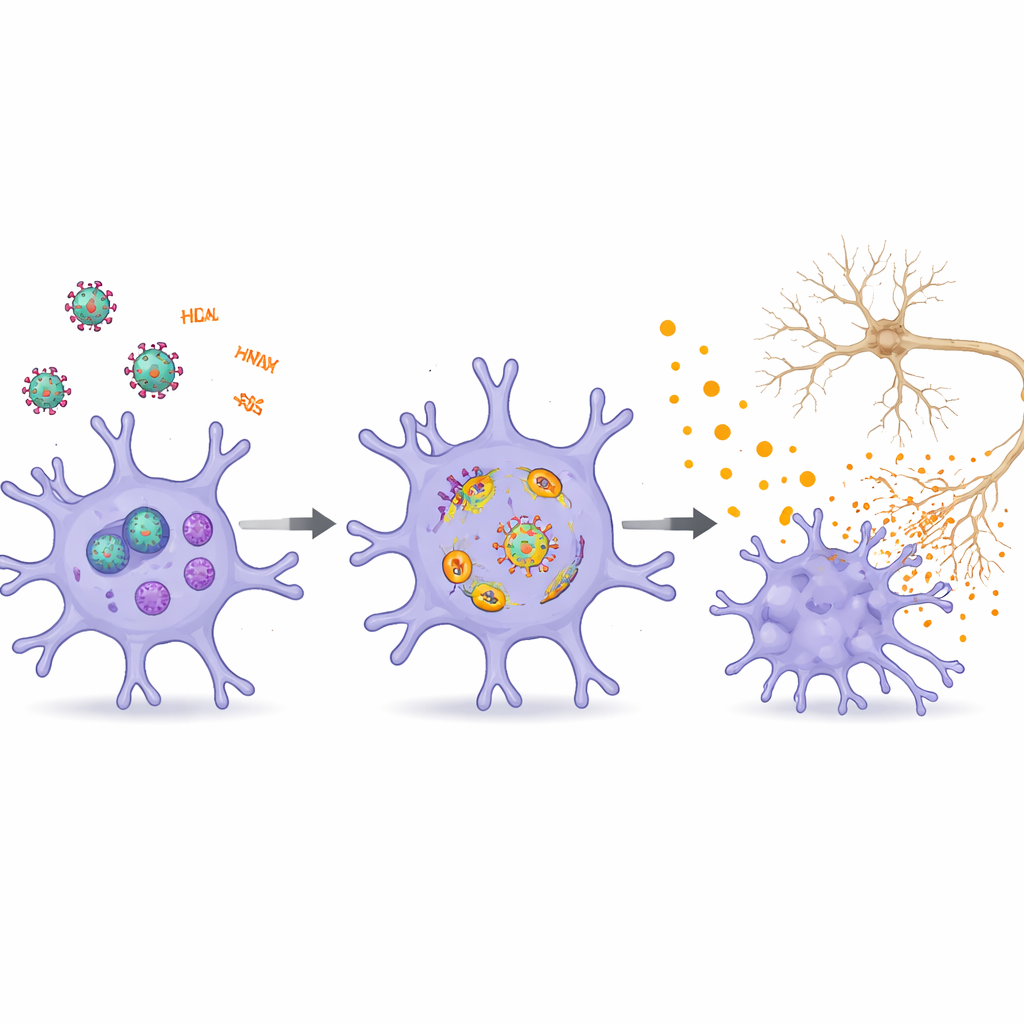
Autorzy opisują, jak specyficzne składniki HIV — w szczególności białka Tat, gp120, Vpr, Nef oraz różne RNA wirusowe — wielokrotnie popychają mikroglej w stan zapalny. Tat i gp120, uwalniane z zakażonych komórek, wiążą się z receptorami na mikrogleju i zaburzają równowagę wapniową, funkcjonowanie mitochondriów oraz systemy komórkowego recyklingu. Wyzwala to wewnątrzkomórkowe czujniki zagrożenia, które inicjują uwalnianie komunikatorów chemicznych zdolnych uszkadzać sąsiednie neurony. Fragmenty RNA wirusa, nawet jeśli nie doprowadzają do pełnej replikacji wirusa, są rozpoznawane jako sygnały alarmowe wewnątrz mikrogleju. Aktywują one wrodzone ścieżki odpornościowe i komplexy inflammasomu, które działają jak molekularne zapadki, kończąc się wybuchami molekuł zapalnych i czasami ogniistą formą śmierci komórki, co dodatkowo napędza miejscowe uszkodzenia.
Stres komórkowy, żelazo i starzenie się mikrogleju
Ponad prostą aktywacją „włącz–wyłącz”, przegląd podkreśla głębsze zmiany komórkowe, które z czasem czynią mikroglej bardziej toksycznym. Tat może wprowadzać mikroglej w stan podobny do senescencji, przypominający przyspieszone starzenie: te komórki dzielą się rzadziej, gromadzą uszkodzenia oksydacyjne i wydzielają wyższe poziomy czynników zapalnych. Tat promuje również wyspecjalizowaną formę śmierci komórkowej zwaną ferroptozą, zależną od żelaza i niekontrolowanego uszkodzenia lipidów, która coraz częściej łączy się z chorobami neurodegeneracyjnymi. Równocześnie Tat zaburza mitofagię — selektywne usuwanie zużytych mitochondriów — oraz szerszą autofagię, system utylizacji odpadów komórkowych. Gdy te procesy oczyszczania zawodzą, uszkodzone mitochondria i lipidy się kumulują, wzrasta liczba reaktywnych cząsteczek, a kluczowe szlaki zapalne, takie jak NF-κB i inflammasom NLRP3, łatwiej ulegają aktywacji, blokując mikroglej w samopodtrzymującej się szkodliwej pętli.
Dialog między komórkami mózgu rozprzestrzenia szkodę
Przegląd umieszcza mikroglej w szerszej sieci komórek mózgowych wpływanych przez HIV. Białka i RNA wirusa uszkadzają neurony bezpośrednio, zakłócając produkcję energii, transport endolizosomalny i delikatne rozgałęzienia wspierające synapsy, co przyczynia się do problemów z pamięcią i uczeniem się. Osłabiają barierę krew–mózg, umożliwiając napływ większej liczby komórek odpornościowych i toksycznych sygnałów do mózgu. Astrocyty i oligodendrocyty, które wspierają neurony i utrzymują istotę białą, także reagują na czynniki HIV, stając się zapalne, sędziwe lub podatne na śmierć komórkową. Zewnątrzkomórkowe pęcherzyki transportują białka wirusowe i regulatorowe RNA między tymi typami komórek, wzmacniając sygnały stresu i utrwalając cykle neurozapalania oraz dysfunkcji sieciowej.
Nowe drogi ku spokojniejszym mózgom
Dla osoby niebędącej specjalistą kluczowy wniosek jest taki, że NeuroHIV nie wynika wyłącznie z aktywnego rozwoju wirusa, lecz z utrzymującego się „molekularnego szumu” pochodzącego od HIV, który przez lata utrzymuje mikroglej i inne komórki mózgu w stanie podwyższonej gotowości. To przewlekłe, tli się zapalenie stopniowo eroduje zdrowie mózgu. Mapując główne węzły molekularne — takie jak składniki inflammasomu, sygnalizacja NF-κB, defekty w recyklingu komórkowym, uszkodzenia zależne od żelaza oraz konkretne microRNA — autorzy wyznaczają obiecujące cele dla przyszłych terapii wykraczających poza standardowe leki przeciwretrowirusowe. Takie terapie miałby na celu wyciszenie aktywności wirusa w rezerwuarach mózgowych, przywrócenie zdrowego zachowania mikrogleju i przerwanie błędnych pętli zapalnych, dając nadzieję na zachowanie funkcji poznawczych i jakości życia osób żyjących z HIV.
Cytowanie: Zhao, J., Bu, F., Wu, H. et al. Neuroinflammation and NeuroHIV: understanding the role of HIV-1 related factors in microglial activation. Transl Psychiatry 16, 194 (2026). https://doi.org/10.1038/s41398-026-03941-7
Słowa kluczowe: NeuroHIV, mikroglej, neurozapalanie, powikłania mózgowe HIV, rezerwuary HIV