Clear Sky Science · de
Neuroinflammation und NeuroHIV: das Verständnis der Rolle HIV-1‑bezogener Faktoren bei der Mikrogliaaktivierung
Warum HIV das Gehirn weiterhin belastet
Jahrzehnte nach der Entdeckung von HIV haben viele Menschen mit dem Virus weiterhin Probleme mit dem Gedächtnis, verlangsamtem Denken, Stimmungsschwankungen und Bewegungsstörungen. Diese Symptome, zusammengefasst unter dem Begriff „NeuroHIV“, bestehen selbst im Zeitalter wirksamer antiretroviraler Medikamente fort. Dieser Übersichtsartikel untersucht, warum das Gehirn verletzlich bleibt, mit Fokus auf die Mikroglia — die residenten Immunzellen des Gehirns — und darauf, wie verbliebene HIV‑bezogene Moleküle sie in einen chronisch schädlichen Aktivierungszustand drängen können.
Die Wächter des Gehirns, die sich gegen es wenden
Mikroglia fungieren normalerweise als Hausmeister und Wachposten des Gehirns. Sie beseitigen Schutt, formen Verbindungen zwischen Nervenzellen und reagieren schnell auf Infektionen oder Verletzungen. Da Mikroglia von Natur aus die Rezeptoren exprimieren, die HIV für das Eindringen in Zellen nutzt, und viele Jahre überdauern können, werden sie zu langfristigen Zufluchtsorten für das Virus im zentralen Nervensystem. Selbst wenn antiretrovirale Therapie die aktive Virusvermehrung im Blut unterdrückt, können infizierte Mikroglia weiterhin HIV‑Genmaterial beherbergen und virale Proteine sowie RNA produzieren. Diese verbliebenen viralen Produkte, zusammen mit kleinen regulatorischen RNAs und winzigen membranumhüllten Partikeln, sogenannten extrazellulären Vesikeln, können Mikroglia von hilfreichen Wächtern in chronische Störenfriede verwandeln.
Wie virale Fragmente anhaltende Gehirnentzündung schüren
Die Autoren beschreiben, wie spezifische HIV‑Bestandteile — insbesondere die Proteine Tat, gp120, Vpr, Nef und verschiedene virale RNAs — Mikroglia wiederholt in einen entzündlichen Modus treiben. Tat und gp120, die aus infizierten Zellen freigesetzt werden, binden an Rezeptoren auf Mikroglia und stören das Kalziumgleichgewicht, die mitochondriale Gesundheit und die zellulären Recycling‑Systeme. Dadurch werden intrazelluläre Gefahrensensoren aktiviert, die die Freisetzung chemischer Botenstoffe auslösen, welche benachbarte Neurone schädigen können. Virale RNA‑Fragmente, selbst wenn sie nicht zu vollständiger Virusreplikation führen, werden in Mikroglia als Alarmsignale erkannt. Sie aktivieren angeborene Immunwege und Inflammasom‑Komplexe, die wie molekulare Stolperdrähte wirken, und münden in Schüben entzündlicher Moleküle und manchmal in eine feurige Form des Zelltods, die den lokalen Schaden weiter antreibt.
Zellstress, Eisen und Alterung in Mikroglia
Über einfache „Ein‑/Aus“‑Immunaktivierung hinaus hebt die Übersicht tiefere zelluläre Veränderungen hervor, die Mikroglia im Laufe der Zeit toxischer machen. Tat kann Mikroglia in einen seneszenzähnlichen Zustand treiben, der einer beschleunigten Alterung ähnelt: Diese Zellen teilen sich weniger, akkumulieren oxidative Schäden und sezernieren höhere Mengen entzündlicher Faktoren. Tat fördert außerdem eine spezialisierte Form des Zelltods namens Ferroptose, die von Eisen und außer Kontrolle geratener Lipidschäden abhängt und zunehmend mit neurodegenerativen Erkrankungen in Verbindung gebracht wird. Gleichzeitig stört Tat die Mitophagie — die selektive Beseitigung verschlissener Mitochondrien — sowie die allgemeine Autophagie, das Abfallentsorgungssystem der Zelle. Wenn diese Reinigungsprozesse versagen, häufen sich beschädigte Mitochondrien und Lipide, reaktive Moleküle steigen an und wichtige Entzündungswege wie NF‑κB und das NLRP3‑Inflammasom lassen sich leichter aktivieren, wodurch Mikroglia in eine sich selbst erhaltende schädliche Schleife eingespannt werden.
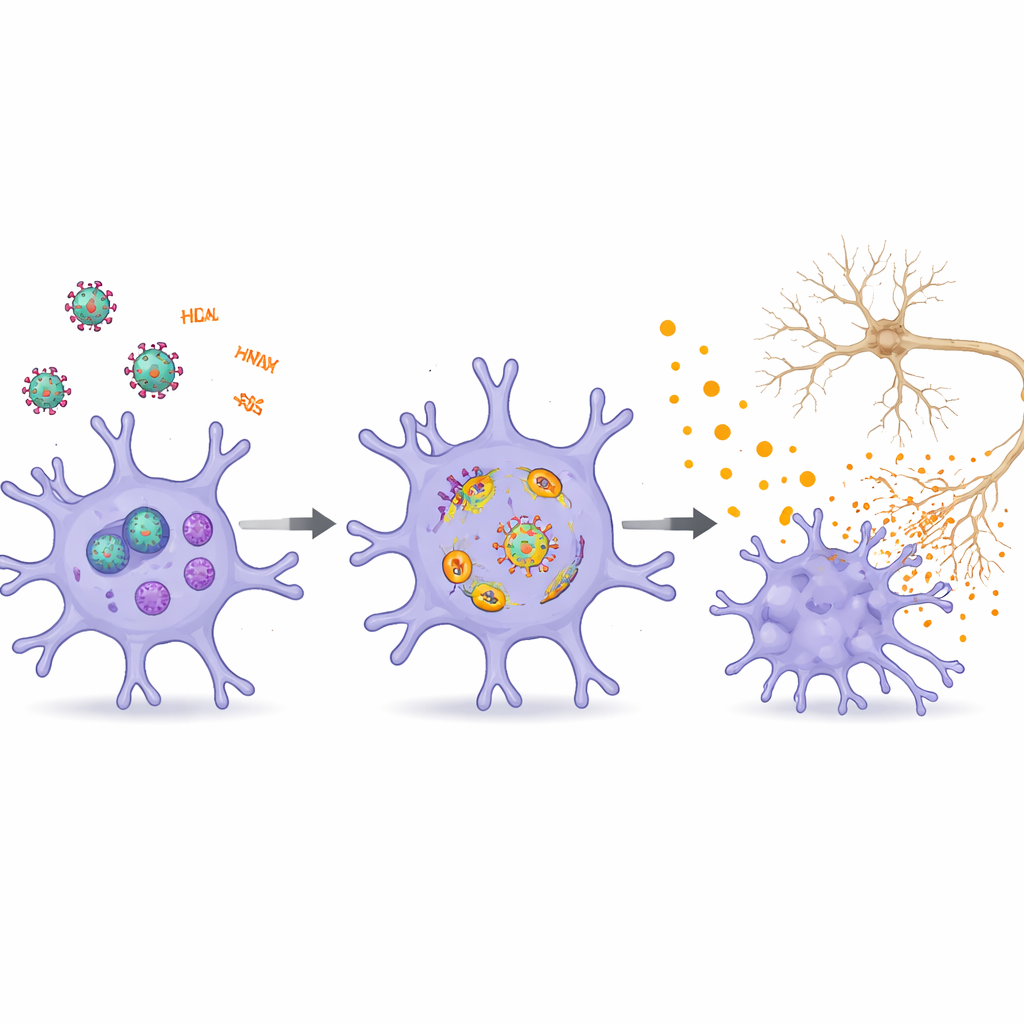
Kommunikation zwischen Hirnzellen verbreitet den Schaden
Die Übersicht stellt Mikroglia in ein größeres Netzwerk von Hirnzellen, die durch HIV beeinflusst werden. Virale Proteine und RNAs schädigen Neurone direkt, indem sie die Energieproduktion, den endolysosomalen Transport und die feinen Verzweigungen, die Synapsen unterstützen, stören, was zu Problemen beim Gedächtnis und Lernen beiträgt. Sie schwächen die Blut‑Hirn‑Schranke und erlauben so mehr Immunzellen und toxische Signale, ins Gehirn einzudringen. Astrozyten und Oligodendrozyten, die Neurone unterstützen und die weiße Substanz erhalten, reagieren ebenfalls auf HIV‑Faktoren, indem sie entzündet, seneszent oder zelltodanfällig werden. Extrazelluläre Vesikel transportieren virale Proteine und regulatorische RNAs zwischen diesen Zelltypen, verstärken Stresssignale und verfestigen Zyklen von Neuroinflammation und Netzwerkdysfunktion.
Neue Wege zu einem ruhigeren Gehirn
Für Laien lautet die Kernbotschaft, dass NeuroHIV nicht einfach durch aktive Virusvermehrung verursacht wird, sondern durch ein anhaltendes „molekulares Rauschen“ von HIV, das Mikroglia und andere Hirnzellen jahrelang in Alarmbereitschaft hält. Diese chronische, schwelende Entzündung zermürbt nach und nach die Gehirngesundheit. Indem die Hauptmolekular‑Knotenpunkte kartiert werden — wie Inflammasom‑Komponenten, NF‑κB‑Signalgebung, defektes zelluläres Recycling, eisengetriebene Schäden und spezifische microRNAs — skizzieren die Autoren vielversprechende Ziele für künftige Therapien, die über die standardmäßigen antiretroviralen Medikamente hinausgehen. Solche Behandlungen würden darauf abzielen, virale Aktivität in Hirnreservoiren zu dämpfen, gesundes Mikroglia‑Verhalten wiederherzustellen und die teuflischen Rückkopplungsschleifen der Entzündung zu unterbrechen, um so die Erhaltung von Kognition und Lebensqualität bei Menschen mit HIV zu fördern.
Zitation: Zhao, J., Bu, F., Wu, H. et al. Neuroinflammation and NeuroHIV: understanding the role of HIV-1 related factors in microglial activation. Transl Psychiatry 16, 194 (2026). https://doi.org/10.1038/s41398-026-03941-7
Schlüsselwörter: NeuroHIV, Mikroglia, Neuroinflammation, HIV‑bedingte Hirnkomplikationen, HIV‑Reservoire