Clear Sky Science · ar
الالتهاب العصبي وNeuroHIV: فهم دور عوامل مرتبطة بـ HIV-1 في تفعيل الخلايا الصغروفية
لماذا لا يزال HIV يزعج الدماغ
بعد عقود من اكتشاف فيروس نقص المناعة البشرية، لا يزال كثير من الأشخاص المصابين يعانون من مشاكل في الذاكرة، بطء التفكير، تغيرات في المزاج، وصعوبات في الحركة. تُجمع هذه المشكلات تحت مصطلح «NeuroHIV» وتستمر حتى في عصر الأدوية المضادة للفيروسات القوية. تستعرض هذه المراجعة سبب بقاء الدماغ عرضة للضرر، مع التركيز على الخلايا الصغروفية — خلايا المناعة المقيمة في الدماغ — وكيف أن جزيئات متبقية مرتبطة بـ HIV يمكن أن تحافظ على هذه الخلايا في حالة تفعيل مزمن وضار.
حراس الدماغ الذين انقلبوا ضده
تعمل الخلايا الصغروفية عادة كعامل تنظيف ومراقبة في الدماغ. تزيل الحطام، تشكّل وصلات بين الخلايا العصبية، وتستجيب بسرعة للعدوى أو الإصابة. وبما أن الخلايا الصغروفية تعبر طبيعياً عن المستقبلات التي يستخدمها HIV لدخول الخلايا ويمكن أن تعيش لسنوات، فإنها تصبح ملاذات طويلة الأمد للفيروس داخل الجهاز العصبي المركزي. حتى عندما تكبح العلاجات المضادة للفيروسات التكاثر الفيروسي النشط في الدم، يمكن للخلايا الصغروفية المصابة أن تستمر في احتواء المادة الوراثية للفيروس وإنتاج بروتينات وRNA فيروسي. هذه المنتجات الفيروسية المتبقية، إلى جانب قطع RNA تنظيمية صغيرة وحويصلات غشائية صغيرة تُسمى الحويصلات خارج الخلية، يمكن أن تدفع الخلايا الصغروفية من دور الحارس المفيد نحو حالة تفعيل مزمنة ومضرة.
كيف تغذي الشظايا الفيروسية الالتهاب المستمر في الدماغ
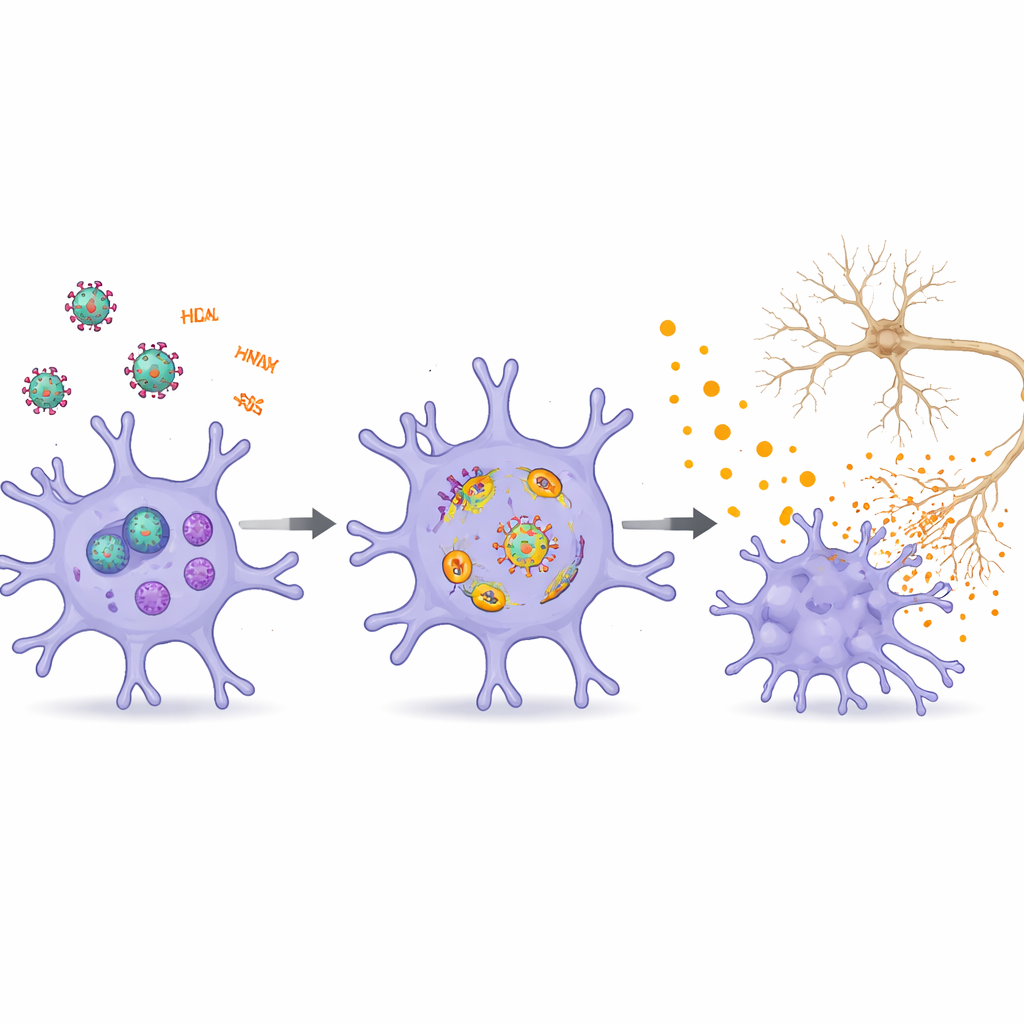
يصف المؤلفون كيف أن مكونات محددة من HIV — خصوصاً البروتينات Tat وgp120 وVpr وNef وأنواع متعددة من RNAs الفيروسية — تدفع الخلايا الصغروفية مراراً إلى وضع التهابي. يرتبط Tat وgp120، اللذان يُفرَزان من الخلايا المصابة، بمستقبلات على الخلايا الصغروفية ويعكّران توازن الكالسيوم، وصحة الميتوكوندريا، وأنظمة إعادة تدوير الخلايا. هذا يشغل مجسات داخلية للخطر تؤدي إلى إطلاق رسولات كيميائية قادرة على إلحاق الضرر بالخلايا العصبية المجاورة. كما تُكتشف شظايا RNA الفيروسية، حتى عندما لا تؤدي إلى تكاثر فيروسي كامل، كإشارات إنذار داخل الخلايا الصغروفية. تُفعّل هذه الشظايا مسارات المناعة الفطرية ومجمعات الإنفلاماسوم التي تتصرف كزناد جزيئي، مما ينتهي بانفجارات من الجزيئات الالتهابية وأحياناً شكل ناري من موت الخلايا يزيد من الضرر المحلي.
إجهاد الخلايا والحديد والشيخوخة داخل الخلايا الصغروفية
بعيداً عن التفعيل المناعي البسيط «تشغيل–إيقاف»، تبرز المراجعة تغيّرات خلوية أعمق تجعل الخلايا الصغروفية أكثر سمّية مع مرور الوقت. يمكن لـ Tat دفع الخلايا الصغروفية نحو حالة شبيهة بالهرم: تنقسم هذه الخلايا أقل، تتراكم فيها أضرار أكسدية، وتفرز مستويات أعلى من العوامل الالتهابية. كما يروّج Tat لشكل متخصص من موت الخلايا يسمى الفِرُّوبْتوزيس (ferroptosis)، الذي يعتمد على الحديد وتلف الدهون خارج السيطرة، والذي يرتبط بشكل متزايد بأمراض التنكس العصبي. في الوقت نفسه، يعطل Tat عملية التخلص الانتقائي من الميتوكوندريا التالفة (الابتلاع البِلّوري الميتوكوندري أو mitophagy) والابتلاع الذاتي الأوسع للخلايا (autophagy)، نظام التخلص من النفايات داخل الخلية. عندما تفشل هذه العمليات التنظيفية، تتراكم الميتوكوندريا والدهون التالفة، ترتفع الجزيئات التفاعلية، وتصبح مسارات التهابية رئيسية مثل NF-κB وإنفلاماسوم NLRP3 أسهل في التفعيل، مما يحبس الخلايا الصغروفية في حلقة ضارة مستمرة ذاتية التعزيز.
الحوار بين خلايا الدماغ ينشر الضرر
تضع المراجعة الخلايا الصغروفية ضمن شبكة أكبر من خلايا الدماغ المتأثرة بـ HIV. تُلحق البروتينات والـ RNA الفيروسية ضرراً مباشراً بالخلايا العصبية عن طريق اضطراب إنتاج الطاقة، وحركة الحويصلات النهائية والليزوزومية، والتفرعات الدقيقة التي تدعم التشابكات العصبية، مساهِمةً في مشكلات الذاكرة والتعلّم. تُضعف هذه العوامل الحاجز الدماغي الدموي، مما يسمح بدخول المزيد من خلايا المناعة والإشارات السامة إلى الدماغ. كما تستجيب النجميات والخلايا قليلة التغصّن، التي تدعم الخلايا العصبية وتحافظ على المادة البيضاء، لعوامل HIV بالتهاب أو دخول حالة هرمة أو الميل إلى موت الخلايا. تنقل الحويصلات خارج الخلية البروتينات الفيروسية وRNAs التنظيم بين هذه الأنواع الخلوية، مما يضخم إشارات الضيق ويعزز دورات الالتهاب العصبي واختلال الشبكات.
طرق جديدة نحو أدمغة أكثر هدوءًا
للشخص غير المتخصص، الرسالة الأساسية هي أن NeuroHIV لا ينجم ببساطة عن نمو فيروسي نشط، بل عن «ضوضاء جزيئية» متبقية من HIV تحافظ على تأهُّب الخلايا الصغروفية وخلايا الدماغ الأخرى على مدى سنوات. هذا الالتهاب المزمن المدخّر يقوّض صحة الدماغ تدريجياً. من خلال رسم خرائط للمحاور الجزيئية الرئيسية — مثل مكونات الإنفلاماسوم، وإشارات NF-κB، وإخفاقات إعادة تدوير الخلايا، والضرر المدفوع بالحديد، وبعض microRNA محددة — يحدّد المؤلفون أهدافاً واعدة للعلاجات المستقبلية التي تتجاوز الأدوية المضادة للفيروسات التقليدية. ستهدف مثل هذه العلاجات إلى كبح نشاط الفيروس داخل مخازن الدماغ، استعادة السلوك الصحي للخلايا الصغروفية، وقطع حلقات التغذية الراجعة الالتهابية الخبيثة، ما قد يقدّم أملاً في الحفاظ على الإدراك وجودة الحياة لدى الأشخاص الذين يعيشون مع HIV.
الاستشهاد: Zhao, J., Bu, F., Wu, H. et al. Neuroinflammation and NeuroHIV: understanding the role of HIV-1 related factors in microglial activation. Transl Psychiatry 16, 194 (2026). https://doi.org/10.1038/s41398-026-03941-7
الكلمات المفتاحية: NeuroHIV, الخلايا الصغروفية, الالتهاب العصبي, مضاعفات فيروس HIV في الدماغ, مخازن HIV