Clear Sky Science · ru
Нейровоспаление и NeuroHIV: понимание роли факторов, связанных с ВИЧ‑1, в активации микроглии
Почему ВИЧ всё ещё наносит вред мозгу
Десятилетия спустя после открытия ВИЧ многие люди, живущие с вирусом, по‑прежнему испытывают проблемы с памятью, замедленное мышление, изменения настроения и нарушения двигательной функции. Эти симптомы, объединяемые термином «NeuroHIV», сохраняются даже в эпоху эффективной антиретровирусной терапии. В этом обзоре исследуется, почему мозг остаётся уязвимым: внимание сосредоточено на микроглии — резидентных иммунных клетках мозга — и на том, как остаточные молекулы, связанные с ВИЧ, могут удерживать их в хроническом, вредоносном состоянии активации.
Сторожа мозга, повернувшиеся против него
Микроглия обычно выполняет роль уборщиков и стражей мозга. Она удаляет мусор, формирует связи между нервными клетками и быстро реагирует на инфекцию или повреждение. Поскольку микроглия естественно экспрессирует рецепторы, которыми пользуется ВИЧ для проникновения в клетки, и может существовать годами, она становится долгосрочным убежищем для вируса в центральной нервной системе. Даже когда антиретровирусная терапия подавляет активную репликацию вируса в крови, инфицированные микроглиальные клетки могут сохранять генетический материал ВИЧ и производить вирусные белки и РНК. Эти остающиеся вирусные продукты, наряду с малыми регуляторными РНК и крошечными мембранными пакетами — внеклеточными везикулами, — способны сместить микроглию из полезных стражей в хронических источников вреда.
Как фрагменты вируса подпитывают продолжающееся воспаление мозга
Авторы описывают, как специфические компоненты ВИЧ — особенно белки Tat, gp120, Vpr, Nef и различные вирусные РНК — многократно переводят микроглию в воспалительное состояние. Tat и gp120, высвобождаемые инфицированными клетками, связываются с рецепторами на микроглии и нарушают баланс кальция, здоровье митохондрий и системы клеточного переработки. Это запускает внутренние сенсоры опасности, которые приводят к выбросу химических медиаторов, способных повреждать соседние нейроны. Вирусные фрагменты РНК, даже когда они не приводят к полной репликации вируса, распознаются как сигналы тревоги внутри микроглии. Они активируют пути врождённого иммунитета и комплексы воспалительных инфламмасом, которые действуют как молекулярные растяжки, кульминирующие вспышками воспалительных молекул и иногда — в виде огненной формы клеточной гибели — дополнительно подпитывают локальное повреждение.
Клеточный стресс, железо и старение внутри микроглии
За пределами простого «включения–выключения» иммунной активации обзор подчёркивает более глубокие клеточные изменения, которые со временем делают микроглию более токсичной. Tat может переводить микроглию в состояние, похожее на сенесценцию — ускоренное старение: такие клетки реже делятся, накапливают оксидативные повреждения и секретируют больше провоспалительных факторов. Tat также способствует специализированной форме смерти клеток — ферроптозу, который зависит от железа и неконтролируемого окислительного повреждения липидов и всё чаще связывается с нейродегенеративными заболеваниями. Одновременно Tat нарушает митофагию — селективное удаление изношенных митохондрий — и более общие пути аутофагии, систему утилизации клеточного мусора. Когда эти механизмы очистки дают сбой, накапливаются повреждённые митохондрии и липиды, повышается уровень реактивных молекул, и ключевые воспалительные пути, такие как NF-κB и инфламмасома NLRP3, легче активируются, запирая микроглию в самоподдерживающейся вредной петле.
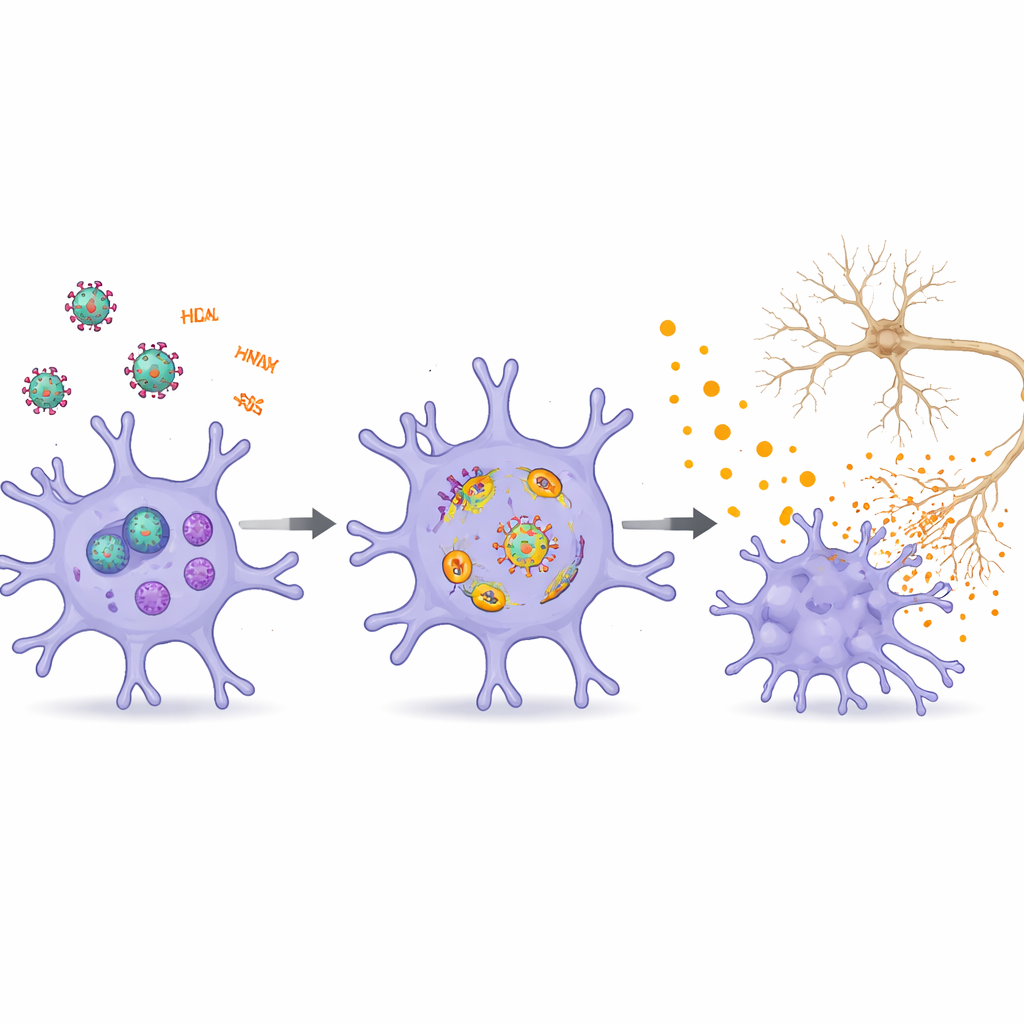
Взаимодействие между клетками мозга распространяет вред
Обзор рассматривает микроглию в контексте более широкой сети клеток мозга, на которые влияет ВИЧ. Вирусные белки и РНК повреждают нейроны напрямую, нарушая выработку энергии, эндолизосомный трафик и тонкие отростки, поддерживающие синапсы, что вносит вклад в проблемы с памятью и обучением. Они ослабляют гематоэнцефалический барьер, позволяя в мозг проникать большему числу иммунных клеток и токсичных сигналов. Астроциты и олигодендроциты, которые поддерживают нейроны и поддерживают белое вещество, также реагируют на факторы ВИЧ, становясь воспалёнными, сенесцентными или склонными к гибели. Внеклеточные везикулы переносят вирусные белки и регуляторные РНК между этими типами клеток, усиливая сигналы бедствия и подкрепляя циклы нейровоспаления и дисфункции сети.
Новые пути к успокоению мозга
Для неспециалиста ключевая мысль заключается в том, что NeuroHIV вызывается не просто активным размножением вируса, а сохраняющимся «молекулярным шумом» от ВИЧ, который держит микроглию и другие клетки мозга в состоянии повышенной бдительности годами. Это хроническое, тлеющее воспаление постепенно разрушает здоровье мозга. Сопоставляя основные молекулярные узлы — такие как компоненты инфламмасомы, сигнальная система NF-κB, дефекты клеточной утилизации, железозависимое повреждение и специфические микроРНК — авторы выделяют перспективные мишени для будущих терапий, выходящих за рамки стандартных антиретровирусных препаратов. Такие подходы будут направлены на подавление вирусной активности в мозговых резервуарах, восстановление нормального поведения микроглии и разрыв порочных циклов воспаления, давая надежду на сохранение когнитивных функций и качества жизни людей, живущих с ВИЧ.
Цитирование: Zhao, J., Bu, F., Wu, H. et al. Neuroinflammation and NeuroHIV: understanding the role of HIV-1 related factors in microglial activation. Transl Psychiatry 16, 194 (2026). https://doi.org/10.1038/s41398-026-03941-7
Ключевые слова: NeuroHIV, микроглия, нейровоспаление, компликации ВИЧ в мозге, резервуары ВИЧ