Clear Sky Science · tr
Nöroinflamasyon ve NeuroHIV: mikroglial aktivasyonda HIV‑1 ilişkili faktörlerin rolünü anlamak
Neden HIV Hâlâ Beyni Rahatsız Ediyor
HIV keşfedildikten on yıllar sonra, virüsle yaşayan birçok kişi hâlâ hafıza sorunları, yavaşlayan düşünme, ruh hali değişiklikleri ve hareket güçlükleriyle mücadele ediyor. “NeuroHIV” terimiyle toplanan bu sorunlar, güçlü antiretroviral ilaçların döneminde bile devam ediyor. Bu derleme makalesi, beynin neden hâlâ savunmasız kaldığını inceliyor; odak noktası beyin yerel bağışıklık hücreleri olan mikroglialar ve kalıcı HIV ilişkili moleküllerin bunları kronik, zararlı bir aktivasyon halinde tutma biçimleri.
Beynin Bekçileri Ona Karşı Dönüyor
Mikroglialar normalde beynin temizlik görevlileri ve gözcüleridir. Atıkları temizler, sinir hücreleri arasındaki bağlantıları şekillendirir ve enfeksiyon veya yaralanmaya hızla yanıt verirler. Mikroglialar doğal olarak HIV’in hücreye girmek için kullandığı reseptörleri ifade ettikleri ve yıllarca yaşayabildikleri için merkezi sinir sistemi içinde virüs için uzun süreli sığınaklar haline gelirler. Antiretroviral tedavi kan içindeki aktif viral replikasyonu baskılasa bile, enfekte mikroglialar HIV’in genetik materyalini barındırmaya ve viral proteinler ile RNA üretmeye devam edebilir. Bu kalıcı viral ürünler, küçük düzenleyici RNA’lar ve ekstrasellüler vezikül adı verilen küçük zarlı paketlerle birlikte, mikrogliaları yardımcı bekçiler konumundan kronik sorun yaratan aktörlere doğru itebilir.
Viral Parçacıklar Süregelen Beyin İnflamasyonunu Nasıl Kışkırtıyor
Yazarlar, özellikle Tat, gp120, Vpr, Nef proteinleri ve çeşitli viral RNA’ların mikrogliaları tekrarlayan şekilde inflamatuar bir moda ittiğini açıklıyor. Enfekte hücrelerden salınan Tat ve gp120, mikroglialardaki reseptörlere bağlanır ve kalsiyum dengesini, mitokondri sağlığını ve hücresel geri dönüşüm sistemlerini bozar. Bu durum, komşu nöronlara zarar verebilecek kimyasal habercilerin salınmasını tetikleyen iç tehlike algılayıcılarını harekete geçirir. Tam viral replikasyona yol açmasalar bile viral RNA fragmanları mikrogliaların içinde alarm sinyalleri olarak algılanır. Bunlar, moleküler tetik sistemi gibi davranan innat bağışıklık yollarını ve inflamazom komplekslerini aktive eder; sonuçta inflamatuar moleküllerin ani salınımları ve bazen yerel hasarı daha da körükleyen ateşli bir hücre ölümü biçimi ortaya çıkar.
Mikroglialarda Hücresel Stres, Demir ve Yaşlanma
Basit bir “açık–kapalı” bağışıklık aktivasyonunun ötesinde, derleme mikrogliaları zaman içinde daha toksik hale getiren daha derin hücresel değişiklikleri vurguluyor. Tat, mikrogliaları hızlandırılmış yaşlanmaya benzeyen bir senesans‑benzeri hâle sürükleyebilir: bu hücreler daha az bölünür, oksidatif hasar biriktirir ve daha yüksek düzeyde inflamatuar faktörler salgılar. Tat ayrıca demir bağımlı ve lipid hasarının kontrolsüzleşmesine dayanan ferroptozis adı verilen özelleşmiş bir hücre ölümü biçimini teşvik eder; bu yol giderek nörodejeneratif hastalıklarla ilişkilendiriliyor. Aynı zamanda Tat, yıpranmış mitokondrilerin seçici olarak uzaklaştırılması olan mitofajiyi ve hücrenin atık‑imalat sistemi olan otofajiyi bozar. Bu temizlik süreçleri başarısız olduğunda, hasarlı mitokondriler ve lipitler birikir, reaktif moleküller artar ve NF-κB ile NLRP3 inflamazomu gibi önemli inflamatuar yollar daha kolay aktive olur; bu durum mikrogliaların kendini sürdüren zararlı bir döngüye kilitlenmesine yol açar.
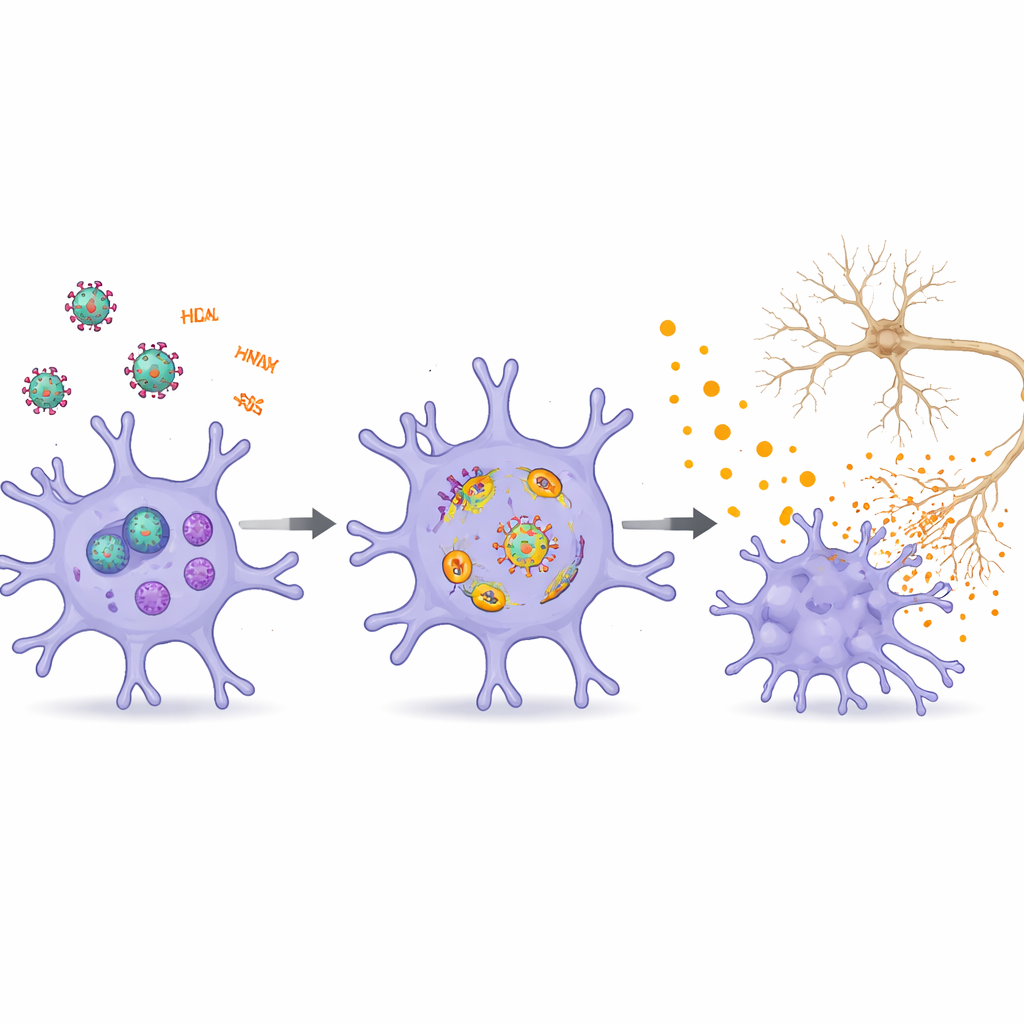
Beyin Hücreleri Arası Konuşma Zararları Yayar
Derleme, mikrogliaları HIV’den etkilenen daha geniş bir beyin hücresi ağının içinde konumlandırıyor. Viral proteinler ve RNA’lar, enerji üretimini, endolizozomal taşımayı ve sinapsları destekleyen hassas dallanmayı bozarak nöronlara doğrudan zarar verir; bu durum hafıza ve öğrenme sorunlarına katkıda bulunur. Kan‑beyin bariyerini zayıflatarak daha fazla bağışıklık hücresi ve toksik sinyalin beyne girmesine izin verirler. Nöronları destekleyen ve ak maddesini koruyan astrositler ile oligodendrositler de HIV faktörlerine inflame, senesans eğilimli veya hücre ölümüne yatkın hale gelerek yanıt verir. Ekstrasellüler veziküller, viral proteinleri ve düzenleyici RNA’ları bu hücre tipleri arasında taşıyarak stres sinyallerini artırır ve nöroinflamasyon ile ağ işlev bozukluğunun döngülerini pekiştirir.
Daha Sakin Beyinlere Doğru Yeni Yollar
Bir meraklıya yönelik temel mesaj, NeuroHIV’in yalnızca aktif viral çoğalmadan kaynaklanmadığı; mikrogliaları ve diğer beyin hücrelerini yıllarca yüksek alarm hâlinde tutan kalıcı bir “moleküler gürültü” nedeniyle oluştuğudur. Bu kronik, sönmek bilmeyen inflamasyon zamanla beyin sağlığını aşındırır. İnflamazom bileşenleri, NF-κB sinyallemesi, kusurlu hücresel geri dönüşüm, demir kaynaklı hasar ve belirli mikroRNA’lar gibi ana moleküler düğüm noktalarını haritalandırarak yazarlar, standart antiretroviral ilaçların ötesine geçen gelecek tedaviler için umut vaat eden hedefleri ortaya koyuyor. Bu tür tedaviler, beyin rezervuarlarındaki viral etkinliği susturmayı, sağlıklı mikroglial davranışı yeniden tesis etmeyi ve inflamasyonun kısır döngülerini kesmeyi amaçlayarak HIV ile yaşayan bireylerde bilişi ve yaşam kalitesini koruma umudu sunabilir.
Atıf: Zhao, J., Bu, F., Wu, H. et al. Neuroinflammation and NeuroHIV: understanding the role of HIV-1 related factors in microglial activation. Transl Psychiatry 16, 194 (2026). https://doi.org/10.1038/s41398-026-03941-7
Anahtar kelimeler: NeuroHIV, mikroglia, nöroinflamasyon, HIV beyin komplikasyonları, HIV rezervuarları