Clear Sky Science · it
Neuroinfiammazione e NeuroHIV: comprendere il ruolo dei fattori correlati all’HIV-1 nell’attivazione delle microglia
Perché l’HIV continua a colpire il cervello
Decenni dopo la scoperta dell’HIV, molte persone che convivono con il virus continuano a soffrire di problemi di memoria, rallentamento del pensiero, alterazioni dell’umore e difficoltà motorie. Questi disturbi, riuniti sotto il termine “NeuroHIV”, persistono anche nell’era dei potenti farmaci antiretrovirali. Questo articolo di revisione esamina perché il cervello resta vulnerabile, concentrandosi sulle microglia — le cellule immunitarie residenti del cervello — e su come le molecole correlate all’HIV persistenti possano mantenerle in uno stato cronico e dannoso di attivazione.
I guardiani del cervello che si rivoltano
Le microglia normalmente agiscono come netturbini e sentinelle del cervello. Eliminano i detriti, scolpiscono le connessioni tra i neuroni e rispondono rapidamente a infezioni o lesioni. Poiché le microglia esprimono naturalmente i recettori che l’HIV usa per entrare nelle cellule e possono vivere per anni, diventano santuari a lungo termine per il virus all’interno del sistema nervoso centrale. Anche quando la terapia antiretrovirale sopprime la replicazione virale attiva nel sangue, le microglia infette possono continuare a ospitare materiale genetico dell’HIV e a produrre proteine virali e RNA. Questi prodotti virali persistenti, insieme a piccoli RNA regolatori e a minuscoli pacchetti membranosi chiamati vescicole extracellulari, possono spingere le microglia da custodi utili a fonti croniche di danno.
Come i frammenti virali alimentano l’infiammazione cerebrale persistente
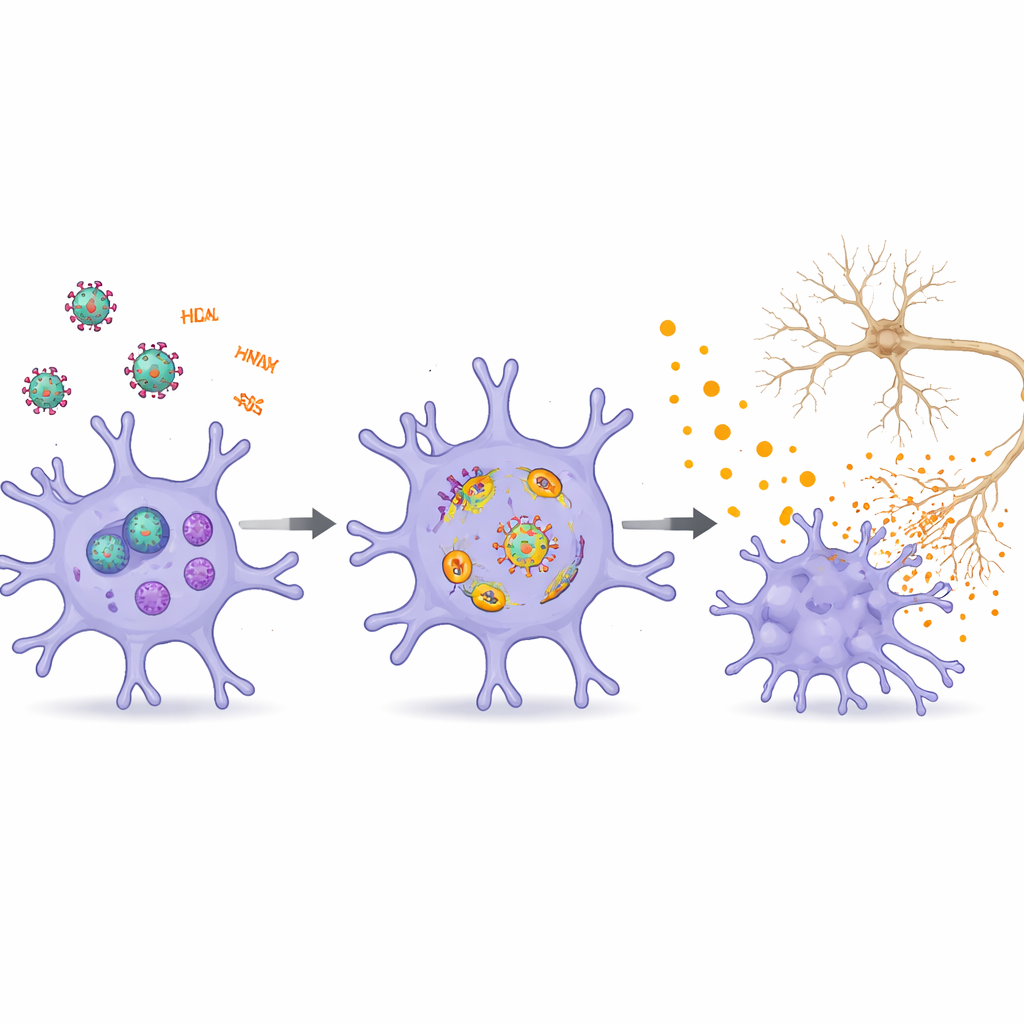
Gli autori descrivono come componenti specifici dell’HIV — in particolare le proteine Tat, gp120, Vpr, Nef e vari RNA virali — indurrebbero ripetutamente le microglia in uno stato infiammatorio. Tat e gp120, rilasciati dalle cellule infette, si legano a recettori sulle microglia e alterano l’equilibrio del calcio, la salute mitocondriale e i sistemi di riciclo cellulare. Ciò attiva sensori di pericolo interni che scatenano il rilascio di messaggeri chimici in grado di danneggiare i neuroni vicini. I frammenti di RNA virale, anche quando non conducono a una replicazione virale completa, vengono rilevati come segnali d’allarme all’interno delle microglia. Attivano vie immunitarie innate e complessi di inflammasoma che funzionano come micce molecolari, culminando in ondate di molecole infiammatorie e talvolta in una forma infiammatoria di morte cellulare che alimenta ulteriormente il danno locale.
Stress cellulare, ferro e invecchiamento nelle microglia
Oltre alla semplice attivazione immunitaria “on–off”, la revisione mette in luce cambiamenti cellulari più profondi che rendono le microglia più tossiche nel tempo. Tat può spingere le microglia verso uno stato simile alla senescenza che ricorda un invecchiamento accelerato: queste cellule si dividono meno, accumulano danni ossidativi e secernono livelli più elevati di fattori infiammatori. Tat promuove anche una forma specializzata di morte cellulare chiamata ferroptosi, che dipende dal ferro e dal danno lipidico incontrollato ed è sempre più collegata a malattie neurodegenerative. Allo stesso tempo, Tat compromette la mitofagia — la rimozione selettiva dei mitocondri usurati — e l’autofagia più ampia, il sistema di smaltimento dei rifiuti della cellula. Quando questi processi di pulizia falliscono, mitocondri danneggiati e lipidi si accumulano, le specie reattive aumentano e vie infiammatorie chiave come NF-κB e l’inflammasoma NLRP3 risultano più facilmente attivabili, intrappolando le microglia in un circuito vizioso autosostenuto di danno.
Il dialogo tra le cellule cerebrali diffonde il danno
La revisione colloca le microglia all’interno di una rete più ampia di cellule cerebrali influenzate dall’HIV. Le proteine e gli RNA virali danneggiano i neuroni direttamente disturbando la produzione di energia, il traffico endolisosomiale e i delicati rami che supportano le sinapsi, contribuendo ai problemi di memoria e apprendimento. Indebolendo la barriera emato-encefalica, permettono l’ingresso di più cellule immunitarie e segnali tossici nel cervello. Astroglia e oligodendrociti, che supportano i neuroni e mantengono la sostanza bianca, rispondono anch’essi ai fattori HIV diventando infiammati, senescenti o suscettibili alla morte cellulare. Le vescicole extracellulari trasportano proteine virali e RNA regolatori tra questi tipi cellulari, amplificando i segnali di disagio e rinforzando i cicli di neuroinfiammazione e disfunzione di rete.
Nuove strade per calmarе il cervello
Per un lettore non specialistico, il messaggio chiave è che la NeuroHIV non è semplicemente causata dalla crescita virale attiva, ma da un “rumore molecolare” persistente dell’HIV che tiene microglia e altre cellule cerebrali in allerta elevata per anni. Questa infiammazione cronica e bruciante erode gradualmente la salute cerebrale. Mappando i principali nodi molecolari — come componenti dell’inflammasoma, la segnalazione NF-κB, il difetto nel riciclo cellulare, il danno guidato dal ferro e specifici microRNA — gli autori delineano obiettivi promettenti per terapie future che vadano oltre i farmaci antiretrovirali standard. Trattamenti di questo tipo mirerebbero a silenziare l’attività virale all’interno dei serbatoi cerebrali, a ripristinare un comportamento microgliale sano e a interrompere i circuiti viziosi dell’infiammazione, offrendo speranza per preservare la cognizione e la qualità della vita delle persone che vivono con l’HIV.
Citazione: Zhao, J., Bu, F., Wu, H. et al. Neuroinflammation and NeuroHIV: understanding the role of HIV-1 related factors in microglial activation. Transl Psychiatry 16, 194 (2026). https://doi.org/10.1038/s41398-026-03941-7
Parole chiave: NeuroHIV, microglia, neuroinfiammazione, complicanze cerebrali da HIV, serbatoi di HIV