Clear Sky Science · zh
血小板导致小鼠蛛网膜下腔出血后微血管栓塞和迟发性神经功能缺损
当脑出血再次袭来
幸存于破裂脑动脉瘤仅是许多患者面临的第一道难关。初次出血数日后,大约一半患者会出现新的、常常严重的神经学问题,如意识混乱、无力或类似中风的症状。临床上称这些为迟发性神经功能缺损,但其确切诱因迄今仍不清楚。这项在小鼠中进行并辅以人体血液检测的研究指出了一个意想不到的“罪魁祸首”:通常用于止血的小而众多的血细胞——血小板,在这种情况下似乎堵塞了大脑最细小的血管,切断了关键的血流。
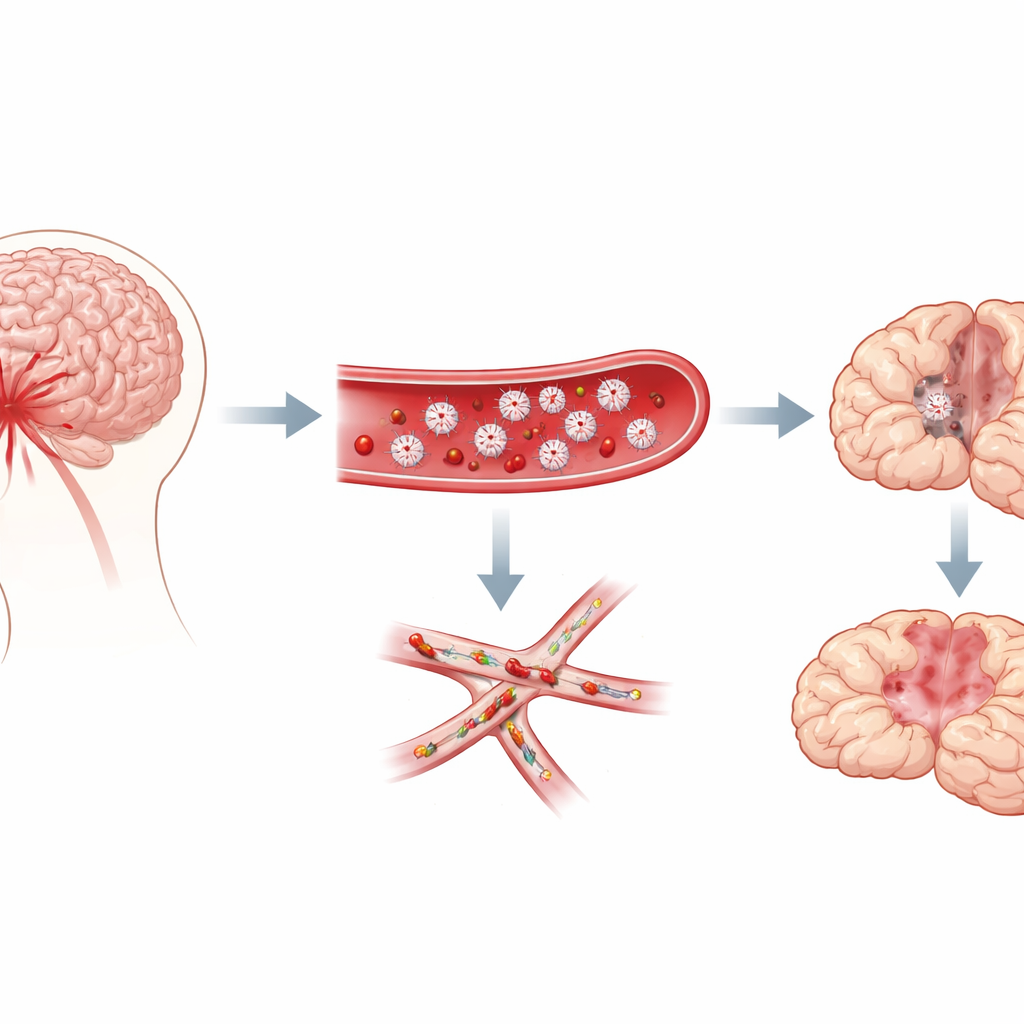
存在于大脑最小血管的微小血栓
研究人员将注意力集中在蛛网膜下腔出血上,这是一种在动脉瘤破裂后充满脑周围间隙的出血。临床上长期观察到,那些随后出现迟发问题的患者通常表现出血液异常易凝的迹象,尸检也显示大脑中散布着无数“微血栓”——针尖大小的血栓。这些血栓富含血小板。然而尚不清楚血小板是导致迟发损伤的元凶还是仅作为旁观者出现。利用经验证的小鼠出血模型,研究团队在一周内追踪了行为表现和脑组织病理,检验血小板活性是否与迟发性缺损的出现相吻合。
开启与关闭血小板
在第一组实验中,科学家测量了血液中已知能激活血小板的化学信号。两种信号,称为PAF和TXB2,在第1天和大约第5天显著升高——这与通常出现迟发问题的高风险窗口相对应。为测试因果关系,他们随后进一步刺激血小板。当小鼠在出血后不久收到额外的PAF时,许多动物死亡且大脑中微血栓增多。在“平静”康复期几天后给予PAF并未导致死亡,但确实引起更差的神经学评分、更多的迟发缺损以及更重的微血栓负担。具有易于迟发性血小板激活基因背景的小鼠表现出类似模式:早期恢复正常,但晚期出现缺损的比率更高。
去除或抑制血小板
既然增强血小板使情况恶化,抑制它们是否有益?为此,团队使用了工程化小鼠,其血小板可在出血前用一种毒素被选择性去除。这些动物并未表现出更多出血或更高的死亡率,但它们的微血栓较少、早期神经功能更好,且出现迟发性衰退的概率显著低于正常小鼠。由于在人体中完全去除血小板并不安全,研究者还测试了几种已上市的药物,这些药物阻断不同的血小板受体——各种信号激活这些细胞或促使其粘连的“对接点”。许多药物改善了早期行为并减少了微血栓,但只有一种药物,替罗非班,能阻断一个关键的“凝集”受体GPIIb/IIIa,在雌性小鼠中明显降低了迟发性缺损的长期发生率。
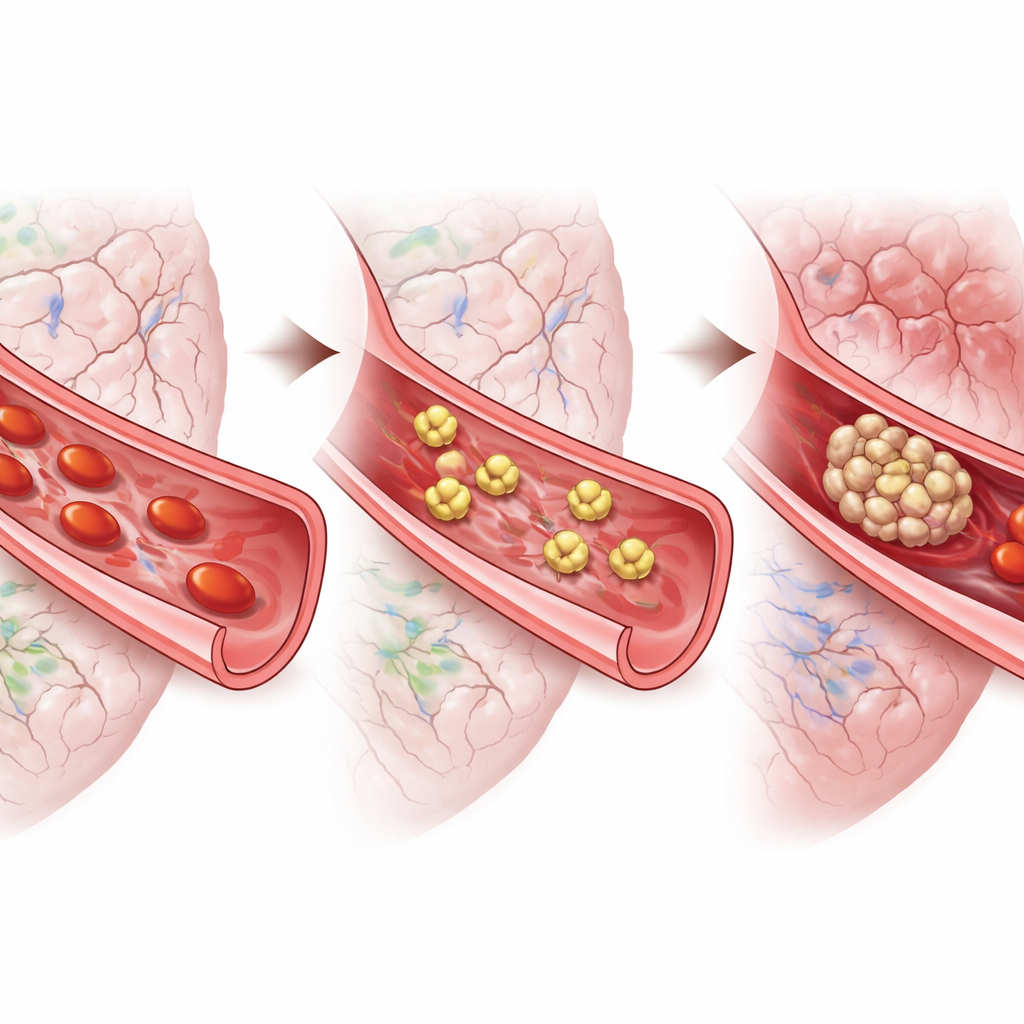
从小鼠到人体
为缩小与人类疾病的差距,研究者从患有动脉瘤性蛛网膜下腔出血的患者体内收集了血小板。在显微镜下,这些细胞高度激活并呈伸展状,符合高度易凝的状态。向样本中加入替罗非班使血小板在出血后早期及随后高风险窗口期都明显不易伸展。另一种针对不同血小板受体的药物效果很小。结合小鼠结果,这些体外检测表明,阻断血小板聚集(即防止它们相互粘连),而不仅仅是抑制某些激活信号,可能是更有前景的策略。
这对未来治疗的意义
这项工作强有力地支持了这样一种观点:血小板不仅仅在脑出血后封堵初始破口——数天之后,它们还促成小簇微血栓,阻塞大脑最细小的血管,为迟发性中风奠定基础。在小鼠中,去除血小板或阻断其主要“粘连”受体可显著减少这些迟发性损伤,而一种已在其他情境中使用的药物替罗非班,也在实验室中抑制了来自患者的过度活化血小板。尽管任何抗血小板治疗都必须权衡增加出血风险,但该研究提供了明确的概念验证:精确靶向血小板聚集的药物有朝一日可能帮助动脉瘤性蛛网膜下腔出血的幸存者免受第二波致命性脑损伤的侵袭。
引用: Dienel, A., Hong, SH., Torres, K. et al. Platelets cause microvascular occlusion and delayed neurological deficits after subarachnoid hemorrhage in mice. Exp Mol Med 58, 1242–1253 (2026). https://doi.org/10.1038/s12276-026-01696-1
关键词: 蛛网膜下腔出血, 血小板, 微血栓, 迟发性脑缺血, 抗血小板治疗