Clear Sky Science · pt
Plaquetas causam oclusão microvascular e déficits neurológicos tardios após hemorragia subaracnoide em camundongos
Quando uma hemorragia cerebral ataca duas vezes
Sobreviver ao rompimento de um aneurisma cerebral é apenas o primeiro obstáculo para muitos pacientes. Dias após o sangramento inicial, cerca de metade desenvolve novos problemas neurológicos, frequentemente devastadores, como confusão, fraqueza ou sintomas semelhantes a AVC. Os médicos chamam isso de déficits neurológicos tardios e, até agora, o gatilho exato permanecia obscuro. Este estudo em camundongos, com testes complementares em sangue humano, aponta um culpado surpreendente: pequenas células sanguíneas chamadas plaquetas que normalmente ajudam a estancar o sangramento mas, nesse contexto, parecem obstruir os menores vasos do cérebro e privar de fluxo sanguíneo vital.
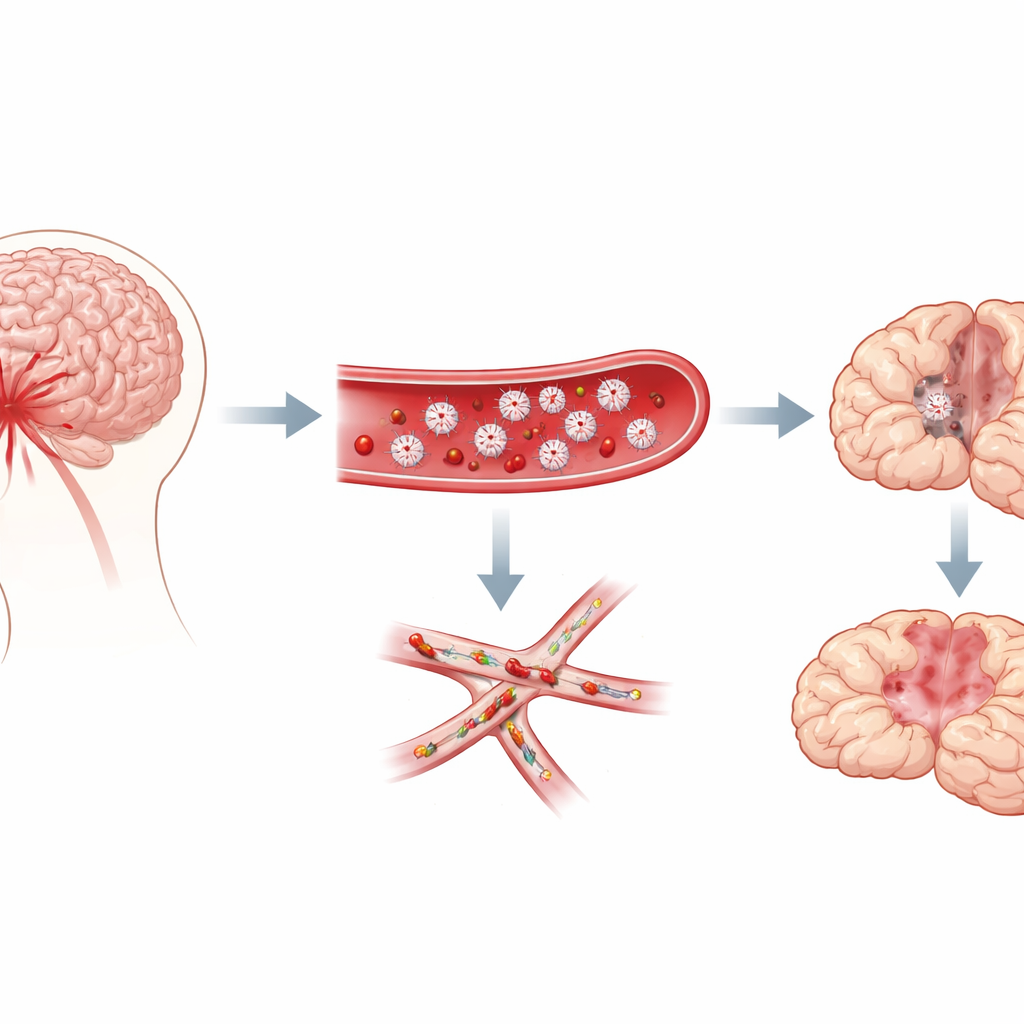
Microcoágulos nos menores vasos do cérebro
Os pesquisadores focaram na hemorragia subaracnoide, um tipo de sangramento que inunda o espaço ao redor do cérebro após o rompimento de um aneurisma. Clínicos há muito observam que pacientes que desenvolvem problemas tardios frequentemente apresentam sinais de tendência aumentada à coagulação, e autópsias revelam inúmeros “microtrombos” — coágulos minúsculos — espalhados pelo cérebro. Esses coágulos são ricos em plaquetas. Ainda assim, não estava claro se as plaquetas realmente causavam o dano tardio ou apenas apareciam como observadoras. Usando um modelo bem estabelecido de hemorragia em camundongos, a equipe acompanhou tanto o comportamento quanto a patologia cerebral ao longo de uma semana, investigando se a atividade plaquetária se alinhava com o aparecimento dos déficits tardios.
Ligando e desligando as plaquetas
No primeiro grupo de experimentos, os cientistas mediram sinais químicos no sangue conhecidos por ativar plaquetas. Dois deles, chamados PAF e TXB2, aumentaram fortemente no primeiro dia e novamente por volta do quinto dia — espelhando a janela de alto risco quando os problemas tardios tipicamente surgem. Para testar causa e efeito, eles então estimularam as plaquetas. Quando camundongos receberam PAF extra logo após o sangramento, muitos morreram e seus cérebros ficaram mais preenchidos de microtrombos. Administrar PAF alguns dias depois, durante a fase de recuperação “silenciosa”, não matou os animais, mas causou piores escores neurológicos, mais déficits tardios e maior carga de microcoágulos. Camundongos geneticamente predispostos à ativação plaquetária tardia exibiram um padrão semelhante: recuperação inicial comum seguida de maior taxa de déficits de aparecimento tardio.
Remover ou acalmar as plaquetas
Se acelerar a atividade das plaquetas piorou a situação, diminuir sua ação poderia ajudar? Para descobrir, a equipe usou camundongos modificados cujas plaquetas podiam ser removidas seletivamente com uma toxina administrada antes da hemorragia. Esses animais não sangraram mais nem tiveram maior mortalidade, mas apresentaram menos microtrombos, melhor função neurológica precoce e chance marcadamente menor de declínio tardio em comparação com camundongos normais. Como remover plaquetas por completo seria inseguro em humanos, os pesquisadores também testaram vários fármacos existentes que bloqueiam diferentes receptores plaquetários — os pontos de ancoragem pelos quais vários sinais ativam essas células ou as fazem aderir entre si. Muitos desses medicamentos melhoraram o comportamento precoce e reduziram os microcoágulos, mas apenas um, o tirofiban, que bloqueia um receptor chave de “agregação” chamado GPIIb/IIIa, reduziu claramente a taxa de déficits tardios a longo prazo em fêmeas.
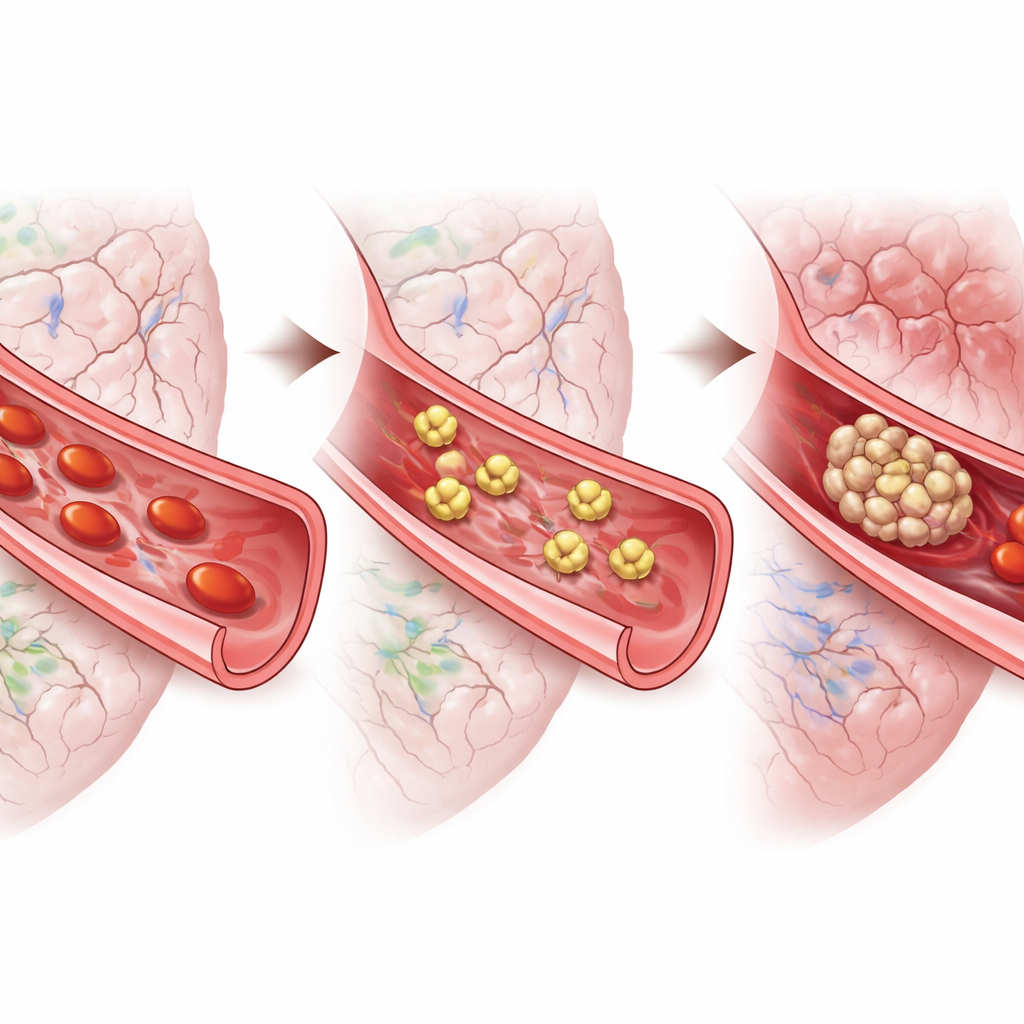
De camundongos para humanos
Para aproximar os achados da doença humana, os investigadores coletaram plaquetas de pacientes que sofreram hemorragia subaracnoide aneurismática. Ao microscópio, essas células estavam altamente ativadas e espalhadas, consistente com um estado de coagulação com gatilho sensível. Adicionar tirofiban às amostras tornou as plaquetas muito menos propensas a se espalhar, tanto nos primeiros dias após o sangramento quanto mais tarde, durante a janela de alto risco para complicações tardias. Outro medicamento que mirava um receptor plaquetário diferente teve pouco efeito. Juntando-se aos resultados em camundongos, esses testes sugerem que bloquear a agregação plaquetária, em vez de apenas atenuar alguns sinais de ativação, pode ser a estratégia mais promissora.
O que isso significa para tratamentos futuros
Este trabalho constrói um caso sólido de que as plaquetas fazem mais do que vedar a ruptura inicial após uma hemorragia cerebral: dias depois, elas ajudam a formar aglomerados de microcoágulos que bloqueiam os menores vasos do cérebro e preparam o terreno para AVCs tardios. Em camundongos, remover plaquetas ou bloquear seu principal receptor “de velcro” reduziu drasticamente essas lesões tardias, e um medicamento já usado em outros contextos, o tirofiban, também conteve a hiperativação plaquetária de pacientes humanos em laboratório. Embora qualquer tratamento antiplaquetário deva ser equilibrado com o risco de sangramento aumentado, o estudo oferece uma prova de conceito clara de que fármacos bloqueadores de plaquetas cuidadosamente direcionados poderiam, um dia, ajudar a proteger sobreviventes de hemorragia subaracnoide aneurismática contra uma perigosa segunda onda de dano cerebral.
Citação: Dienel, A., Hong, SH., Torres, K. et al. Platelets cause microvascular occlusion and delayed neurological deficits after subarachnoid hemorrhage in mice. Exp Mol Med 58, 1242–1253 (2026). https://doi.org/10.1038/s12276-026-01696-1
Palavras-chave: hemorragia subaracnoide, plaquetas, microtrombos, isquemia cerebral tardia, terapia antiplaquetária