Clear Sky Science · fr
Les plaquettes provoquent une occlusion microvasculaire et des déficits neurologiques retardés après une hémorragie sous‑arachnoïdienne chez la souris
Quand une hémorragie cérébrale frappe une seconde fois
Survivre à la rupture d’un anévrisme cérébral n’est que la première épreuve pour de nombreux patients. Quelques jours après la saignée initiale, près de la moitié développent de nouveaux problèmes neurologiques souvent dévastateurs, comme de la confusion, une faiblesse ou des symptômes de type AVC. Les cliniciens qualifient ces troubles de déficits neurologiques retardés, et jusqu’à présent, le déclencheur exact restait obscur. Cette étude chez la souris, étayée par des tests sur du sang humain, désigne un coupable surprenant : de minuscules cellules sanguines appelées plaquettes qui, normalement, aident à arrêter le saignement mais, dans ce contexte, semblent boucher les plus fins vaisseaux du cerveau et étouffer l’apport sanguin vital.
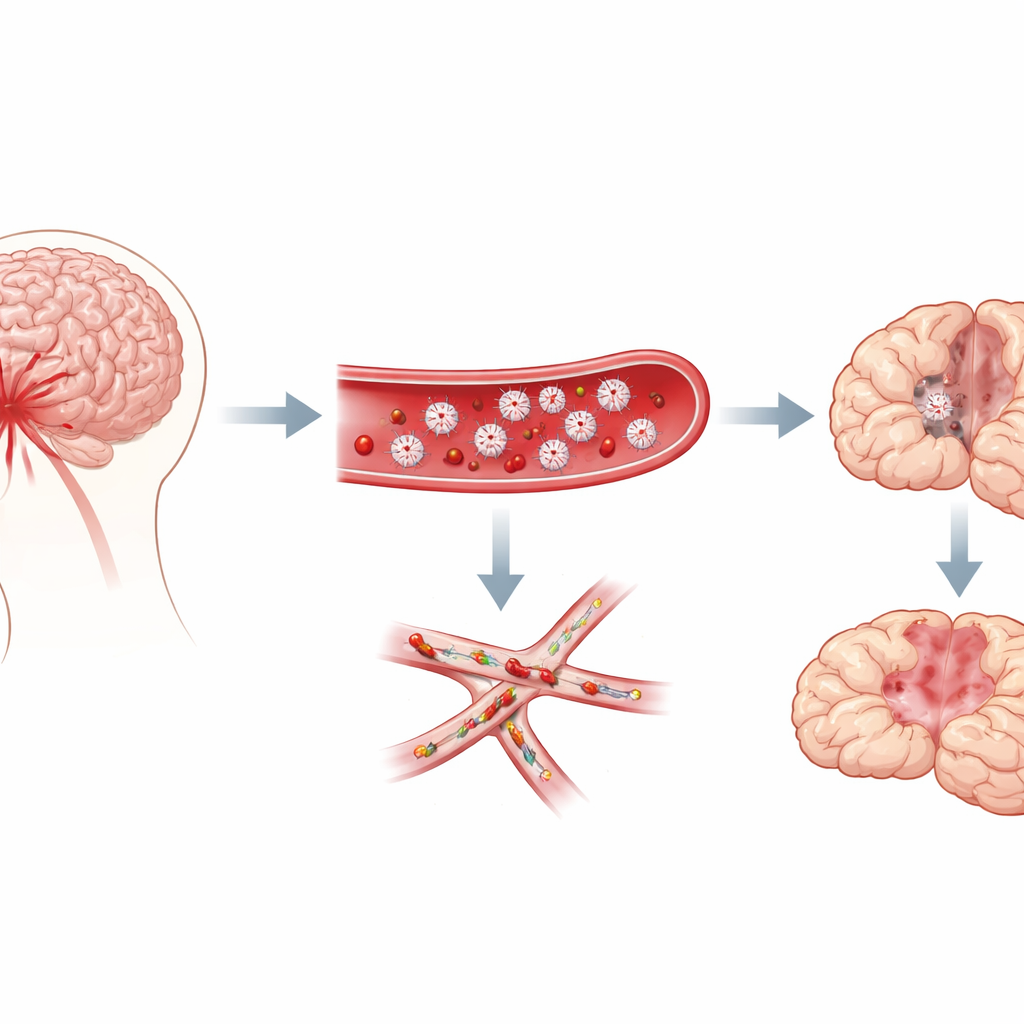
Petits caillots dans les plus petits vaisseaux du cerveau
Les chercheurs se sont concentrés sur l’hémorragie sous‑arachnoïdienne, un type de saignement qui inonde l’espace autour du cerveau après la rupture d’un anévrisme. Les cliniciens observent depuis longtemps que les patients qui développeront des troubles retardés présentent souvent des signes d’un état prothrombotique, et les autopsies montrent d’innombrables « microthrombi » — des caillots microscopiques — parsemant le cerveau. Ces caillots sont riches en plaquettes. Il n’était cependant pas clair si les plaquettes causaient réellement les lésions retardées ou si elles n’étaient que des témoins. En utilisant un modèle murin bien établi de cette hémorragie, l’équipe a suivi comportement et pathologie cérébrale sur une semaine, pour savoir si l’activité plaquettaire coïncidait avec l’apparition des déficits retardés.
Activer et désactiver les plaquettes
Dans la première série d’expériences, les scientifiques ont mesuré des signaux chimiques dans le sang connus pour réveiller les plaquettes. Deux d’entre eux, appelés PAF et TXB2, ont fortement augmenté au jour un puis de nouveau autour du jour cinq — reflétant la fenêtre à haut risque où apparaissent typiquement les problèmes retardés. Pour tester la causalité, ils ont ensuite stimulé davantage les plaquettes. Lorsque des souris ont reçu du PAF peu après la saignée, beaucoup sont mortes et leur cerveau a été davantage encombré de microthrombi. Administrer du PAF quelques jours plus tard, durant la phase « silencieuse » de récupération, n’a pas tué les animaux mais a aggravé les scores neurologiques, augmenté les déficits retardés et alourdi la charge en microcaillots. Des souris génétiquement prédisposées à une activation plaquettaire retardée ont montré un schéma similaire : une récupération précoce ordinaire suivie d’un taux plus élevé de déficits apparaissant tardivement.
Éliminer ou calmer les plaquettes
Si stimuler les plaquettes aggravait la situation, réduire leur activité pouvait‑il aider ? Pour le savoir, l’équipe a utilisé des souris modifiées dont les plaquettes pouvaient être retirées sélectivement par une toxine administrée avant l’hémorragie. Ces animaux ne saignaient pas davantage et ne mouraient pas plus, mais ils présentaient moins de microthrombi, une meilleure fonction neurologique précoce et une probabilité nettement réduite de déclin retardé par rapport aux souris normales. Parce que supprimer totalement les plaquettes serait dangereux chez l’humain, les chercheurs ont aussi testé plusieurs médicaments existants qui bloquent différents récepteurs plaquettaires — les points d’ancrage par lesquels divers signaux activent ces cellules ou les font s’agréger. Nombre de ces médicaments ont amélioré le comportement précoce et diminué les microcaillots, mais un seul, le tirofiban, qui bloque un récepteur clé de l’« agrégation » appelé GPIIb/IIIa, a clairement réduit le taux à long terme de déficits retardés chez les souris femelles.
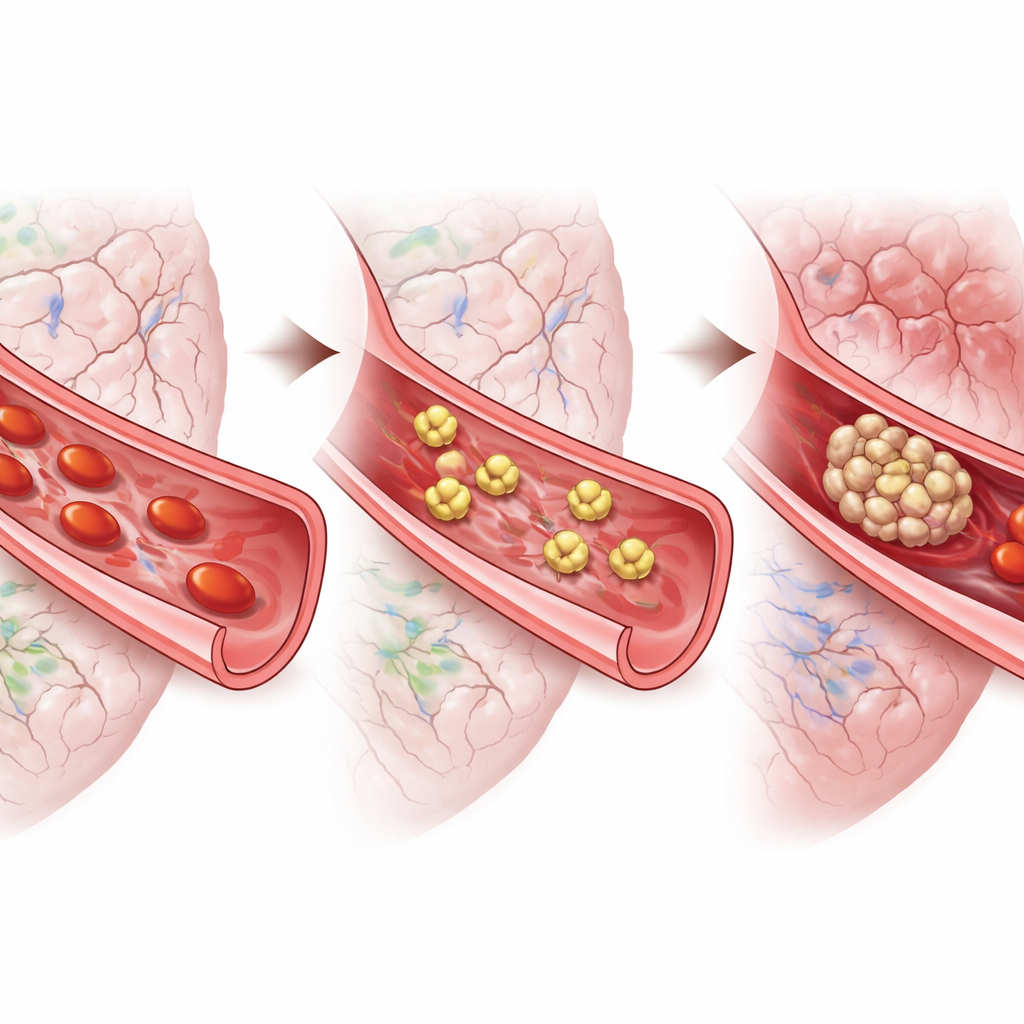
Des souris aux humains
Pour rapprocher ces résultats de la maladie humaine, les investigateurs ont prélevé des plaquettes chez des patients ayant subi une hémorragie sous‑arachnoïdienne anévrysmale. Au microscope, ces cellules étaient fortement activées et étalées, cohérent avec un état d’hypercoagulabilité. L’ajout de tirofiban aux échantillons rendait les plaquettes beaucoup moins enclines à s’étaler, tant dans les premiers jours après la saignée que plus tard, pendant la fenêtre à haut risque de complications retardées. Un autre médicament ciblant un récepteur plaquettaire différent avait peu d’effet. Avec les résultats chez la souris, ces tests suggèrent que bloquer l’agrégation plaquettaire, plutôt que d’atténuer seulement certains signaux d’activation, pourrait être la stratégie la plus prometteuse.
Ce que cela implique pour les traitements futurs
Ce travail fournit des arguments solides montrant que les plaquettes font plus que colmater la rupture initiale après une hémorragie cérébrale : quelques jours plus tard, elles contribuent à former des amas de petits caillots qui bloquent les plus petits vaisseaux du cerveau et préparent le terrain pour des AVC retardés. Chez la souris, éliminer les plaquettes ou bloquer leur principal récepteur « Velcro » a fortement réduit ces lésions retardées, et un médicament déjà utilisé dans d’autres contextes, le tirofiban, a également calmé les plaquettes hyperactives prélevées chez des patients en laboratoire. Bien que tout traitement antiplaquettaire doive être pesé contre le risque d’aggravation du saignement, l’étude offre une preuve de concept claire que des médicaments ciblant précisément l’agrégation plaquettaire pourraient un jour aider à protéger les survivants d’une hémorragie sous‑arachnoïdienne anévrysmale d’une dangereuse seconde vague de lésions cérébrales.
Citation: Dienel, A., Hong, SH., Torres, K. et al. Platelets cause microvascular occlusion and delayed neurological deficits after subarachnoid hemorrhage in mice. Exp Mol Med 58, 1242–1253 (2026). https://doi.org/10.1038/s12276-026-01696-1
Mots-clés: hémorragie sous‑arachnoïdienne, plaquettes, microthrombi, ischémie cérébrale retardée, thérapie antiplaquettaire