Clear Sky Science · sv
Blodplättar orsakar mikrovaskulär ocklusion och fördröjda neurologiska försämringar efter subaraknoidalblödning hos möss
När en hjärnblödning slår till två gånger
Att överleva en sprucken hjärnaneurysm är bara det första hindret för många patienter. Dagar efter den första blödningen utvecklar ungefär hälften nya, ofta förödande, neurologiska problem som förvirring, svaghet eller stroke-liknande symtom. Läkare kallar detta fördröjda neurologiska försämringar, och fram tills nu har den exakta utlösaren varit oklar. Denna studie i möss, med stödjande tester på mänskligt blod, pekar ut en överraskande bov: små blodceller kallade blodplättar som normalt hjälper till att stoppa blödning men som i detta sammanhang tycks täppa igen hjärnans finaste kärl och kväva viktigt blodflöde.
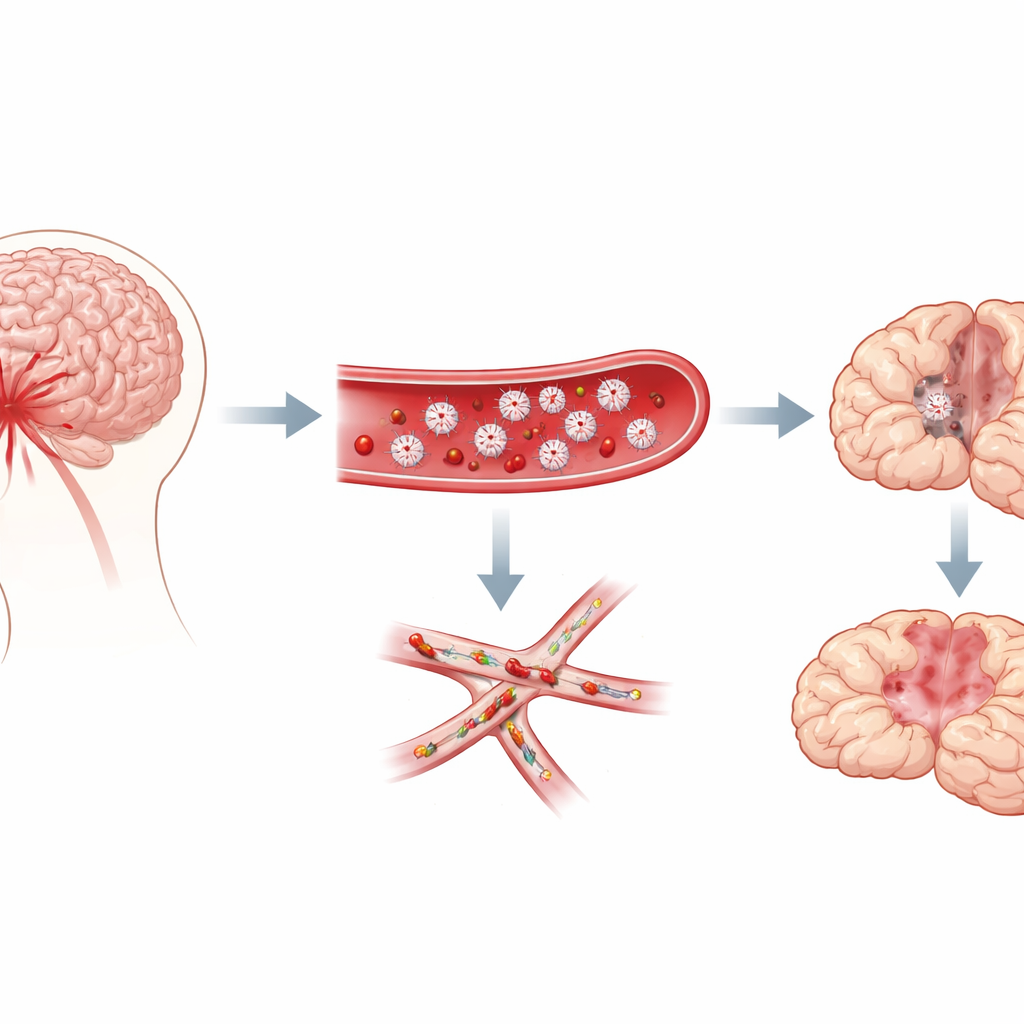
Små koagler i hjärnans minsta kärl
Forskarna fokuserade på subaraknoidalblödning, en typ av blödning som fyller utrymmet runt hjärnan efter att en aneurysm brustit. Kliniker har länge noterat att patienter som senare får fördröjda problem ofta visar tecken på att deras blod är ovanligt benäget att koagulera, och obduktioner avslöjar otaliga ”mikrotromber” — punktformiga koagler — utspridda i hjärnan. Dessa koagler är rika på blodplättar. Ändå var det oklart om blodplättar faktiskt orsakar den fördröjda skadan eller bara är åskådare. Med hjälp av en väletablerad musmodell av denna blödning följde teamet både beteende och hjärnpatologi under en vecka för att undersöka om blodplättsaktivitet samspelade med uppkomsten av fördröjda försämringar.
Slå av och på blodplättarna
I den första serien experiment mätte forskarna kemiska signaler i blodet som är kända för att väcka blodplättar. Två, kallade PAF och TXB2, steg markant dag ett och återigen runt dag fem — vilket speglade det riskfönster då fördröjade problem vanligtvis uppträder. För att testa orsak och verkan pressade de sedan blodplättarna hårdare. När möss fick extra PAF strax efter blödningen dog många och deras hjärnor fylldes av fler mikrotromber. Att ge PAF några dagar senare, under den ”tysta” återhämtningsfasen, dödade inte djuren men gav sämre neurologiska poäng, fler fördröjda försämringar och större börda av mikrotromber. Möss genetiskt benägna att få fördröjd blodplättsaktivering visade ett liknande mönster: normalt tidigt tillfrisknande följt av en högre frekvens av sena uppträdande försämringar.
Ta bort eller lugna blodplättarna
Om att öka blodplättsaktivitet förvärrade tillståndet, kunde att dämpa dem hjälpa? För att ta reda på det använde teamet manipulerade möss vars blodplättar selektivt kunde avlägsnas med ett toxin givet före blödningen. Dessa djur blödde inte mer eller dog oftare, men de hade färre mikrotromber, bättre tidig neurologisk funktion och en markant lägre sannolikhet för fördröjd försämring än normala möss. Eftersom att ta bort blodplättar helt vore osäkert hos människor testade forskarna också flera befintliga läkemedel som blockerar olika blodplättsreceptorer — de infästningspunkter genom vilka olika signaler aktiverar dessa celler eller får dem att klibba ihop. Många av dessa läkemedel förbättrade tidigt beteende och minskade mikrotromber, men endast ett, tirofiban, som blockerar en viktig ”aggregations”receptor kallad GPIIb/IIIa, minskade tydligt den långsiktiga frekvensen av fördröjda försämringar hos honor.
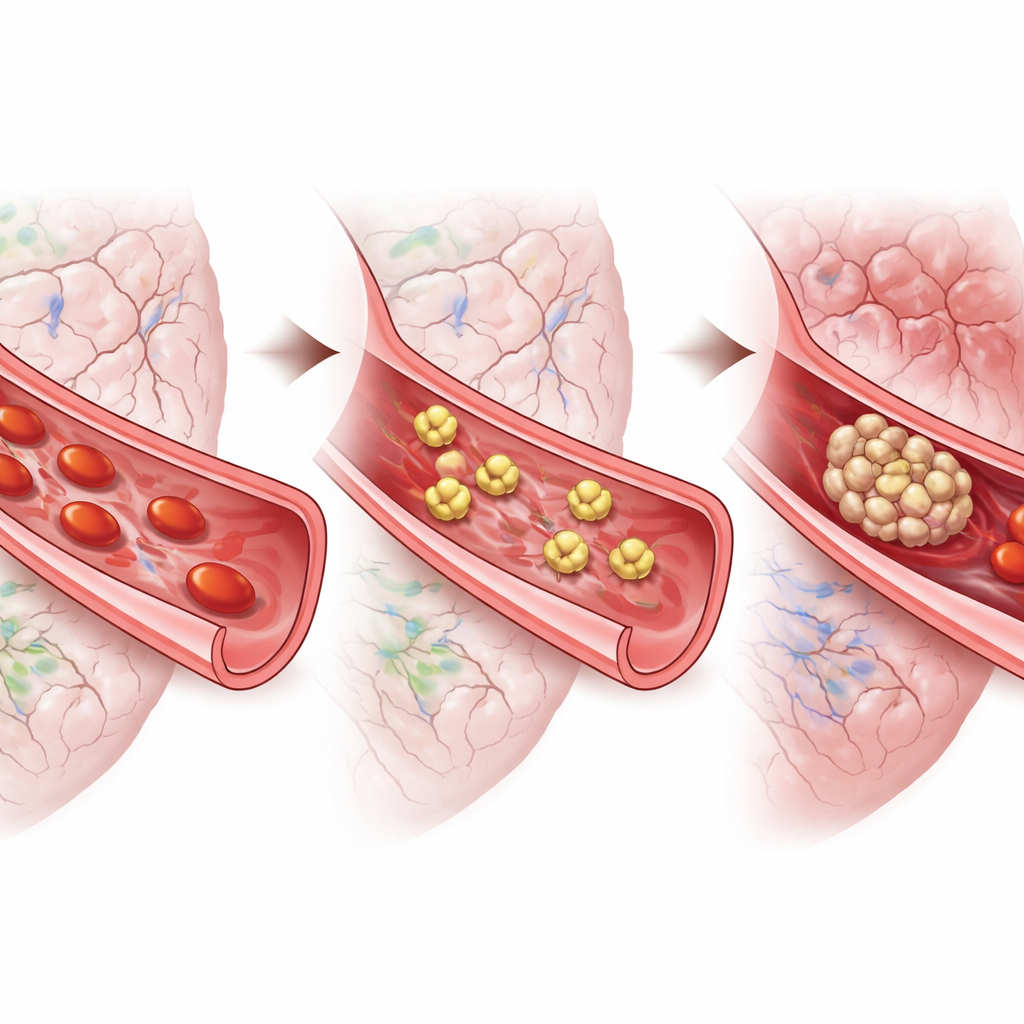
Från möss till människor
För att överbrygga gapet till mänsklig sjukdom samlade forskarna blodplättar från patienter som drabbats av aneurysmal subaraknoidalblödning. Under mikroskopet var dessa celler starkt aktiverade och utspända, vilket stämmer med ett känsligt koagulationstillstånd. Att tillsätta tirofiban till proverna gjorde blodplättarna mycket mindre benägna att sprida ut sig, både under de första dagarna efter blödningen och senare under det hög-riskfönster som är förknippat med fördröjade komplikationer. Ett annat preparat som riktade sig mot en annan blodplättsreceptor hade liten effekt. Tillsammans med musresultaten tyder dessa tester på att blockering av blodplättsaggregation, snarare än enbart dämpning av vissa aktiveringssignaler, kan vara den mest lovande strategin.
Vad detta innebär för framtida behandling
Detta arbete bygger ett starkt fall för att blodplättar gör mer än att täppa igen den initiala rupturen efter en hjärnblödning: dagar senare hjälper de till att bilda kluster av små koagler som blockerar hjärnans minsta kärl och banar väg för fördröjda stroke-liknande skador. Hos möss minskade borttagning av blodplättar eller blockering av deras viktigaste ”Velcro”-receptor dessa fördröjda skador kraftigt, och ett läkemedel som redan används i andra sammanhang, tirofiban, dämpade också överaktiva blodplättar från mänskliga patienter i laboratoriet. Medan varje antitrombocytbehandling måste vägas mot risken för ökad blödning erbjuder studien ett tydligt proof-of-concept att noggrant riktade blodplättsblockerande läkemedel en dag skulle kunna hjälpa överlevare av aneurysmal subaraknoidalblödning att undvika en farlig andra våg av hjärnskador.
Citering: Dienel, A., Hong, SH., Torres, K. et al. Platelets cause microvascular occlusion and delayed neurological deficits after subarachnoid hemorrhage in mice. Exp Mol Med 58, 1242–1253 (2026). https://doi.org/10.1038/s12276-026-01696-1
Nyckelord: subaraknoidalblödning, blodplättar, mikro-tromber, fördröjd cerebral ischemia, antitrombocytbehandling