Clear Sky Science · he
טסיות דם גורמות לסתימת מיקרו־כלי ותסמינים נוירולוגיים מאוחרים לאחר דימום תת־עכבישי בעכברים
כאשר דימום מוחי פוגע פעמיים
להישרדות מקרע של אנאוריזמה במוח יש משמעות בלבד כמכשול ראשון עבור רבים מהמטופלים. ימים לאחר הדימום הראשוני, בערך מחצית נוטים לפתח בעיות נוירולוגיות חדשות ולעתים הרסניות כגון בלבול, חולשה או תסמינים בדמיון לשבץ. רופאים מכנים זאת ליקויים נוירולוגיים מאוחרים, ועד כה הטריגר המדויק נותר מעורפל. המחקר הזה בעכברים, עם בדיקות תומכות על דם אנושי, מאתר נבל מפתיע: תאי דם זעירים שנקראים טסיות, שבדרך כלל עוזרות לעצור דימום, אך בהקשר הזה נראה כי הם סותמות את כלי הדם הקטנים ביותר במוח וחוסמות זרימת דם חיונית.
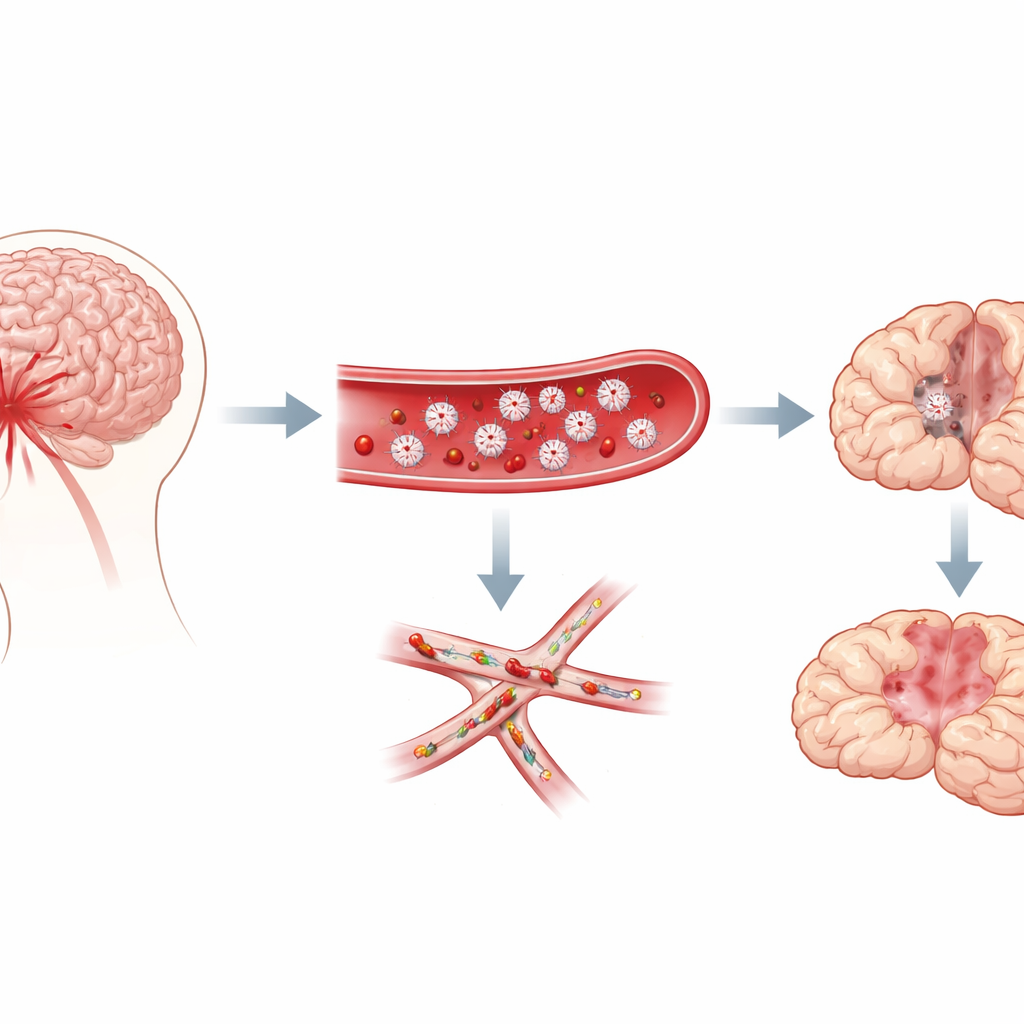
קרישים זעירים בכלי הדם הקטנים ביותר של המוח
החוקרים התרכזו בדימום תת־עכבישי, סוג של דימום שממלא את המרחב סביב המוח לאחר קרע אנאוריזמה. קלינאים רואים כבר זמן רב כי מטופלים שמפתחים לאחר מכן בעיות מאוחרות לעתים מראים סימנים לכך שהדם שלהם נוטה לקרישה יתר על המידה, ונתיחי מוח מגלים אינספור "מיקרו־קרישי"—קרישי נקודה—מרוכזים ברחבי המוח. קרישים אלה עשירים בטסיות. עם זאת, לא היה ברור האם הטסיות גורמות לנזק המאוחר או סתם מופיעות כצופים. באמצעות מודל עכבר מבוסס של דימום זה, הצוות עקב גם אחר ההתנהגות וגם אחר פתולוגיית המוח במשך שבוע, ושאל האם פעילות הטסיות תואמת להופעת הליקויים המאוחרים.
הפעלה וכיבוי של טסיות
בסט הניסויים הראשון המדענים מדדו אותות כימיים בדם הידועים כמעוררים טסיות. שניים מהם, הנקראים PAF ו‑TXB2, עלו בחדות ביום הראשון ושוב סביב היום החמישי—מה שמשקף את חלון הסיכון הגבוה בו בדרך כלל מופיעים הבעיות המאוחרות. כדי לבדוק סיבתיות, הם דחפו את הטסיות חזק יותר. כאשר עכברים קיבלו PAF נוסף זמן קצר לאחר הדימום, רבים מתו ומוחותיהם התמלאו ביותר מיקרו־קרישי. מתן PAF כמה ימים מאוחר יותר, במהלך שלב ההתאוששות ה"שקט", לא הרג את בעלי החיים אך גרם לציוני נוירולוגיה גרועים יותר, ליותר ליקויים מאוחרים ועומס כבד יותר של מיקרו־קרישים. לעכברים בעלי נטייה גנטית להפעלת טסיות מאוחרת נצפה דפוס דומה: התאוששות מוקדמת רגילה שאחריה שיעור גבוה יותר של ליקויים שמופיעים מאוחר.
הסרה או הרגעת טסיות
אם הגברה של פעילות הטסיות החמירה את המצב, האם הפחתתן תעזור? כדי לבדוק זאת השתמשו הצוות בעכברים מהונדסים שבהם ניתן להסיר טסיות באופן סלקטיבי באמצעות רעל שניתן לפני הדימום. בעלי החיים האלה לא דיממו יותר ולא מתו בשיעור גבוה יותר, אך היה להם פחות מיקרו־קרישי, תפקוד נוירולוגי מוקדם טוב יותר והסתברות נמוכה משמעותית לירידה מאוחרת מאשר בעכברים רגילים. משום שהסרת כל הטסיות לחלוטין תהיה מסוכנת בבני אדם, החוקרים גם בדקו מספר תרופות קיימות החוסמות קולטנים שונים של טסיות—נקודות עגינה דרכן אותות שונים מפעילים תאים אלה או גורמים להיצמדות ביניהם. רבות מהתרופות הללו שיפרו את ההתנהגות המוקדמת וצמצמו את המיקרו־הקרישים, אך רק אחת, טירופיובן, שחוסמת קולטור אגירה מרכזי הנקרא GPIIb/IIIa, הורידה בצורה ברורה את שיעור ההופעה המאוחרת של ליקויים בעכברות.
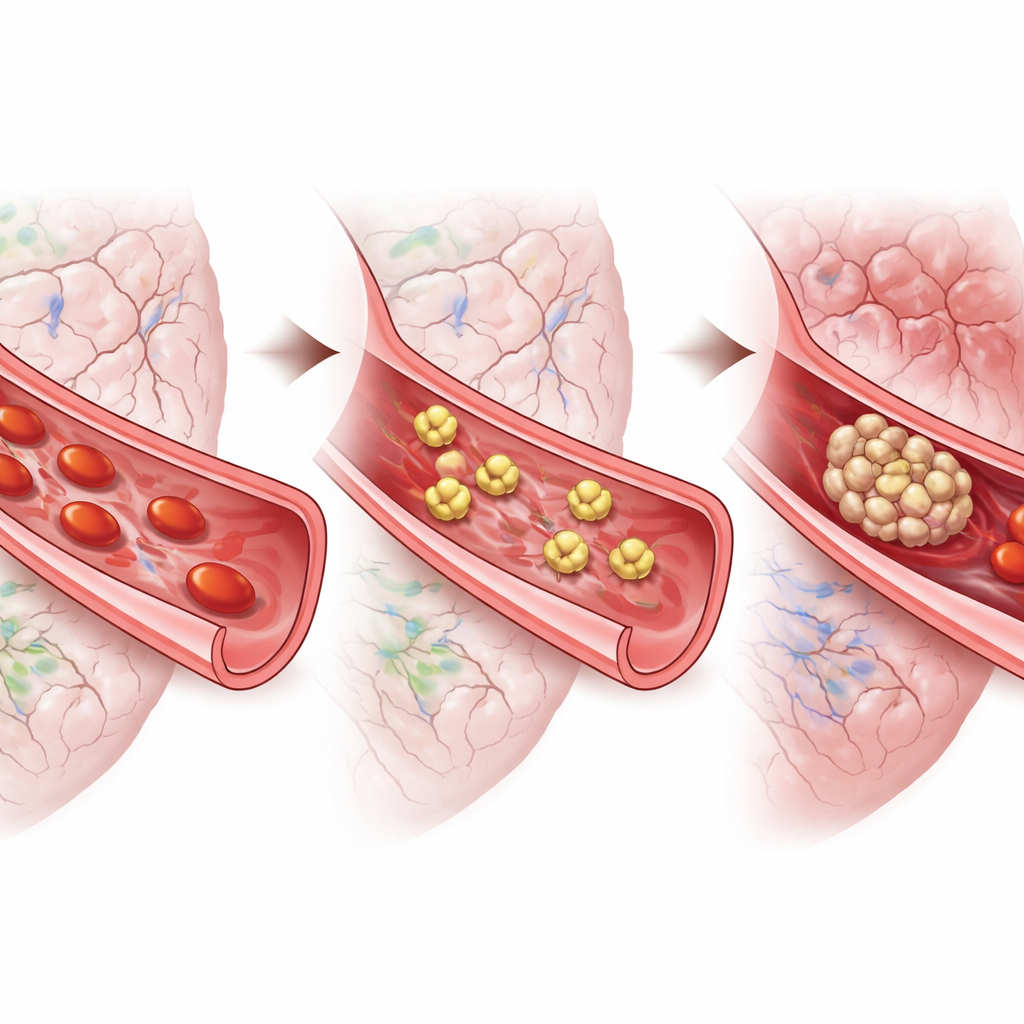
מעכברים לבני אדם
כדי לגשר אל המחלה האנושית, החוקרים אספו טסיות מחולים שסבלו מדימום תת־עכבישי אנאוריזמלי. תחת מיקרוסקופ, תאים אלה היו במצב הפעלה גבוה ומתפרשים, תואם למצב קרישה רגיש. הוספת טירופיובן לדגימות הפכה את הטסיות לפחות מועדות להתפשטות, הן בימים הראשונים לאחר הדימום והן מאוחר יותר במהלך חלון הסיכון להופעות מאוחרות. תרופה אחרת המיועדת לקולטן טסיות שונה הראתה השפעה מועטה. יחד עם התוצאות מהעכברים, הממצאים האלה מצביעים על כך שהחסימה של הידבקות הטסיות, ולא רק על דיכוי חלק מאותות ההפעלה, עשויה להיות האסטרטגיה המבטיחה ביותר.
מה המשמעות לטיפול עתידי
עבודה זו בונה טיעון חזק לכך שטסיות עושות יותר מאשר לסתום את הקרע הראשוני לאחר דימום מוחי: ימים אחר כך הן מסייעות ליצור צרורות של קרישים זעירים החוסמים את כלי הדם הקטנים ביותר במוח ומכינים את הבמה לשבצים מאוחרים. בעכברים, הסרת טסיות או חסימת קולטור ה"וולקרו" העיקרי שלהן צמצמו באופן חד את הפגיעות המאוחרות, ותרופה שכבר בשימוש בהקשרים אחרים, טירופיובן, גם הרגעה טסיות פעילות יתר ממטופלים אנושיים במעבדה. למרות שכל טיפול נוגד־טסיות צריך לאזן בין הסיכון לדימום מוגבר, המחקר מציע הוכחת עקרון ברורה שהתרופות החוסמות טסיות באופן ממוקד יכולות יום אחד לסייע להגן על שורדי דימום תת־עכבישי אנאוריזמלי מפני גל שני מסוכן של נזק מוחי.
ציטוט: Dienel, A., Hong, SH., Torres, K. et al. Platelets cause microvascular occlusion and delayed neurological deficits after subarachnoid hemorrhage in mice. Exp Mol Med 58, 1242–1253 (2026). https://doi.org/10.1038/s12276-026-01696-1
מילות מפתח: דימום תת־עכבישי, טסיות דם, מיקרו־קרישים, איסכמיה מוחית מאוחרת, טיפול נוגד־טסיות