Clear Sky Science · es
Las plaquetas causan oclusión microvascular y déficits neurológicos diferidos tras una hemorragia subaracnoidea en ratones
Cuando una hemorragia cerebral golpea por segunda vez
Sobrevivir a la ruptura de un aneurisma cerebral es solo el primer escollo para muchos pacientes. Días después del sangrado inicial, aproximadamente la mitad desarrolla nuevos y a menudo devastadores problemas neurológicos como confusión, debilidad o síntomas semejantes a un ictus. Los médicos denominan a esto déficits neurológicos diferidos, y hasta ahora el desencadenante exacto ha permanecido oscuro. Este estudio en ratones, con pruebas complementarias en sangre humana, señala a un villano sorprendente: unas células sanguíneas diminutas llamadas plaquetas que normalmente ayudan a detener el sangrado pero que, en este contexto, parecen obstruir los vasos más finos del cerebro y cortar el flujo sanguíneo vital.
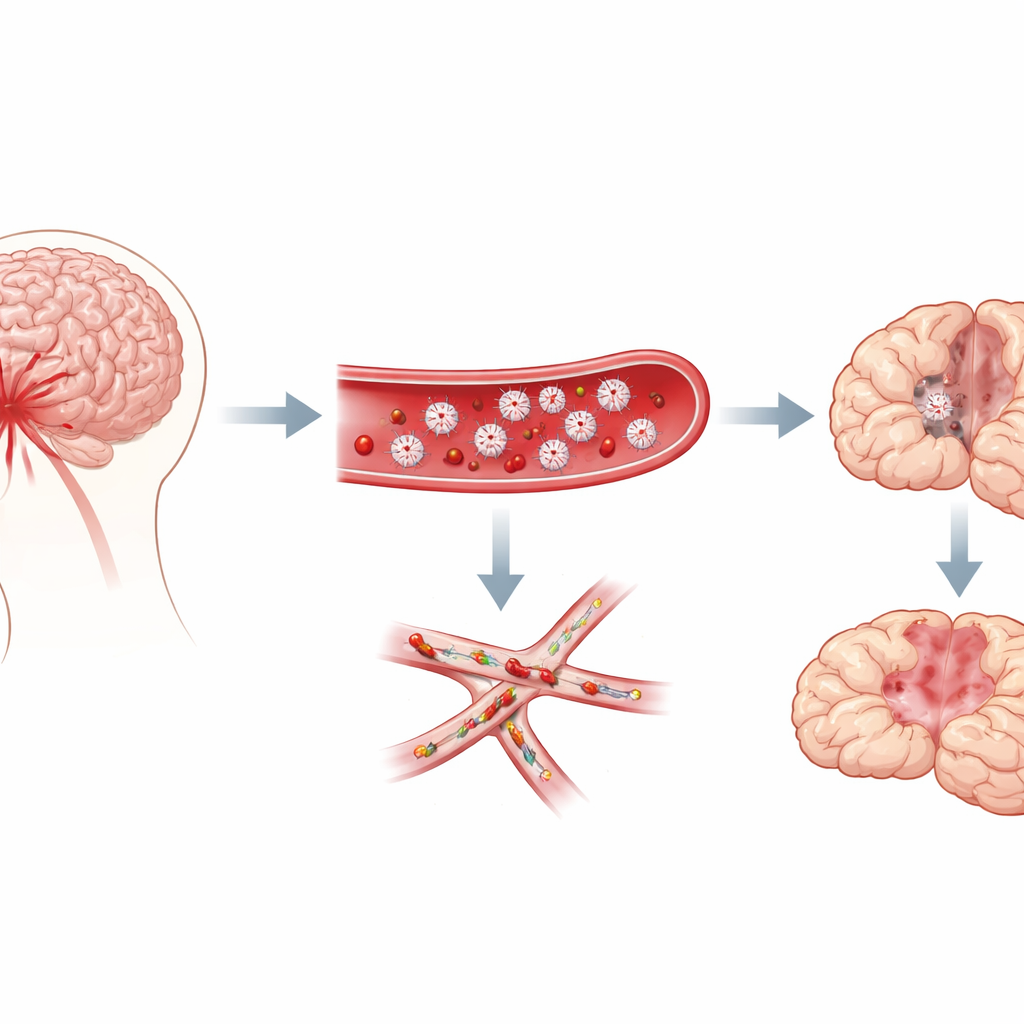
Microcoágulos en los vasos más pequeños del cerebro
Los investigadores se centraron en la hemorragia subaracnoidea, un tipo de sangrado que inunda el espacio alrededor del cerebro tras la ruptura de un aneurisma. Los clínicos han observado desde hace tiempo que los pacientes que desarrollan problemas diferidos suelen mostrar señales de que su sangre tiende a coagularse con más facilidad, y las autopsias revelan numerosos “microtrombos”, coágulos diminutos, repartidos por el cerebro. Estos coágulos son ricos en plaquetas. Sin embargo, no quedaba claro si las plaquetas provocaban realmente el daño diferido o simplemente estaban presentes como espectadores. Usando un modelo murino bien establecido de esta hemorragia, el equipo siguió tanto el comportamiento como la patología cerebral durante una semana, preguntándose si la actividad plaquetaria coincidía con la aparición de los déficits diferidos.
Encender y apagar las plaquetas
En la primera serie de experimentos, los científicos midieron señales químicas en la sangre conocidas por activar plaquetas. Dos de ellas, llamadas PAF y TXB2, aumentaron bruscamente el día uno y de nuevo alrededor del día cinco, reflejando la ventana de alto riesgo cuando habitualmente aparecen los problemas diferidos. Para probar causalidad, luego estimularon más a las plaquetas. Cuando los ratones recibieron PAF adicional poco después del sangrado, muchos murieron y sus cerebros se llenaron de más microtrombos. Administrar PAF unos días más tarde, durante la fase de recuperación “silenciosa”, no mató a los animales pero sí empeoró las puntuaciones neurológicas, aumentó los déficits diferidos y elevó la carga de microcoágulos. Ratones genéticamente predispuestos a una activación plaquetaria tardía mostraron un patrón similar: una recuperación temprana ordinaria seguida de una mayor tasa de déficits de aparición tardía.
Eliminar o calmar las plaquetas
Si aumentar la actividad plaquetaria empeoraba las cosas, ¿reducirla podría ayudar? Para averiguarlo, el equipo usó ratones modificados cuyas plaquetas podían eliminarse selectivamente con una toxina administrada antes de la hemorragia. Estos animales no sangraron más ni murieron con mayor frecuencia, pero presentaron menos microtrombos, mejor función neurológica temprana y una probabilidad notablemente menor de deterioro diferido que los ratones normales. Dado que eliminar por completo las plaquetas sería inseguro en personas, los investigadores también probaron varios fármacos existentes que bloquean distintos receptores plaquetarios —los puntos de anclaje mediante los cuales diversas señales activan estas células o las hacen agregarse. Muchos de estos fármacos mejoraron el comportamiento temprano y redujeron los microcoágulos, pero solo uno, tirofibán, que bloquea un receptor clave de “agregación” llamado GPIIb/IIIa, redujo claramente la tasa a largo plazo de déficits diferidos en ratonas.
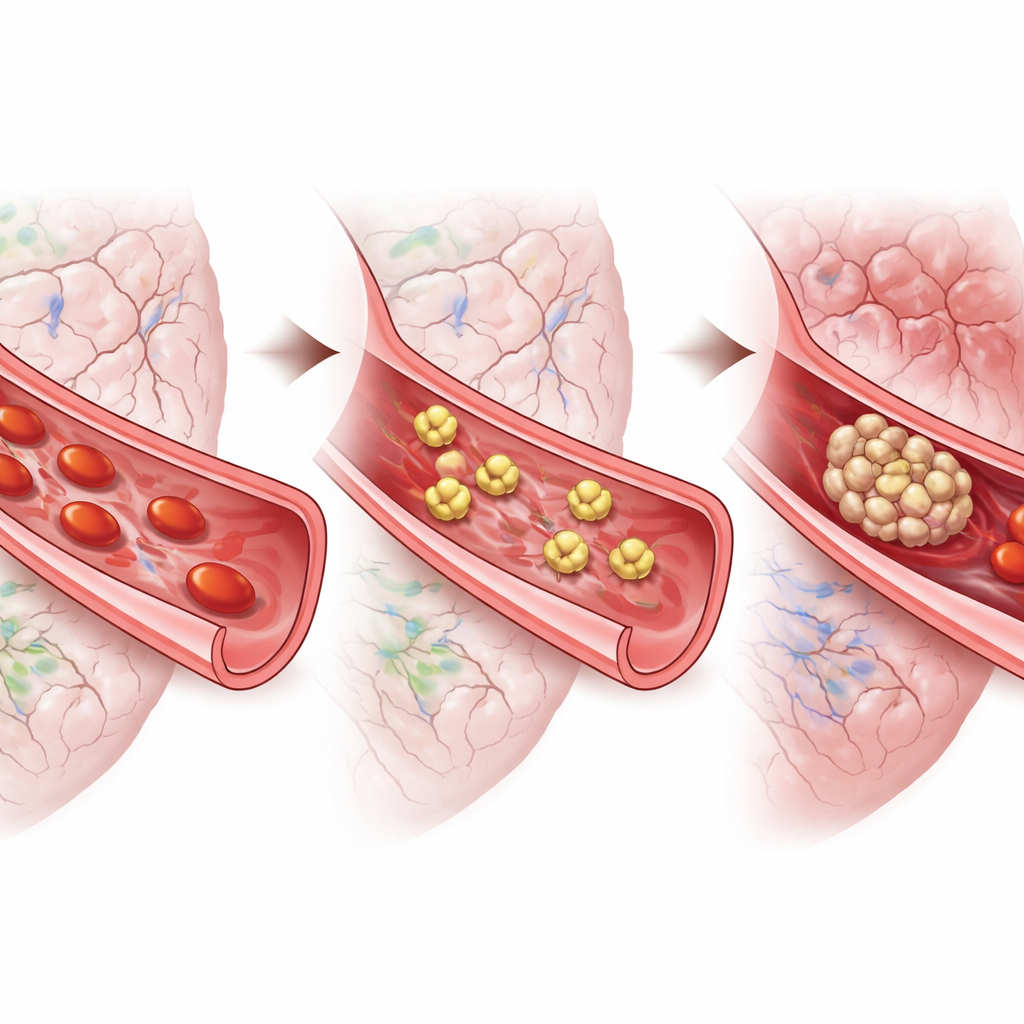
De los ratones a las personas
Para acercar los hallazgos a la enfermedad humana, los investigadores recogieron plaquetas de pacientes que habían sufrido una hemorragia subaracnoidea aneurismática. Bajo el microscopio, estas células estaban muy activadas y extendidas, coherente con un estado de coagulación de muy baja tolerancia. Añadir tirofibán a las muestras hizo que las plaquetas fueran mucho menos propensas a extenderse, tanto en los primeros días tras el sangrado como más tarde, durante la ventana de alto riesgo de complicaciones diferidas. Otro fármaco dirigido a un receptor plaquetario distinto tuvo poco efecto. Junto con los resultados en ratones, estas pruebas sugieren que bloquear la agregación plaquetaria, más que simplemente atenuar algunas señales de activación, podría ser la estrategia más prometedora.
Qué significa esto para tratamientos futuros
Este trabajo refuerza la hipótesis de que las plaquetas hacen más que taponar la ruptura inicial tras un sangrado cerebral: días después, contribuyen a formar racimos de microcoágulos que obstruyen los vasos más pequeños del cerebro y preparan el terreno para ictus diferidos. En ratones, eliminar las plaquetas o bloquear su principal receptor de “velcro” redujo con contundencia estas lesiones diferidas, y un fármaco ya usado en otros contextos, el tirofibán, también moderó la hiperactividad plaquetaria de pacientes humanos en el laboratorio. Aunque cualquier tratamiento antiplaquetario debe sopesarse frente al riesgo de más sangrado, el estudio ofrece una prueba de concepto clara de que fármacos dirigidos con precisión contra la agregación plaquetaria podrían algún día ayudar a proteger a los sobrevivientes de una hemorragia subaracnoidea aneurismática de una peligrosa segunda oleada de daño cerebral.
Cita: Dienel, A., Hong, SH., Torres, K. et al. Platelets cause microvascular occlusion and delayed neurological deficits after subarachnoid hemorrhage in mice. Exp Mol Med 58, 1242–1253 (2026). https://doi.org/10.1038/s12276-026-01696-1
Palabras clave: hemorragia subaracnoidea, plaquetas, microtrombos, isquemia cerebral diferida, terapia antiplaquetaria