Clear Sky Science · pl
Płytki krwi wywołują zamknięcie mikrokrążenia i opóźnione deficyty neurologiczne po krwotoku podpajęczynówkowym u myszy
Kiedy krwawienie mózgowe uderza po raz drugi
Przeżycie pęknięcia tętniaka mózgu to tylko pierwszy próg dla wielu pacjentów. Kilka dni po pierwotnym krwawieniu u około połowy pojawiają się nowe, często wyniszczające problemy neurologiczne, takie jak zaburzenia świadomości, osłabienie czy objawy przypominające udar. Lekarze nazywają to opóźnionymi deficytami neurologicznymi, a ich dokładny mechanizm przez długi czas pozostawał niejasny. Badanie na mysich modelach, wspierane badaniami na ludzkiej krwi, wskazuje zaskakującego winowajcę: drobne komórki krwi zwane płytkami, które normalnie pomagają zatrzymać krwawienie, lecz w tym kontekście wydają się zatykać najdrobniejsze naczynia mózgu i dusić jego dopływ krwi.
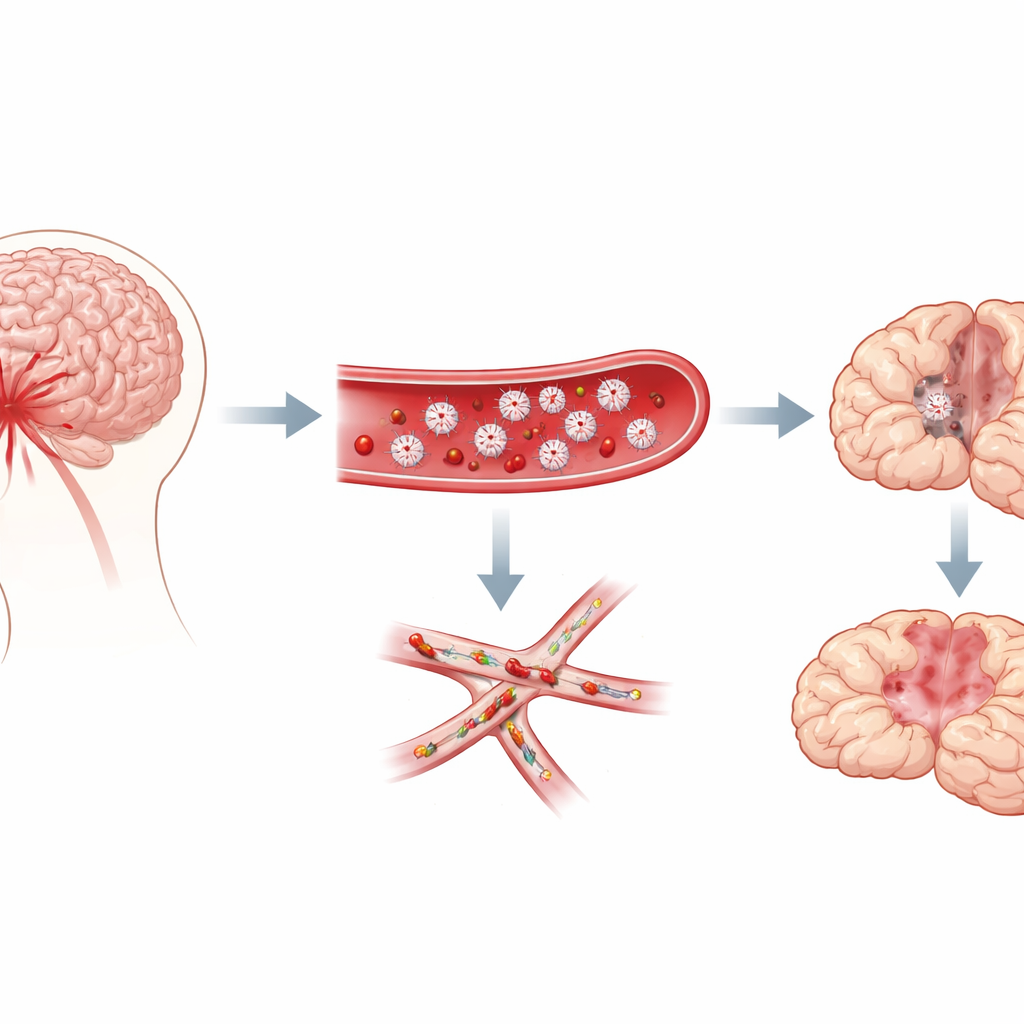
Maleńkie skrzepy w najmniejszych naczyniach mózgu
Naukowcy skupili się na krwotoku podpajęczynówkowym, rodzaju krwawienia, które zalewa przestrzeń wokół mózgu po pęknięciu tętniaka. Klinicyści od dawna zauważali, że pacjenci, u których później rozwijają się opóźnione problemy, często mają cechy krwi skłonnej do nadmiernego krzepnięcia, a sekcje zwłok ukazują liczne „mikrozakrzepy” — maleńkie skrzepy rozproszone po mózgu. Te skrzepy bogate są w płytki. Nie było jednak jasne, czy to płytki są przyczyną opóźnionych uszkodzeń, czy tylko się tam pojawiają. Wykorzystując dobrze opisany model krwotoku u myszy, zespół śledził zachowanie i patologię mózgu przez tydzień, badając, czy aktywność płytek koreluje z wystąpieniem opóźnionych deficytów.
Włączanie i wyłączanie płytek
W pierwszym szeregu eksperymentów badacze zmierzyli chemiczne sygnały we krwi, które są znane z pobudzania płytek. Dwa z nich, zwane PAF i TXB2, gwałtownie wzrosły w pierwszym dniu, a potem ponownie około piątego dnia — odzwierciedlając okno wysokiego ryzyka, kiedy zazwyczaj pojawiają się opóźnione problemy. Aby sprawdzić związek przyczynowo-skutkowy, następnie zwiększyli aktywność płytek. Kiedy myszy otrzymały dodatkowy PAF wkrótce po krwawieniu, wiele z nich zmarło, a ich mózgi wypełniły się większą ilością mikrozakrzepów. Podanie PAF kilka dni później, podczas „cichego” etapu rekonwalescencji, nie powodowało śmierci zwierząt, lecz pogarszało wyniki neurologiczne, zwiększało liczbę opóźnionych deficytów i obciążenie mikrozakrzepami. Myszy genetycznie predysponowane do opóźnionej aktywacji płytek wykazywały podobny wzorzec: zwykła wczesna regeneracja, a następnie większe występowanie późno pojawiających się deficytów.
Usuwanie lub uspokajanie płytek
Jeśli zwiększenie aktywności płytek pogarszało stan, czy ich stłumienie może pomóc? Aby to sprawdzić, zespół użył zmodyfikowanych myszy, których płytki można było selektywnie usunąć toksyną podaną przed krwotokiem. Te zwierzęta nie krwawiły więcej ani nie umierały częściej, ale miały mniej mikrozakrzepów, lepszą wczesną funkcję neurologiczną i znacznie niższe ryzyko opóźnionego pogorszenia w porównaniu z normalnymi myszami. Ponieważ całkowite pozbawienie płytek byłoby u ludzi niebezpieczne, badacze przetestowali też kilka dostępnych leków blokujących różne receptory płytek — miejsca przyłączania, przez które różne sygnały aktywują komórki lub powodują ich agregację. Wiele z tych leków poprawiało wczesne zachowanie i zmniejszało liczbę mikrozakrzepów, lecz tylko jeden, tirofiban, blokujący kluczowy receptor agregacji GPIIb/IIIa, wyraźnie zmniejszył długoterminową częstość opóźnionych deficytów u samic myszy.
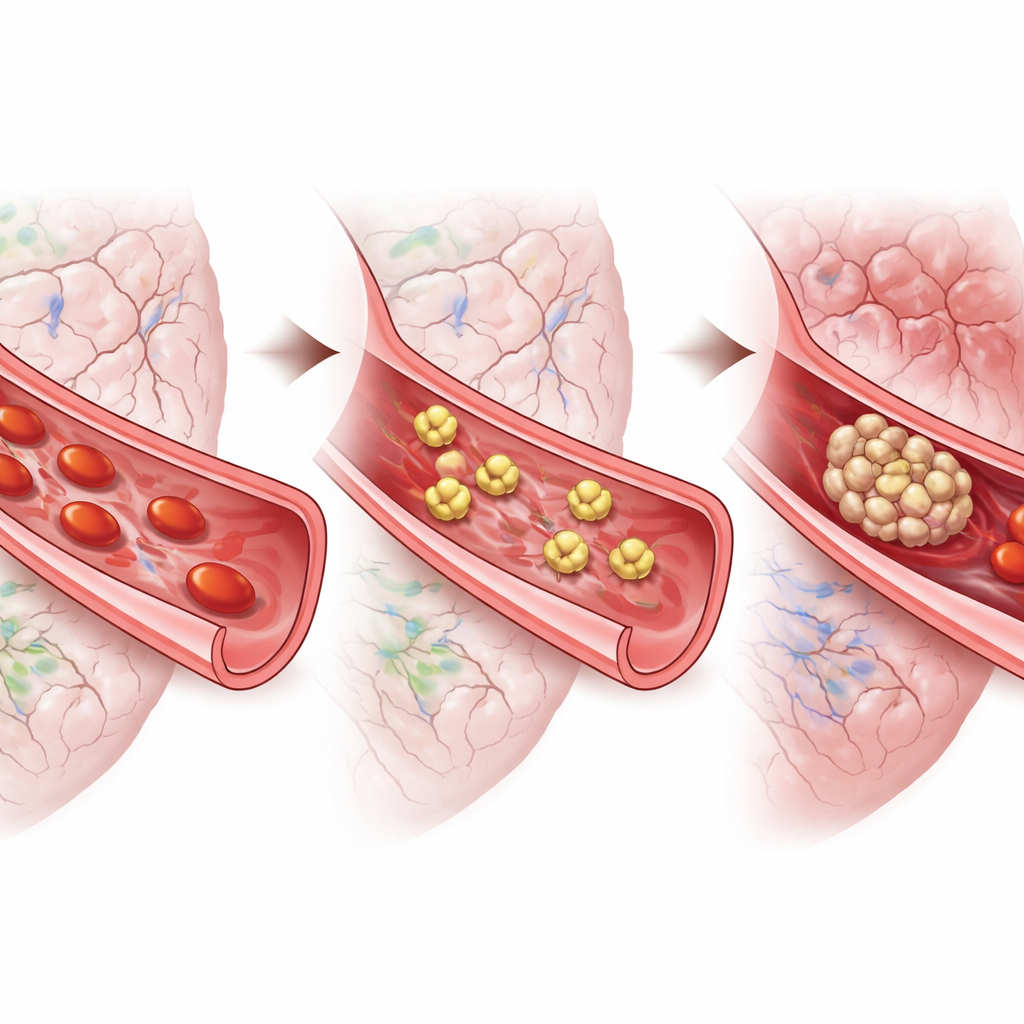
Od myszy do ludzi
Aby zbliżyć wyniki do stanu u ludzi, badacze pobrali płytki od pacjentów po tętniakowym krwotoku podpajęczynówkowym. Pod mikroskopem komórki te były silnie aktywowane i rozpostarte, co odpowiada stanowi nadmiernej gotowości do krzepnięcia. Dodanie tirofibanu do próbek sprawiło, że płytki znacznie rzadziej się rozkładały i rozprzestrzeniały, zarówno w pierwszych dniach po krwawieniu, jak i później, w oknie wysokiego ryzyka opóźnionych powikłań. Inny lek celujący w inny receptor płytkowy miał niewielki efekt. Razem z wynikami na myszach testy te sugerują, że blokowanie zlepiania się płytek, a nie jedynie tłumienie niektórych sygnałów aktywacyjnych, może być najbardziej obiecującą strategią.
Co to oznacza dla przyszłego leczenia
Praca ta dostarcza silnych dowodów, że płytki robią więcej niż tylko zatkać pierwotne pęknięcie po krwawieniu mózgu: kilka dni później przyczyniają się do tworzenia skupisk maleńkich skrzepów, które zamykają najmniejsze naczynia mózgowe i przygotowują grunt pod opóźnione udary. U myszy usunięcie płytek lub zablokowanie ich głównego „rzepu” znacznie zmniejszało te opóźnione uszkodzenia, a lek stosowany już w innych wskazaniach, tirofiban, także osłabił nadweraktywowane płytki od pacjentów w warunkach laboratoryjnych. Choć każda terapia przeciwpłytkowa musi być wyważona z ryzykiem zwiększonego krwawienia, badanie stanowi jasny dowód koncepcji, że precyzyjnie ukierunkowane leki blokujące zlepianie się płytek mogą w przyszłości pomóc chronić osoby, które przeżyły tętniakowy krwotok podpajęczynówkowy, przed groźną drugą falą uszkodzeń mózgu.
Cytowanie: Dienel, A., Hong, SH., Torres, K. et al. Platelets cause microvascular occlusion and delayed neurological deficits after subarachnoid hemorrhage in mice. Exp Mol Med 58, 1242–1253 (2026). https://doi.org/10.1038/s12276-026-01696-1
Słowa kluczowe: krwotok podpajęczynówkowy, płytki krwi, mikrozakrzepy, opóźniona niedokrwistość mózgowa, terapia przeciwpłytkowa