Clear Sky Science · ru
Тромбоциты вызывают окклюзию микрососудов и отсроченные неврологические дефициты после субарахноидального кровоизлияния у мышей
Когда кровоизлияние в мозг бьет повторно
Пережить разрыв мозговой аневризмы — лишь первая преграда для многих пациентов. Через несколько дней после первоначального кровотечения примерно у половины развиваются новые, часто разрушительные неврологические нарушения — спутанность сознания, слабость или симптомы, похожие на инсульт. Врачи называют это отсроченными неврологическими дефицитами, и до недавнего времени точный триггер оставался неясным. Это исследование на мышах с дополнительными тестами на крови людей указывает на неожиданных виновников: крошечные клетки крови — тромбоциты, которые обычно помогают останавливать кровотечение, но в этой ситуации, по-видимому, закупоривают самые мелкие сосуды мозга и лишают его жизненно важного кровоснабжения.
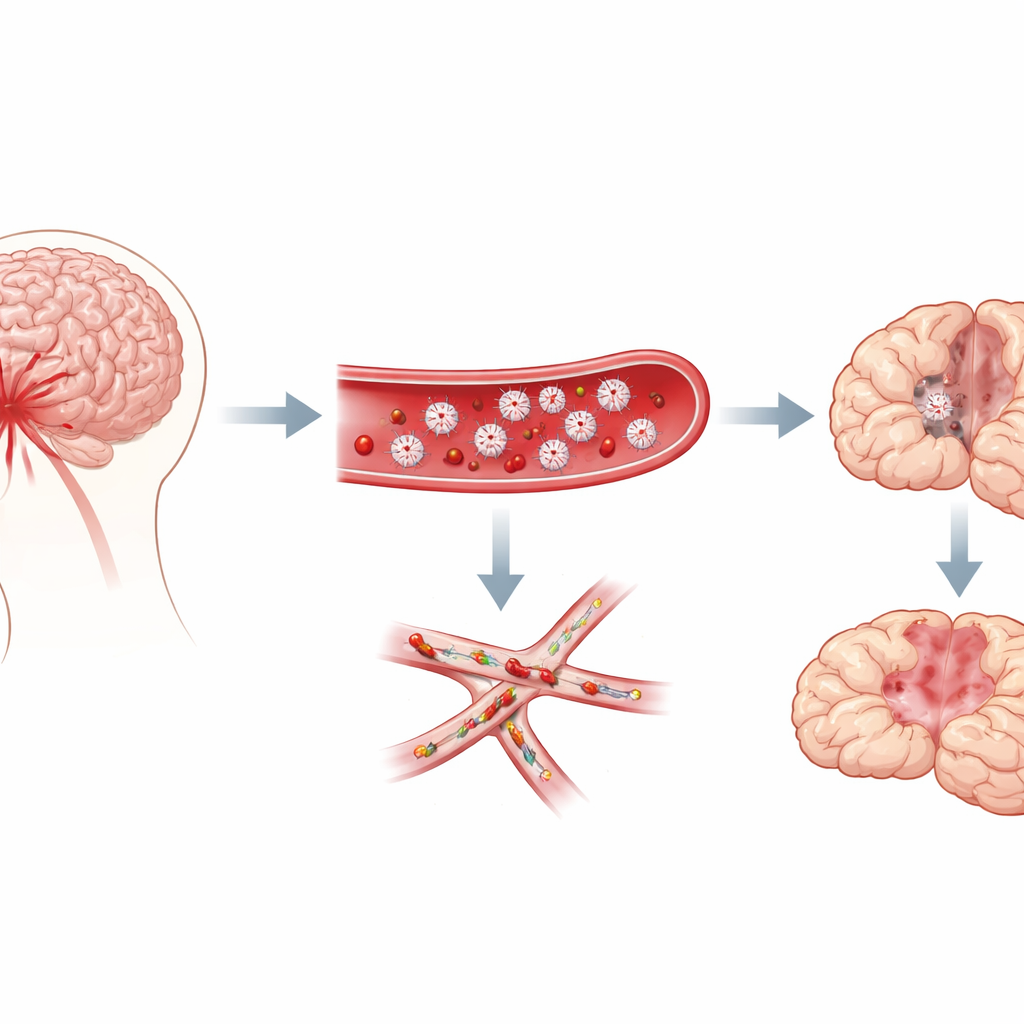
Крошечные сгустки в самых мелких сосудах мозга
Исследователи сосредоточились на субарахноидальном кровоизлиянии — виде кровотечения, которое заливает пространство вокруг мозга после разрыва аневризмы. Клиницисты давно замечали, что у пациентов, у которых затем появляются отсроченные проблемы, часто обнаруживаются признаки повышенной свертываемости крови, а при вскрытиях видны бесчисленные «микротромбы» — точечные сгустки, усеивающие мозг. Эти сгустки богаты тромбоцитами. Однако не было ясно, вызывают ли тромбоциты сами отсроченное повреждение или просто присутствуют как попутные наблюдатели. Используя хорошо зарекомендовавшую себя модель этого кровотечения у мышей, команда отслеживала поведение и патологию мозга в течение недели, чтобы выяснить, совпадает ли активность тромбоцитов с началом отсроченных дефицитов.
Включение и выключение тромбоцитов
В первом наборе экспериментов ученые измеряли химические сигналы в крови, которые известны тем, что активируют тромбоциты. Две молекулы, называемые PAF и TXB2, резко повышались на первый день и снова примерно на пятый день — повторяя окно высокого риска, когда обычно появляются отсроченные проблемы. Чтобы проверить причинно-следственную связь, они затем усилили стимуляцию тромбоцитов. Когда мышам вводили дополнительный PAF вскоре после кровоизлияния, многие погибли, а их мозги оказались переполнены микротромбами. Введение PAF через несколько дней, в «тихой» фазе восстановления, не убивало животных, но ухудшало неврологические показатели, вызывало больше отсроченных дефицитов и увеличивало нагрузку микросгустков. Мыши, генетически предрасположенные к отсроченной активации тромбоцитов, продемонстрировали схожую картину: обычное раннее восстановление, за которым следовал более высокий уровень поздно возникающих дефицитов.
Удаление или подавление тромбоцитов
Если усиление активности тромбоцитов ухудшало исход, помогло бы их подавление? Чтобы выяснить это, команда использовала трансгенных мышей, тромбоциты которых можно было избирательно удалить с помощью токсина, вводимого до кровоизлияния. Эти животные не кровоточили сильнее и не умирали чаще, но у них было меньше микротромбов, лучше раннее неврологическое состояние и значительно меньший риск отсроченного ухудшения по сравнению с нормальными мышами. Поскольку полное удаление тромбоцитов было бы небезопасно для людей, исследователи также проверили несколько существующих препаратов, блокирующих разные рецепторы тромбоцитов — точки связывания, через которые разнообразные сигналы активируют эти клетки или заставляют их слипаться. Многие из этих препаратов улучшали раннее поведение и сокращали число микротромбов, но только один — тирофибан, блокирующий ключевой рецептор агрегации GPIIb/IIIa, — явно снизил долгосрочную частоту отсроченных дефицитов у самок мышей.
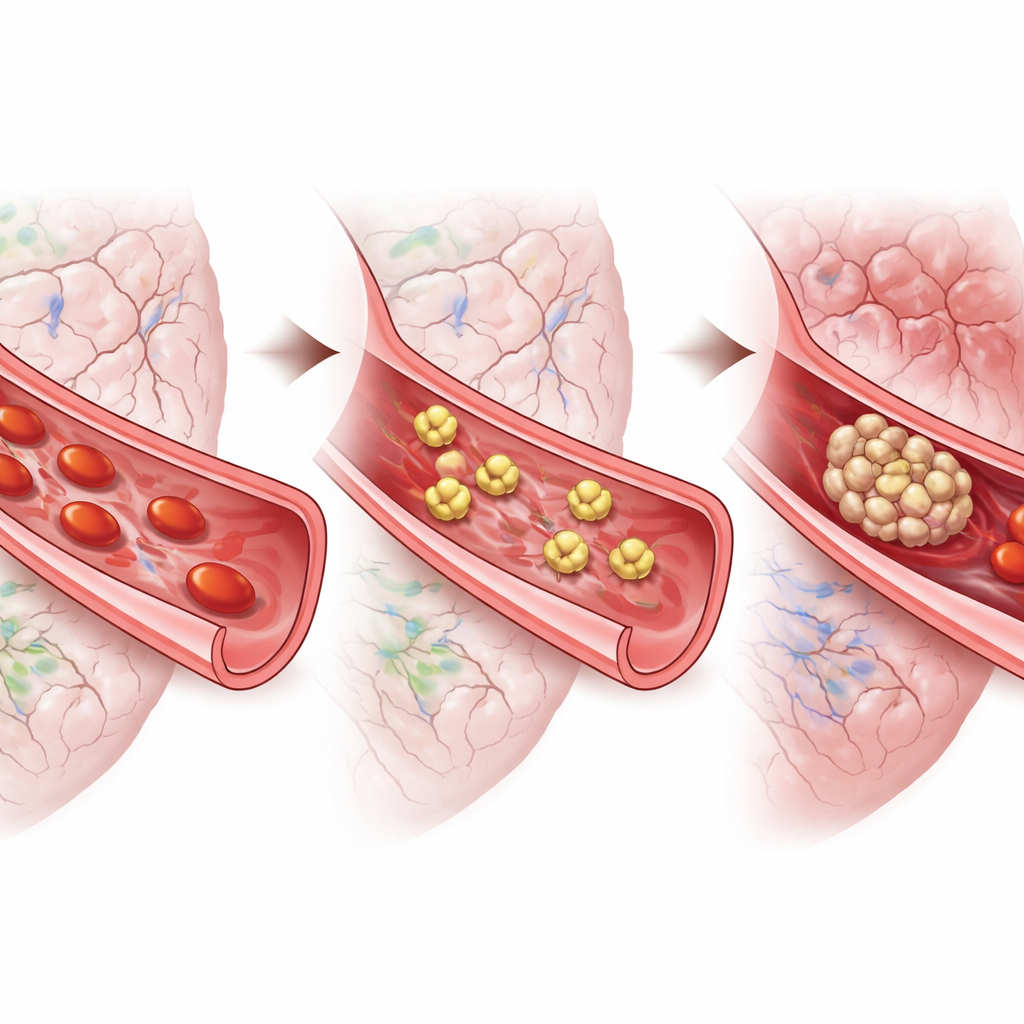
От мышей к людям
Чтобы приблизить результаты к человеческой болезни, исследователи собрали тромбоциты у пациентов, перенесших аневризматическое субарахноидальное кровоизлияние. Под микроскопом эти клетки были сильно активированы и распластаны, что соответствует состоянию повышенной тромбообразующей готовности. Добавление тирофибана в образцы делало тромбоциты значительно менее склонными к распластыванию как в первые дни после кровоизлияния, так и позже, в окне высокого риска для отсроченных осложнений. Другой препарат, нацеленный на иной рецептор тромбоцитов, оказал мало эффекта. В совокупности с результатами на мышах эти тесты предполагают, что блокирование слипание тромбоцитов, а не просто подавление отдельных сигналов активации, может быть наиболее перспективной стратегией.
Что это означает для будущего лечения
Эта работа дает убедительные доказательства того, что тромбоциты делают не только роль затычки для начального разрыва при кровоизлиянии в мозг: спустя дни они участвуют в формировании кластеров крошечных сгустков, которые блокируют самые мелкие сосуды мозга и создают почву для отсроченных инсультов. У мышей удаление тромбоцитов или блокирование их главного «липкого» рецептора резко снижало эти отсроченные повреждения, а препарат, уже используемый в других клинических ситуациях — тирофибан — также подавлял гиперактивные тромбоциты пациентов в лабораторных условиях. Хотя любая антиагрегантная терапия должна взвешиваться с риском усиления кровотечения, исследование демонстрирует четкое доказательство концепции: целенаправленные препараты, препятствующие слипанию тромбоцитов, в будущем могут помочь защитить выживших после аневризматического субарахноидального кровоизлияния от опасной второй волны повреждений мозга.
Цитирование: Dienel, A., Hong, SH., Torres, K. et al. Platelets cause microvascular occlusion and delayed neurological deficits after subarachnoid hemorrhage in mice. Exp Mol Med 58, 1242–1253 (2026). https://doi.org/10.1038/s12276-026-01696-1
Ключевые слова: субарахноидальное кровоизлияние, тромбоциты, микротромбы, отсроченная церебральная ишемия, антиагрегантная терапия