Clear Sky Science · nl
Bloedplaatjes veroorzaken microvasculaire afsluiting en vertraagde neurologische tekorten na subarachnoïdale bloeding bij muizen
Als een hersenbloeding nog eens toeslaat
Het overleven van een gesprongen hersenaneurysma is voor veel patiënten slechts de eerste hindernis. Dagen na de eerste bloeding ontwikkelt ongeveer de helft nieuwe, vaak verwoestende neurologische problemen zoals verwardheid, zwakte of stroke‑achtige klachten. Artsen noemen dit vertraagde neurologische tekorten, en tot nu toe bleef de precieze trigger onduidelijk. Deze studie bij muizen, met ondersteunende tests op menselijk bloed, wijst een verrassende boosdoener aan: piepkleine bloedcellen genaamd bloedplaatjes die normaal bloedingen helpen stoppen maar in deze situatie de fijnste vaten van de hersenen lijken te verstoppen en zo de vitale bloedtoevoer afklemmen.
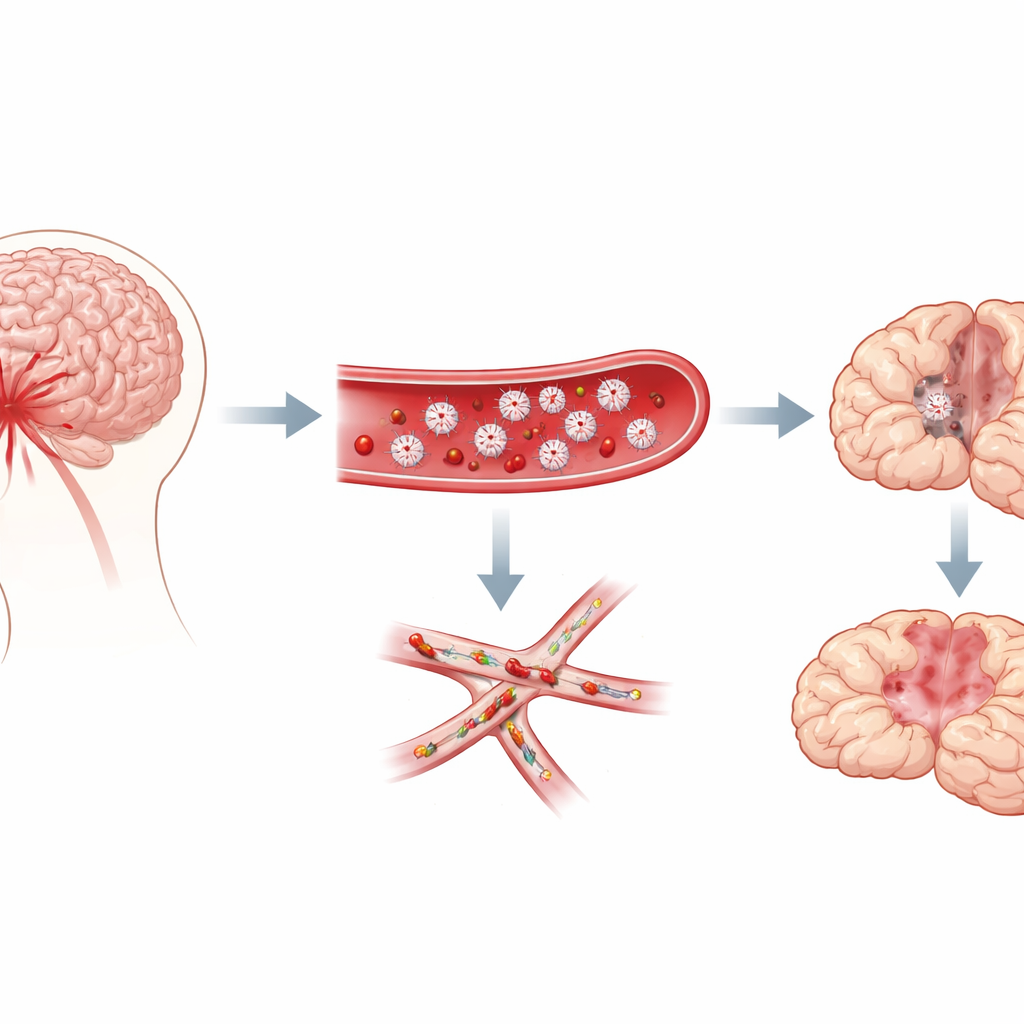
Kleine klontertjes in de kleinste vaten van de hersenen
De onderzoekers richtten zich op subarachnoïdale bloeding, een type bloeding dat de ruimte rond de hersenen overstroomt nadat een aneurysma is gescheurd. Klinische waarnemingen lieten al zien dat patiënten die later problemen krijgen vaak tekenen vertonen van een verhoogde neiging tot stolling, en autopsies tonen talloze “microthrombi” — microscopische stolselletjes — verspreid door de hersenen. Deze stolselletjes bevatten veel bloedplaatjes. Het was echter onduidelijk of bloedplaatjes daadwerkelijk de vertraagde schade veroorzaken of alleen maar als toeschouwers aanwezig zijn. Met een goed bekend muismodel van deze bloeding volgde het team gedrag en hersenpathologie gedurende een week en vroeg of de activiteit van bloedplaatjes samenviel met het optreden van vertraagde tekorten.
Bloedplaatjes aan- en uitzetten
In de eerste reeks experimenten maten de wetenschappers chemische signalen in het bloed die bloedplaatjes kunnen activeren. Twee daarvan, PAF en TXB2, stegen scherp op dag één en opnieuw rond dag vijf — een patroon dat overeenkomt met het hoogrisico‑venster waarin vertraagde problemen gewoonlijk verschijnen. Om oorzaak en gevolg te testen, activeerden ze de bloedplaatjes extra. Wanneer muizen kort na de bloeding extra PAF kregen, vielen er veel doden en vulden hun hersenen zich met meer microthrombi. PAF enkele dagen later toedienen, tijdens de «stille» herstelperiode, doodde de dieren niet maar leidde wel tot slechtere neurologische scores, meer vertraagde tekorten en een grotere last aan microklontertjes. Muizen met een genetische aanleg voor vertraagde plateletactivatie vertoonden een vergelijkbaar patroon: een normaal vroeg herstel gevolgd door een hogere frequentie van later optredende tekorten.
Bloedplaatjes verwijderen of tot rust brengen
Als het opvoeren van bloedplaatjes de situatie verslechterde, kon het verlagen ervan helpen? Om dat te onderzoeken gebruikten de onderzoekers genetisch gewijzigde muizen waarvan de bloedplaatjes selectief konden worden verwijderd met een toxine dat vóór de bloeding werd gegeven. Deze dieren bleden niet meer of stierven niet vaker, maar ze hadden minder microthrombi, betere vroege neurologische functie en een aanzienlijk lagere kans op vertraagde achteruitgang dan normale muizen. Omdat het volledig weghalen van bloedplaatjes bij mensen onveilig zou zijn, testten de onderzoekers ook verschillende bestaande geneesmiddelen die verschillende plaatjesreceptoren blokkeren — de aanhechtingspunten waarlangs signalen deze cellen activeren of ze samen laten klonteren. Veel van deze middelen verbeterden het vroege gedrag en verminderden microklontertjes, maar slechts één, tirofiban, dat een cruciale «aggregatie»‑receptor GPIIb/IIIa blokkeert, verminderde duidelijk de langetermijnfrequentie van vertraagde tekorten bij vrouwelijke muizen.
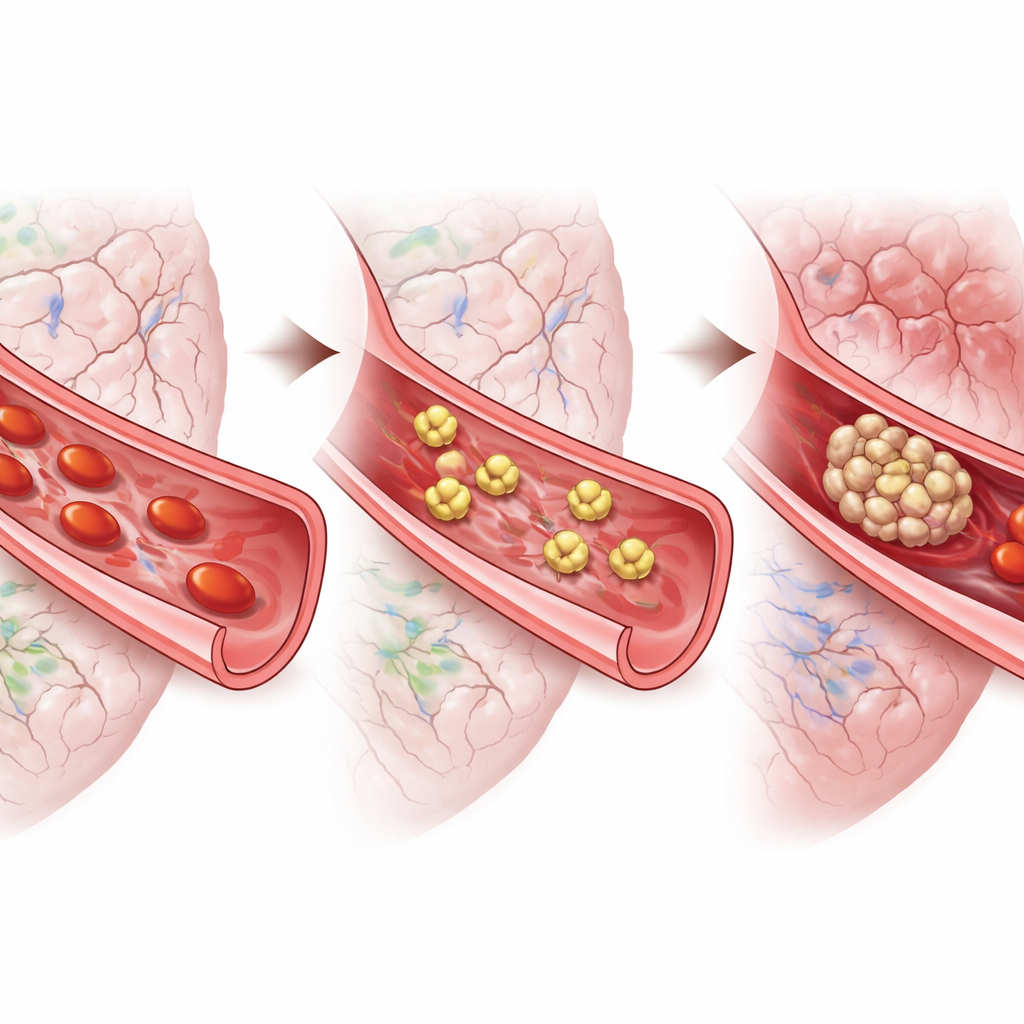
Van muizen naar mensen
Om de vertaalslag naar menselijke ziekte te maken, verzamelden de onderzoekers bloedplaatjes van patiënten die een aneurysmatische subarachnoïdale bloeding hadden doorgemaakt. Onder de microscoop waren deze cellen sterk geactiveerd en uitgespreid, wat overeenstemt met een uiterst prikkelbare stollingstoestand. Het toevoegen van tirofiban aan de monsters maakte de plaatjes veel minder geneigd zich uit te spreiden, zowel in de eerste dagen na de bloeding als later tijdens het hoogrisico‑venster voor vertraagde complicaties. Een ander middel dat een andere plaatjesreceptor targette had weinig effect. Samen met de muisgegevens suggereren deze tests dat het blokkeren van plaatjesagglutinatie, in plaats van alleen het dempen van sommige activatiesignalen, wellicht de meest veelbelovende strategie is.
Wat dit betekent voor toekomstige behandelingen
Dit werk levert sterke aanwijzingen dat bloedplaatjes meer doen dan alleen het stoppen van de initiële scheur na een hersenbloeding: dagen later helpen ze clusters van kleine stolselletjes te vormen die de kleinste vaten van de hersenen verstoppen en het toneel bereiden voor vertraagde beroertes. Bij muizen verminderde het wegnemen van bloedplaatjes of het blokkeren van hun belangrijkste «klittenband»‑receptor deze vertraagde schade sterk, en een geneesmiddel dat al in andere settings wordt gebruikt, tirofiban, temperde ook overactieve bloedplaatjes van menselijke patiënten in het laboratorium. Hoewel elke antiplateletbehandeling moet worden afgewogen tegen het risico op meer bloedingen, levert de studie een duidelijk proof‑of‑concept: zorgvuldig gerichte middelen die plaatjesaggregatie blokkeren zouden ooit kunnen helpen overlevenden van aneurysmatische subarachnoïdale bloeding te beschermen tegen een gevaarlijke tweede golf van hersenschade.
Bronvermelding: Dienel, A., Hong, SH., Torres, K. et al. Platelets cause microvascular occlusion and delayed neurological deficits after subarachnoid hemorrhage in mice. Exp Mol Med 58, 1242–1253 (2026). https://doi.org/10.1038/s12276-026-01696-1
Trefwoorden: subarachnoïdale bloeding, bloedplaatjes, microthrombi, vertraagde cerebrale ischemie, antiplatelettherapie