Clear Sky Science · de
Thrombozyten verursachen mikrovaskuläre Okklusion und verzögerte neurologische Defizite nach Subarachnoidalblutung bei Mäusen
Wenn eine Hirnblutung ein zweites Mal zuschlägt
Das Überleben eines geplatzten Hirnaneurysmas ist für viele Patientinnen und Patienten nur die erste Hürde. Tage nach der ersten Blutung entwickeln etwa die Hälfte neue, oft verheerende neurologische Probleme wie Verwirrung, Schwäche oder schlaganfallähnliche Symptome. Ärztinnen und Ärzte bezeichnen diese Erscheinungen als verzögerte neurologische Defizite; der genaue Auslöser war bislang unklar. Diese Studie an Mäusen, ergänzt durch Tests mit menschlichem Blut, macht einen überraschenden Übeltäter aus: winzige Blutplättchen, sogenannte Thrombozyten, die normalerweise Blutungen stoppen, scheinen in diesem Kontext die feinsten Hirngefäße zu verstopfen und die lebenswichtige Durchblutung zu beeinträchtigen.
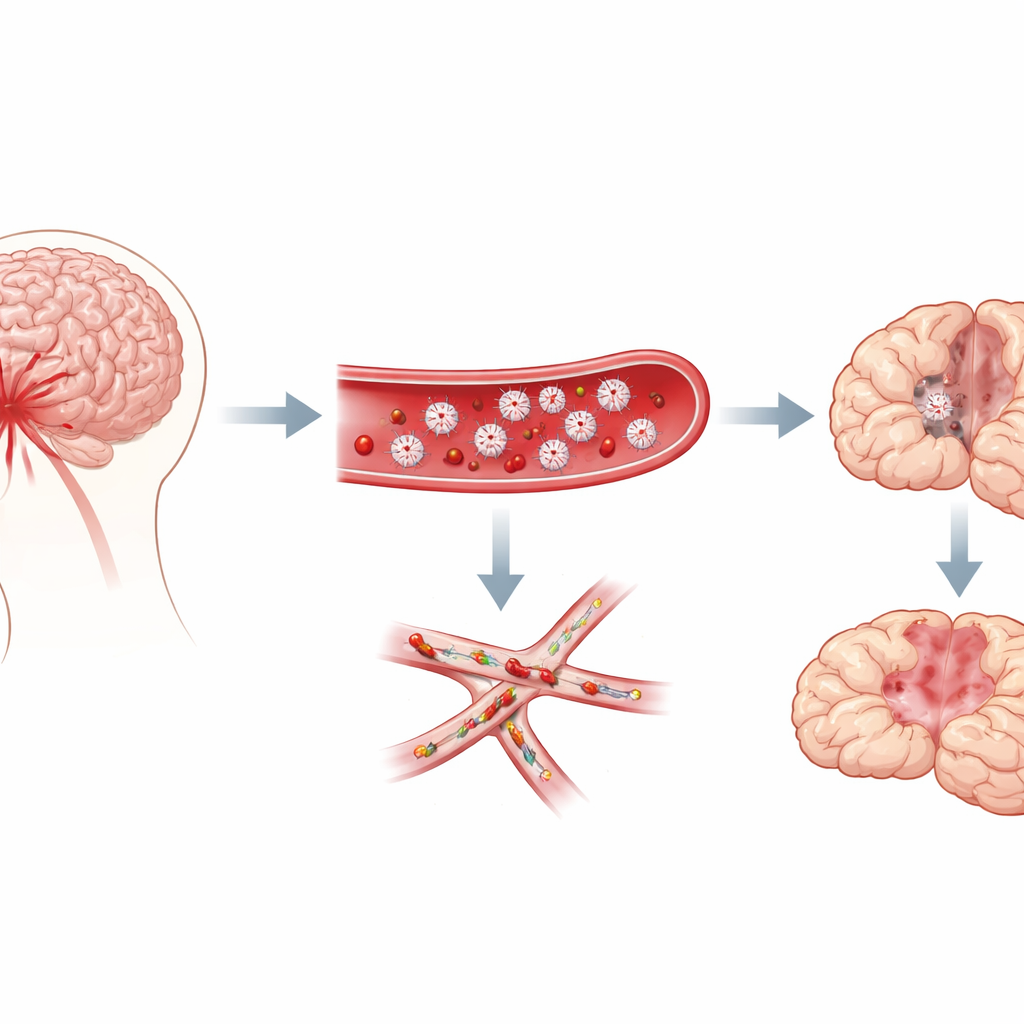
Winzige Gerinnsel in den kleinsten Gefäßen des Gehirns
Die Forschenden konzentrierten sich auf die Subarachnoidalblutung, eine Form der Blutung, die nach dem Ruptur eines Aneurysmas den Raum um das Gehirn überschwemmt. Kliniker beobachten seit Langem, dass Patientinnen und Patienten, die später verzögerte Probleme entwickeln, häufig Zeichen einer vermehrten Gerinnungsneigung zeigen; Autopsien zeigen zahllose „Mikrothromben“—punktuelle Gerinnsel—im Gehirn. Diese Gerinnsel sind reich an Thrombozyten. Unklar war jedoch, ob Thrombozyten die verzögerten Schäden tatsächlich verursachen oder nur als Beiwerk auftreten. Mithilfe eines etablierten Mausmodells dieser Blutung verfolgte das Team Verhalten und Gehirnpathologie über eine Woche und prüfte, ob die Thrombozytenaktivität mit dem Auftreten der verzögerten Defizite korrelierte.
Thrombozyten an- und ausschalten
In der ersten Versuchsreihe bestimmten die Wissenschaftlerinnen und Wissenschaftler Botenstoffe im Blut, die dafür bekannt sind, Thrombozyten zu aktivieren. Zwei davon, PAF und TXB2, stiegen am ersten Tag und erneut um den fünften Tag stark an—ein Muster, das dem Hochrisikofenster entspricht, in dem verzögerte Probleme typischerweise auftreten. Um Ursache und Wirkung zu prüfen, verstärkten sie die Thrombozytenaktivierung. Wenn Mäusen kurz nach der Blutung zusätzliches PAF verabreicht wurde, starben viele Tiere und ihre Gehirne waren mit mehr Mikrothromben durchsetzt. Wurde PAF einige Tage später während der „ruhigen“ Erholungsphase gegeben, tötete es die Tiere zwar nicht, führte aber zu schlechteren neurologischen Punkten, mehr verzögerten Defiziten und einer stärkeren Belastung durch Mikrogerinnsel. Mäuse, die genetisch zu verzögerter Thrombozytenaktivierung neigten, zeigten ein ähnliches Bild: eine normale frühe Erholung, gefolgt von einer höheren Rate spät auftretender Defizite.
Thrombozyten entfernen oder beruhigen
Wenn eine verstärkte Thrombozytenaktivierung die Lage verschlechterte, konnte das Abschwächen helfen? Um das zu testen, setzten die Forschenden gentechnisch veränderte Mäuse ein, bei denen Thrombozyten selektiv mit einem vor der Blutung verabreichten Toxin entfernt werden konnten. Diese Tiere bluteten nicht häufiger und starben nicht öfter, hatten aber weniger Mikrothromben, bessere frühe neurologische Funktion und eine deutlich geringere Wahrscheinlichkeit eines verzögerten Leistungsabfalls als normale Mäuse. Da das vollständige Entfernen von Thrombozyten beim Menschen unsicher wäre, testeten die Forschenden außerdem mehrere bereits verfügbare Medikamente, die verschiedene Thrombozytenrezeptoren blockieren—die Andockstellen, über die Signale diese Zellen aktivieren oder ihre Verklumpung fördern. Viele dieser Wirkstoffe verbesserten das frühe Verhalten und verringerten Mikrogerinnsel, doch nur eines davon, Tirofiban, das einen zentralen „Aggregations“-Rezeptor namens GPIIb/IIIa blockiert, senkte bei weiblichen Mäusen eindeutig die Langzeitrate verzögerter Defizite.
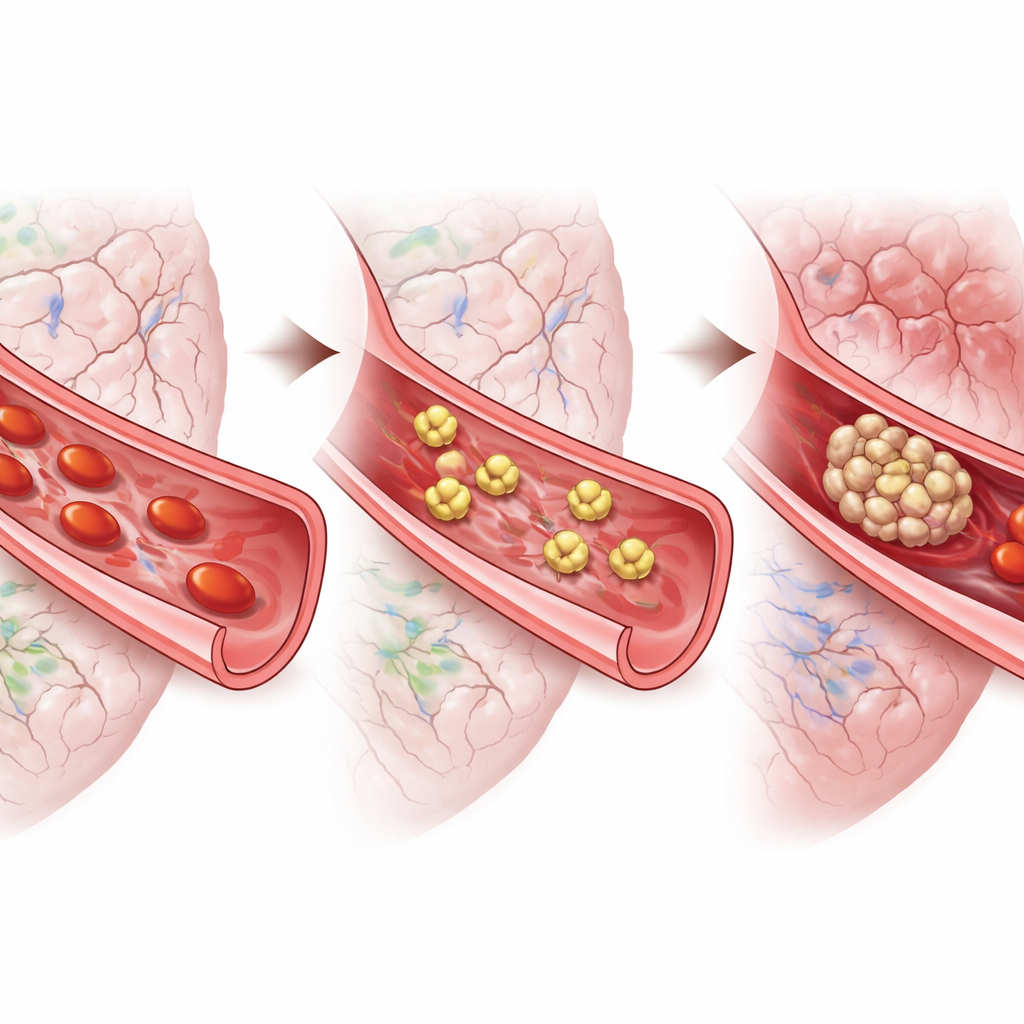
Von Mäusen zu Menschen
Um den Bezug zur menschlichen Erkrankung herzustellen, entnahmen die Untersuchenden Thrombozyten von Patientinnen und Patienten, die eine aneurysmatische Subarachnoidalblutung erlitten hatten. Unter dem Mikroskop waren diese Zellen stark aktiviert und ausgebreitet, was einem sehr leicht auslösbaren Gerinnungszustand entspricht. Die Zugabe von Tirofiban zu den Proben verringerte deutlich die Ausbreitung der Thrombozyten, sowohl in den ersten Tagen nach der Blutung als auch später im Hochrisikofenster für verzögerte Komplikationen. Ein anderes auf einen anderen Thrombozytenrezeptor zielendes Präparat zeigte kaum Wirkung. Zusammen mit den Mausdaten deuten diese Tests darauf hin, dass das Verhindern der Thrombozytenverklumpung—und nicht bloß das Dämpfen einzelner Aktivierungssignale—die vielversprechendste Strategie sein könnte.
Was das für künftige Behandlungen bedeutet
Diese Arbeit stützt die Annahme, dass Thrombozyten mehr tun, als nur die initiale Ruptur nach einer Hirnblutung zu verschließen: Tage später tragen sie zur Bildung von Clustern winziger Gerinnsel bei, die die kleinsten Gefäße des Gehirns verstopfen und den Boden für verzögerte Schlaganfälle bereiten. Bei Mäusen reduzierte das Entfernen von Thrombozyten oder das Blockieren ihres wichtigsten „Klett“-Rezeptors diese verzögerten Schäden deutlich, und ein bereits in anderen Situationen verwendetes Medikament, Tirofiban, dämpfte auch im Labor überaktive Thrombozyten von menschlichen Patienten. Obwohl jede antithrombozytäre Behandlung gegen ein erhöhtes Blutungsrisiko abgewogen werden muss, liefert die Studie einen klaren Proof-of-Concept, dass gezielt wirkende Thrombozytenblocker eines Tages Überlebende aneurysmatischer Subarachnoidalblutungen vor einer gefährlichen zweiten Welle von Hirnschäden schützen könnten.
Zitation: Dienel, A., Hong, SH., Torres, K. et al. Platelets cause microvascular occlusion and delayed neurological deficits after subarachnoid hemorrhage in mice. Exp Mol Med 58, 1242–1253 (2026). https://doi.org/10.1038/s12276-026-01696-1
Schlüsselwörter: Subarachnoidalblutung, Thrombozyten, Mikrothromben, verzögerte zerebrale Ischämie, Thrombozytenhemmung