Clear Sky Science · tr
Glioblastomanın moleküler alt tipleri ve (in vitro) temozolomid yanıtı
Bu beyin kanseri çalışması neden önemli
Glioblastoma, erişkinlerde en yaygın ve en öldürücü beyin kanseri türüdür ve mevcut standart ilaç temozolomid bile hastaya genellikle yalnızca birkaç aylık yaşam süresi kazandırır. Bu çalışma, hastalar ve klinisyenler için doğrudan alaka taşıyan bir soruyu soruyor: bir glioblastomanın moleküler “kişiliği” tedaviye nasıl yanıt vereceğini öngörebilir mi ve bazı tümörler neden bu kadar çabuk ilaç direncine kavuşuyor?
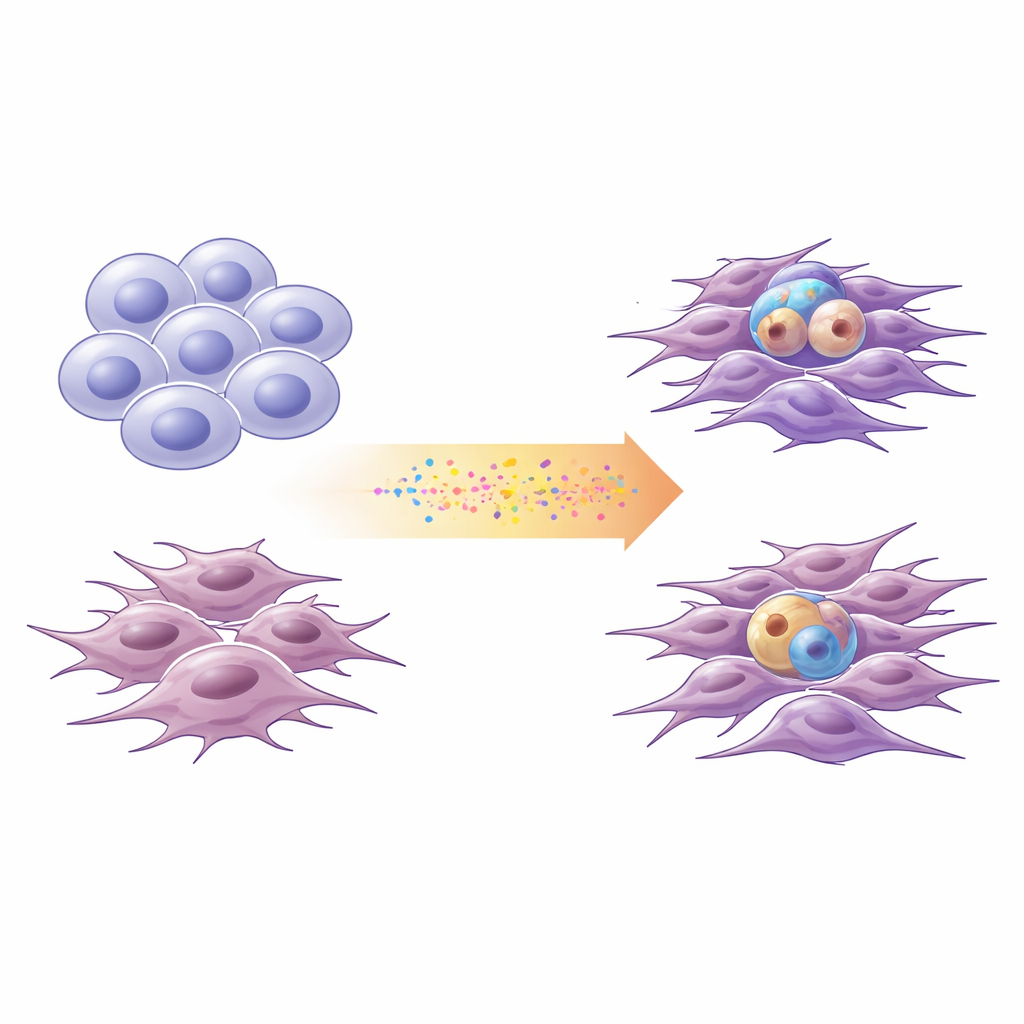
Glioblastomanın iki ana görünümleri
Araştırmacılar giderek glioblastoma hücrelerini iki geniş durum arasındaki bir spektrum olarak tanımlıyor. “Proneural” hücreler olgunlaşmamış sinir hücrelerine benzer: kök‑benzeri bölünürler ve çeşitli soylar üretebilirler. “Mezenkimal” hücreler ise daha çok strese uğramış, sertleşmiş hayatta kalanlara benzer: daha hareketli, invaziv ve iltihapla ilişkili olurlar. Dört hastadan yeni türetilmiş hücrelerin yanı sıra standart bir laboratuvar hücre hattını kullanarak ekip, her kültürü bu proneural–mezenkimal eksen üzerinde konumlandırmak için DNA değişiklikleri ve gen aktivitesini profilledi. Bu basitleştirilmiş iki durumlu ölçeğin, büyük kamu glioblastoma veri setlerinde görülen transkripsiyonel çeşitliliğin çoğunu yakaladığını doğruladılar.
Kök‑benzeri davranış ve CD44 bilmecesi
Serbest yüzeyli sferoidler halinde büyüme ve karışık bir popülasyonu yeniden oluşturma yeteneği gibi kök‑benzeri özellikler sıklıkla terapi direncinin suçlusu olarak gösterilir. Yazarlar yayımlanmış dört‑gen kök‑benzerlik programını nicelendirip çarpıcı bir desen buldular: spektrumun proneural ucundaki hücreler tutarlı olarak daha yüksek kök‑benzerlik puanları gösterirken, mezenkimal hücreler daha düşük puan aldı. Aynı zamanda tartışmalı bir yüzey molekülü olan CD44’ü yeniden ele aldılar; bazen kök hücre işareti olarak anılır. Kendi ellerindeki verilere göre daha yüksek CD44, hem kendi kültürlerinde hem bağımsız veri setlerinde mezenkimal durumla ve daha düşük kök‑benzerlikle ilişkilendi, tersine değil. Proneural bir kültürden düşük‑CD44 ve yüksek‑CD44 hücreleri fiziksel olarak ayırdıklarında, düşük‑CD44 grubu daha plastik davranıp orijinal karışımı yeniden doldurabilen daha çok kök hücre benzeri özellikler gösterdi; yüksek‑CD44 grubu ise daha farklılaşmış ve mezenkimal‑benzeri görünüyordu.
Tümör hücreleri çevreleriyle nasıl iletişim kurar
CD44 en iyi hyaluronik asit için bir reseptör olarak bilinir; hyaluronik asit beyin ekstrasellüler matriksinin şeker açısından zengin bir bileşenidir. Ekip görüşlerini hyaluronik‑asit bağlayıcı birçok proteini de kapsayacak şekilde genişletti. Mezenkimal hücrelerin bu matrikse tutunup içeri alabilecek yüzey reseptörlerinde zenginleştiğini, proneural hücrelerin ise koruyucu bir niş oluşturmaya yardım eden daha fazla matris‑yapıcı bileşen ürettiğini buldular. İşlevsel olarak, temozolomid ile ekstra hyaluronik asidi birleştirdiklerinde, mezenkimal hücrelerin göçü reseptörleri daha yoğun kullandıklarıyla tutarlı şekilde yavaşladı; oysa proneural hücreler daha az etkilendi. Bu, tümör ile mikroçevresinin birbirini pekiştirebileceği alt tipe özgü mekanizmalara işaret ediyor.
Temozolomid hücreleri daha sert bir duruma itiyor
Çalışmanın özü bu farklı hücre durumlarının temozolomide nasıl yanıt verdiğini ele alıyor. İlk 24 saatte, artan ilaç dozları mezenkimal hücrelerin büyümesini kısıtlarken proneural hücrelerin bölünme hızına neredeyse dokunmadı. 72 saat boyunca ve geniş bir doz aralığında, genel ilaç duyarlılığı (klasik IC50 ölçüsü) basitçe alt tipe bağlı değildi. Bununla birlikte ekip klinikteki tekrarlı dozlamayı taklit ettiğinde—tedavi, iyileşmeye izin verme, sonra yeniden tedavi—proneural kültürler öne çıktı: bir maruziyetten sonra daha az proliferatif hale gelirken ikinci turda belirgin şekilde daha dirençli oldular; oysa mezenkimal kültürlerde duyarlılıkta çok az değişim oldu. Gen ifadesi analizi, neredeyse toksik temozolomid dozlarının tüm hücrelerde geniş bir “mezenkimal kayma”yı tetiklediğini gösterdi: iltihap ve doku yeniden şekillendirmeyle ilişkili yollar yükselirken, özellikle başlangıçta proneural olan hücrelerde kök‑benzerlik ilişkilendirilmiş programlar düştü. Yine de bu proneural kaynaklı hücreler görece yüksek kök‑benzeri potansiyellerini korudular; bu da geçici bir gerileme yaşayıp daha sonra nüksü besleyebileceklerini düşündürüyor.
Oksijen seviyeleri direncin dengesini kaydırıyor
Gerçek tümörler oksijen arzı açısından yamalıdır ve düşük oksijenli bölgelerin tedavi direncini teşvik ettiği bilinmektedir. Kobalt klorür kullanarak hipoksi‑benzeri bir yanıt tetiklediklerinde araştırmacılar, oksijen durumunun alt tip ile güçlü şekilde etkileştiğini buldular. Simüle edilmiş hipoksi altında proneural hücreler proliferasyonu azalttı ama metabolik aktiviteyi artırdı; bu durumda temozolomide maruz kaldıklarında daha iyi hayatta kaldılar ve daha fazla göç ettiler. Buna karşın mezenkimal hücreler aynı hipoksik sinyal altında ilaca karşı daha savunmasız hale gelme eğilimindeydi. Ekip hipoksinin temozolomid gücünü kök‑benzerlik puanına göre nasıl değiştirdiğini çizdiklerinde, kültürler iki kampa ayrıldı: daha yüksek kök‑benzerlik ve proneural‑benzeri olup daha dirençli hale gelenler ve daha düşük kök‑benzerlik, mezenkimal‑benzeri olup daha duyarlı hale gelenler.
Bu hastalar ve gelecekteki tedaviler için ne anlama geliyor
Herkes için anlaşılır bir çıkarım, tüm glioblastomaların biyolojik olarak aynı olmadığı ve bu farklılıkların tümörlerin tedaviye nasıl dayanıp uyum sağladığı üzerinde etkili olduğudur. Proneural, kök‑benzeri hücrece zengin tümörler temozolomidi özellikle iyi dayanma eğiliminde görünür; mezenkimal‑benzeri daha sert bir duruma kayarlarken, özellikle düşük oksijen koşullarında dayanıklı bir hücre çekirdeğini korurlar. Çalışma, CD44 ve diğer hyaluronik‑asit ilişkili moleküllerin basit kök hücre bayrakları değil, bu sertleşmiş mezenkimal kimliğin göstergeleri olarak daha uygun görülmesi gerektiğini öne sürüyor. Sınırlı sayıda hücre modeli ve büyük ölçüde korelasyonel verilere dayansa da, çalışma proneural–mezenkimal basit ölçeği ve kök‑benzerlik ölçümlerini glioblastomaları sınıflandırmak ve en uyum sağlayıcı, nükse yol açan hücreleri önlemek veya etkisizleştirmek için tedaviler tasarlamak üzere kullanmayı destekliyor.
Atıf: Rancati, S., Campolungo, M., Dalmolin, D.G. et al. Molecular subtypes and the (in vitro) response of glioblastoma to temozolomide. BJC Rep 4, 24 (2026). https://doi.org/10.1038/s44276-026-00228-8
Anahtar kelimeler: glioblastoma, temozolomid direnci, kanser kök hücreleri, tümör hipoksisi, moleküler alt tipler