Clear Sky Science · sv
Molekylära subtyper och glioblastoms (in vitro) respons på temozolomid
Varför denna studie av hjärncancer är viktig
Glioblastom är den vanligaste och dödligaste formen av hjärncancer hos vuxna, och även dagens standardläkemedel, temozolomid, ger vanligen bara några extra månaders överlevnad. Denna studie ställer en fråga med direkt relevans för patienter och kliniker: kan en glioblastoms molekylära ”personlighet” hjälpa till att förutsäga hur den svarar på behandling, och varför vissa tumörer så snabbt blir läkemedelsresistenta?
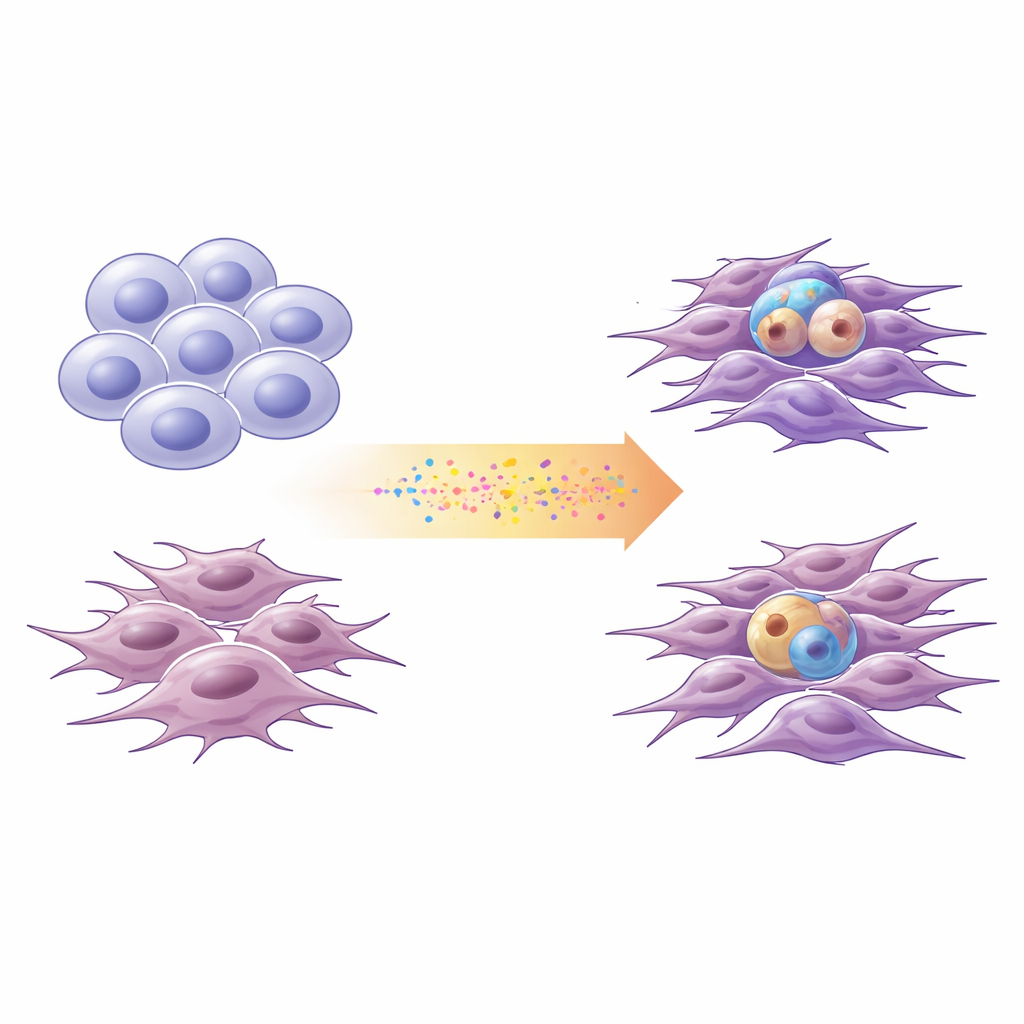
Två huvudvarianter av glioblastom
Forskare beskriver allt oftare glioblastomceller längs ett spektrum mellan två breda tillstånd. ”Proneurala” celler liknar omogna nervceller: de delar sig på ett stamliknande sätt och kan ge upphov till olika avkomlingar. ”Mesenkymala” celler ser mer ut som stressade, härdade överlevare: de är mer rörliga, invasiva och förknippade med inflammation. Med celler nyligen härledda från fyra patienter, samt en standard cellinje, analyserade teamet DNA‑förändringar och genaktivitet för att placera varje kultur på denna proneurala–mesenkymala axel. De bekräftade att denna förenklade tvåtillståndsskala fångade större delen av den transkriptionella mångfalden som ses i stora publika glioblastomdatabaser.
Stamlikt beteende och CD44‑gåtan
Stamliknande egenskaper — såsom förmågan att växa som fritt svävande sfäroider och att återskapa en blandad population — anklagas ofta för terapiresistens. Författarna kvantifierade ett publicerat fyragens‑program för stamhet och fann ett slående mönster: celler i den proneurala delen av spektrumet visade konsekvent högre stamhetspoäng, medan mesenkymala celler fick lägre poäng. Samtidigt återbesökte de ett omstritt ytmolekyl, CD44, som ibland kallas en stamcellsmarkör. I deras händer korrelerade högre CD44 med det mesenkymala tillståndet och lägre stamhet, inte tvärtom, både i deras egna kulturer och i oberoende dataset. När de fysiskt separerade låg‑CD44 och hög‑CD44 celler från en proneutral kultur, uppträdde låg‑CD44‑gruppen mer som stamceller — mer plastisk och kapabel att återbefolka den ursprungliga blandningen — medan hög‑CD44‑gruppen såg mer differentierad och mesenkymal‑lik ut.
Hur tumörceller kommunicerar med omgivningen
CD44 är mest känt som en receptor för hyaluronsyra, en socker‑rik komponent i hjärnans extracellulära matrix. Teamet breddade sin vy för att inkludera många hyaluronsyra‑bindande proteiner. De fann att mesenkymala celler var rikare på ytreceptorer som kan fästa vid och inta denna matrix, medan proneurala celler producerade fler matrix‑byggande komponenter som hjälper till att forma en skyddande nisch. Funktionellt, när de kombinerade temozolomid med extra hyaluronsyra, bromsade mesenkymala celler sin migration, vilket överensstämmer med deras tyngre användning av ytreceptorer, medan proneurala celler påverkades mindre. Detta pekar på subtyp‑specifika sätt där tumören och dess mikro‑miljö kan förstärka varandra.
Temozolomid driver celler mot ett tuffare tillstånd
Studien kärnar i hur dessa olika celltillstånd svarar på temozolomid. Under de första 24 timmarna minskade ökande läkemedelsdoser tillväxten hos mesenkymala celler, men berörde knappt delningshastigheten hos proneurala celler. Över 72 timmar och över ett brett dosintervall följde inte den övergripande läkemedelskänsligheten (det klassiska IC50‑måttet) enbart subtyp. Men när teamet efterliknade upprepad klinisk dosering — behandla, låta återhämta sig och sedan behandla igen — stack de proneurala kulturerna ut: efter en exponering blev de mindre proliferativa men märkbart mer resistenta vid en andra omgång, medan mesenkymala kulturer förändrades lite i sin känslighet. Genuttrycksanalys visade att nästan‑toxiska doser temozolomid drev en bred ”mesenkymal förskjutning” i alla celler: vägar kopplade till inflammation och vävnadsombyggnad ökade, medan stamhetsassocierade program sjönk, särskilt i initialt proneurala celler. Ändå behöll dessa proneuralt härledda celler relativt hög stamlik potential, vilket antyder att de kan krympa tillfälligt men senare driva återfall.
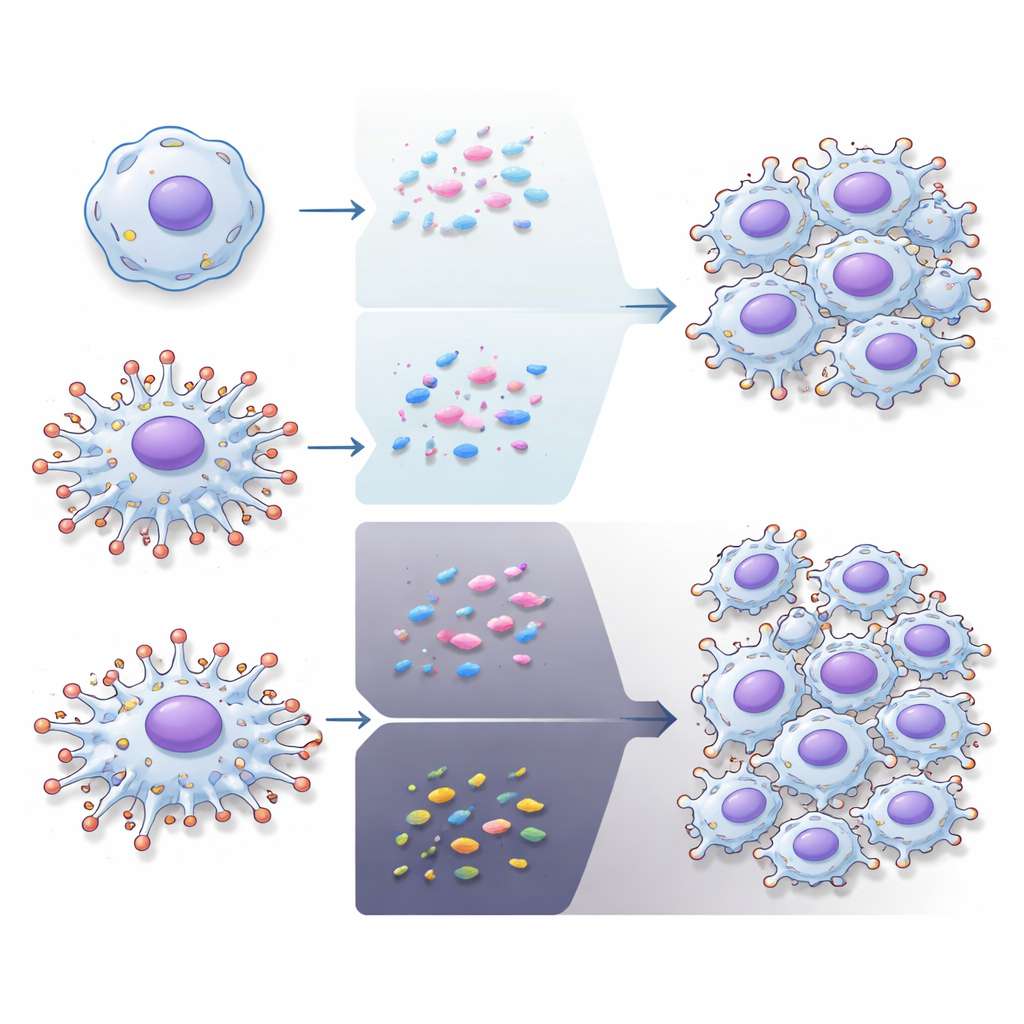
Kvävehalten lutar balansen för resistens
Riktiga tumörer är fläckiga i syretillförsel, och lågsyreområden är kända för att främja behandlingsmotstånd. Genom att använda koboltklorid för att utlösa ett hypoxi‑liknande svar fann forskarna att syrestatus samverkade starkt med subtyp. Under simulerad hypoxi minskade proneurala celler sin proliferation men ökade den metaboliska aktiviteten, och när de utsattes för temozolomid i detta tillstånd överlevde de bättre och migrerade mer. Mesenkymala celler tenderade däremot att bli mer sårbara för läkemedlet under samma hypoxiska signal. När teamet plottade hur hypoxi förändrade temozolomids potens mot stamhetspoängen föll kulturerna i två läger: hög‑stamhet, proneural‑lika celler som blev mer läkemedelsresistenta, och låg‑stamhet, mesenkymal‑lika celler som blev mer känsliga.
Vad detta betyder för patienter och framtida terapier
För en lekmannaläsare är huvudbudskapet att inte alla glioblastom är biologiskt likadana, och dessa skillnader påverkar hur tumörer uthärdar och anpassar sig till behandling. Tumörer som är rikare på proneurala, stamliknande celler verkar särskilt kapabla att klara temozolomid, skifta mot ett tuffare mesenkymalt liknande tillstånd samtidigt som de bevarar en kärna av motståndskraftiga celler, särskilt under låga syreförhållanden. Studien föreslår att CD44 och andra hyaluronsyra‑relaterade molekyler bättre ses som kännetecken för denna härdade mesenkymyta identitet, inte som enkla stamcellsflaggor. Trots att arbetet bygger på ett begränsat antal cellmodeller och till stor del är korrelativt, stöder det användningen av en enkel proneural–mesenkymal skala, tillsammans med stamhetsmått, för att stratifiera glioblastom och för att utforma terapier som förebygger eller oskadliggör de mest anpassningsbara, återfallsdrivande cellerna.
Citering: Rancati, S., Campolungo, M., Dalmolin, D.G. et al. Molecular subtypes and the (in vitro) response of glioblastoma to temozolomide. BJC Rep 4, 24 (2026). https://doi.org/10.1038/s44276-026-00228-8
Nyckelord: glioblastom, motstånd mot temozolomid, cancerstamceller, tumörhypoxi, molekylära subtyper