Clear Sky Science · de
Molekulare Subtypen und die (in vitro) Reaktion von Glioblastom auf Temozolomid
Warum diese Gehirnkrebs‑Studie wichtig ist
Das Glioblastom ist die häufigste und tödlichste Form von Hirnkrebs bei Erwachsenen, und selbst das gegenwärtige Standardmedikament Temozolomid verschafft in der Regel nur einige zusätzliche Monate Lebenszeit. Diese Studie stellt eine direkt für Patienten und Klinikpersonal relevante Frage: Kann die molekulare „Persönlichkeit“ eines Glioblastoms vorhersagen, wie es auf eine Behandlung reagiert, und warum manche Tumoren so rasch medikamentenresistent werden?
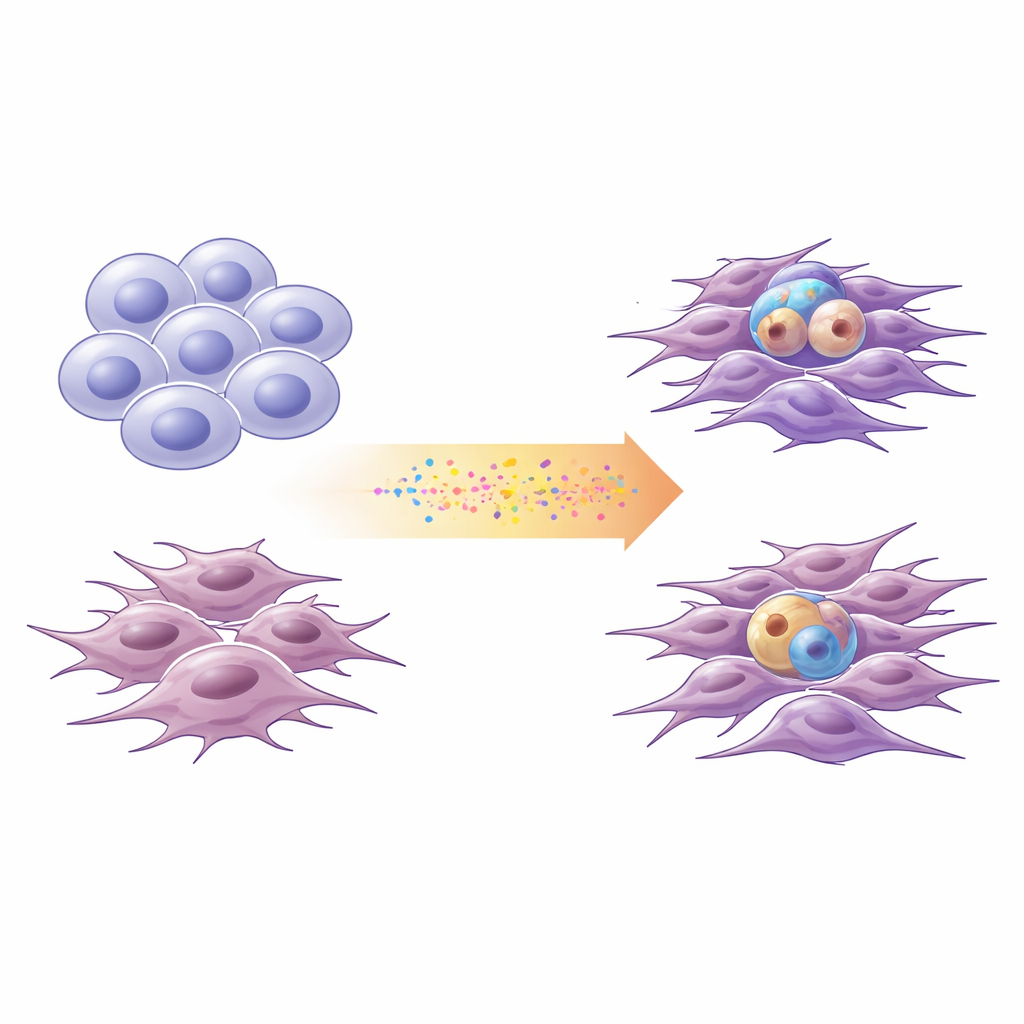
Zwei Hauptausprägungen des Glioblastoms
Forschende beschreiben Glioblastomzellen zunehmend entlang eines Spektrums zwischen zwei breiten Zuständen. „Proneurale“ Zellen ähneln unreifen Nervenzellen: sie teilen sich in stammesähnlicher Weise und können vielfältige Nachkommen hervorbringen. „Mesenchymale“ Zellen wirken eher wie gestresste, widerstandsfähige Überlebende: sie sind beweglicher, invasiver und mit Entzündungszeichen verknüpft. Mit Zellen, die frisch aus vier Patientinnen und Patienten sowie einer Standardlaborzelllinie gewonnen wurden, analysierte das Team DNA‑Veränderungen und Genaktivität, um jede Kultur auf dieser proneural–mesenchymalen Achse zu verorten. Sie bestätigten, dass diese vereinfachte Zwei‑Zustands‑Skala den größten Teil der Transkriptionsvielfalt erfasst, die in großen öffentlichen Glioblastomdatensätzen beobachtet wird.
Stammzell‑ähnliches Verhalten und das CD44‑Rätsel
Stammzellähnliche Eigenschaften — wie die Fähigkeit, als frei schwebende Sphäroide zu wachsen und eine gemischte Population zu regenerieren — werden häufig für Therapieresistenz verantwortlich gemacht. Die Autoren quantifizierten ein publiziertes vier‑Gen‑Programm für Stemness und fanden ein auffälliges Muster: Zellen am proneuralen Ende des Spektrums zeigten konsequent höhere Stemness‑Werte, während mesenchymale Zellen niedriger punkteten. Gleichzeitig betrachteten sie ein kontroverses Oberflächenmolekül, CD44, das manchmal als Stammzellmarker bezeichnet wird, neu. In ihren Händen korrelierte höheres CD44 mit dem mesenchymalen Zustand und mit niedrigerer Stemness, nicht umgekehrt — sowohl in ihren eigenen Kulturen als auch in unabhängigen Datensätzen. Als sie physisch niedrig‑CD44‑ und hoch‑CD44‑Zellen aus einer proneuralen Kultur trennten, verhielt sich die niedrig‑CD44‑Gruppe eher wie Stammzellen — plastischer und in der Lage, die ursprüngliche Mischung wiederherzustellen — während die hoch‑CD44‑Gruppe differenzierter und mesenchymal‑ähnlicher wirkte.
Wie Tumorzellen mit ihrer Umgebung kommunizieren
CD44 ist vor allem als Rezeptor für Hyaluronsäure bekannt, einen zuckerreichen Bestandteil der extrazellulären Matrix des Gehirns. Das Team erweiterte den Blick auf viele hyaluronsäurebindende Proteine. Sie fanden, dass mesenchymale Zellen an der Oberfläche vermehrt Rezeptoren tragen, die diese Matrix anheften und internalisieren können, während proneurale Zellen mehr matrixbildende Komponenten herstellen, die eine schützende Nische formen helfen. Funktionell verlangsamte bei Zugabe von zusätzlicher Hyaluronsäure die Migration mesenchymaler Zellen, was mit ihrer stärkeren Nutzung von Oberflächenrezeptoren vereinbar ist, während proneurale Zellen weniger betroffen waren. Das deutet auf subtyp‑spezifische Mechanismen hin, mit denen Tumor und Mikroumgebung einander verstärken können.
Temozolomid drängt Zellen in einen widerstandsfähigeren Zustand
Der Kern der Studie untersucht, wie diese verschiedenen Zellzustände auf Temozolomid reagieren. In den ersten 24 Stunden schränkten steigende Medikamentendosen das Wachstum mesenchymaler Zellen ein, berührten aber die Teilungsrate proneuraler Zellen kaum. Über 72 Stunden und ein breites Dosis‑Spektrum folgte die Gesamtempfindlichkeit gegenüber dem Medikament (die klassische IC50‑Messung) jedoch nicht einfach dem Subtyp. Simulierten die Forschenden dagegen wiederholte klinische Gaben — behandeln, Erholung zulassen, erneut behandeln — hoben sich die proneuralen Kulturen hervor: Nach einer Exposition wurden sie weniger proliferativ, zeigten jedoch deutlich erhöhte Resistenz gegen eine zweite Runde, während mesenchymale Kulturen nur geringe Veränderungen in ihrer Empfindlichkeit zeigten. Die Genexpressionsanalyse zeigte, dass nahe‑toxische Temozolomid‑Dosen in allen Zellen eine breite „mesenchymale Verschiebung“ antrieben: Signalwege, die mit Entzündung und Gewebsumgestaltung verbunden sind, stiegen, während stemness‑assoziierte Programme sanken, besonders in ursprünglich proneuralen Zellen. Dennoch behielten diese von proneuralen Zellen abgeleiteten Zellen relativ hohes stem‑ähnliches Potenzial, was darauf hindeutet, dass sie sich vorübergehend zusammenziehen, später aber das Rezidiv antreiben könnten.
Sauerstofflevel kippen die Balance der Resistenz
Reale Tumoren sind in ihrer Sauerstoffversorgung ungleichmäßig, und sauerstoffarme Bereiche fördern bekanntermaßen Behandlungsresistenz. Mit Kobaltchlorid, das eine hypoxieähnliche Reaktion auslöst, fanden die Forschenden, dass der Sauerstoffstatus stark mit dem Subtyp interagiert. Unter simuliertem Hypoxie reduzierten proneurale Zellen die Proliferation, steigerten jedoch die Stoffwechselaktivität; in diesem Zustand exponiert gegenüber Temozolomid überlebten sie besser und wanderten mehr. Mesenchymale Zellen dagegen wurden unter demselben hypoxischen Signal tendenziell anfälliger für das Medikament. Als das Team aufzeichnete, wie Hypoxie die Wirksamkeit von Temozolomid im Verhältnis zum Stemness‑Score veränderte, teilten sich die Kulturen in zwei Lager: hoch‑stem‑ähnliche, proneurale‑artige Zellen, die medikamentenresistenter wurden, und niedrig‑stem‑ähnliche, mesenchymale‑artige Zellen, die empfindlicher wurden.
Was das für Patienten und zukünftige Therapien bedeutet
Für eine breite Leserschaft ist die Kernbotschaft: Nicht alle Glioblastome sind biologisch gleich, und diese Unterschiede beeinflussen, wie Tumoren Behandlung überdauern und sich anpassen. Tumoren mit einem Überschuss an proneuralen, stammzellähnlichen Zellen scheinen besonders fähig, Temozolomid zu überstehen, indem sie sich in einen härteren, mesenchymal‑ähnlichen Zustand verschieben und zugleich einen Kern widerstandsfähiger Zellen bewahren — besonders unter niedrigem Sauerstoff. Die Studie legt nahe, dass CD44 und andere hyaluronsäurebezogene Moleküle besser als Merkmale dieser verhärteten mesenchymalen Identität denn als einfache Stammzellmarker verstanden werden. Obwohl die Arbeit auf einer begrenzten Zahl von Zellmodellen beruht und weitgehend korrelativ ist, stützt sie die Verwendung einer einfachen proneural–mesenchymalen Skala zusammen mit Stemness‑Maßen, um Glioblastome zu stratifizieren und Therapien zu entwerfen, die die anpassungsfähigsten, relapse‑treibenden Zellen frühzeitig unterbinden oder entwaffnen.
Zitation: Rancati, S., Campolungo, M., Dalmolin, D.G. et al. Molecular subtypes and the (in vitro) response of glioblastoma to temozolomide. BJC Rep 4, 24 (2026). https://doi.org/10.1038/s44276-026-00228-8
Schlüsselwörter: Glioblastom, Temozolomid-Resistenz, Krebsstammzellen, Tumorhypoxie, molekulare Subtypen