Clear Sky Science · nl
Moleculaire subtypen en de (in vitro) respons van glioblastoom op temozolomide
Waarom deze studie naar hersenkanker ertoe doet
Glioblastoom is de meest voorkomende en dodelijke vorm van hersenkanker bij volwassenen, en zelfs het huidige standaardmiddel, temozolomide, levert meestal slechts enkele extra maanden levensduur op. Deze studie stelt een vraag die directe relevantie heeft voor patiënten en clinici: kan de moleculaire "persoonlijkheid" van een glioblastoom helpen voorspellen hoe het op behandeling zal reageren, en waarom sommige tumoren zo snel medicijnresistent worden?
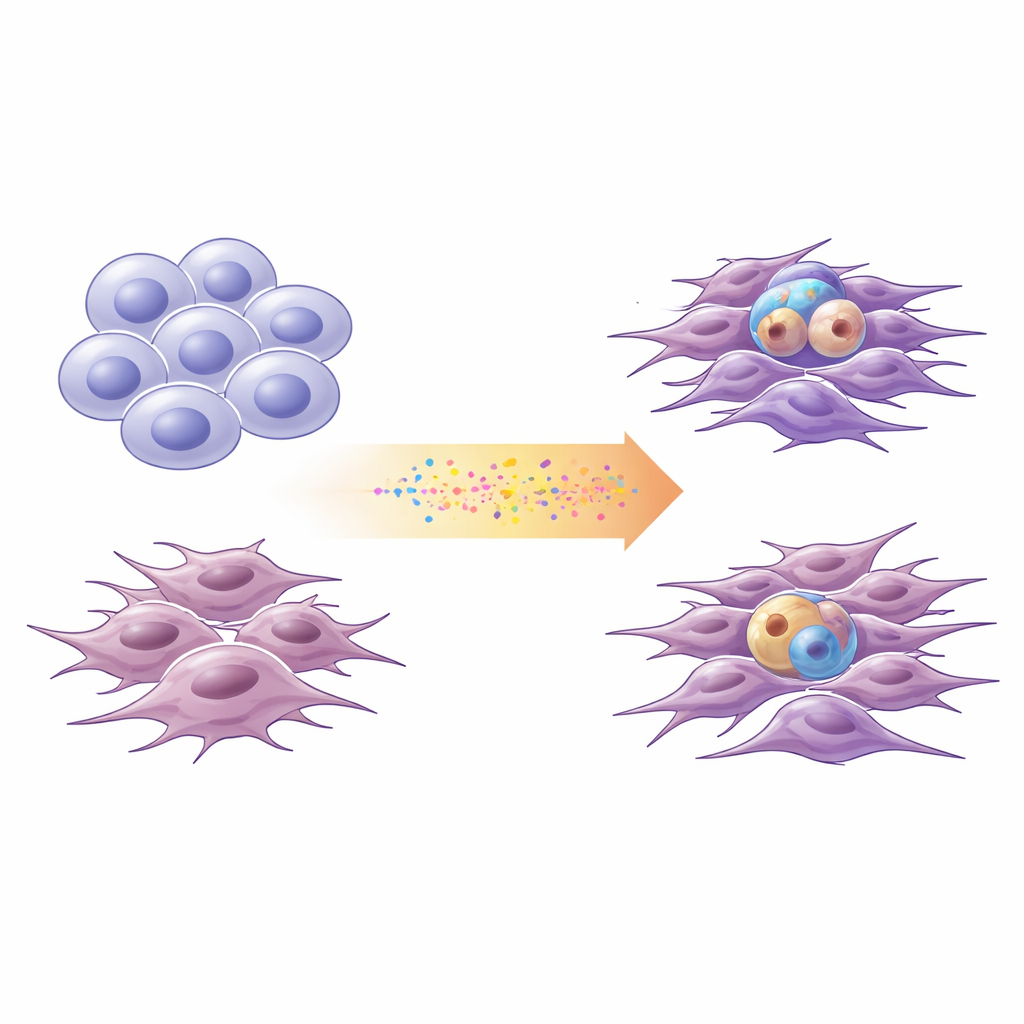
Twee hoofdkarakteren van glioblastoom
Onderzoekers beschrijven glioblastoomcellen steeds vaker langs een spectrum tussen twee brede toestanden. "Proneurale" cellen lijken op onrijpe zenuwcellen: ze delen op een stamcelachtige manier en kunnen diverse nakomelingen voortbrengen. "Mesenchymale" cellen lijken meer op gestresste, geharde overlevers: ze zijn mobieler, invasiever en geassocieerd met ontsteking. Met cellen die recentelijk uit vier patiënten waren verkregen, plus een standaard laboratoriumcelijn, profileerde het team DNA-veranderingen en genactiviteit om elke kweek op deze proneurale–mesenchymale as te plaatsen. Ze bevestigden dat deze vereenvoudigde tweestatenladder het merendeel van de transcriptiediversiteit in grote openbare glioblastoomdatasets vastlegde.
Stamcelachtig gedrag en de CD44-puzzel
Stamcelachtige eigenschappen — zoals het vermogen om als vrijzwevende sferoïden te groeien en een gemengde populatie te regenereren — worden vaak verantwoordelijk gehouden voor therapieresistentie. De auteurs kwantificeerden een gepubliceerde vier-genen stamcelprogramma en vonden een opvallend patroon: cellen aan het proneurale uiteinde van het spectrum toonden consequent hogere stamcelscores, terwijl mesenchymale cellen lagere scores hadden. Tegelijkertijd herbeoordeelden ze een controversiële oppervlaktemolecuul, CD44, soms aangeduid als stamcelmarker. In hun handen correleerde hogere CD44 met de mesenchymale toestand en een lagere stamcelscore, niet andersom, zowel in hun eigen kweekmodellen als in onafhankelijke datasets. Toen ze fysiek laag‑CD44- en hoog‑CD44-cellen scheidden uit een proneurale kweek, gedroeg de laag‑CD44-groep zich meer als stamcellen — plastischer en in staat de oorspronkelijke mix te herbebouwen — terwijl de hoog‑CD44-groep er gedifferentieerder en mesenchymaal‑achtig uitzag.
Hoe tumorcellen met hun omgeving communiceren
CD44 staat vooral bekend als receptor voor hyaluronzuur, een suikerrijk bestanddeel van de extracellulaire matrix van de hersenen. Het team verbreedde hun blik om veel hyaluronzuur‑bindende eiwitten mee te nemen. Ze vonden dat mesenchymale cellen verrijkt waren in oppervlaktereceptoren die aan deze matrix kunnen hechten en deze kunnen internaliseren, terwijl proneurale cellen meer matrixopbouwende componenten produceerden die helpen een beschermend niche te vormen. Functioneel gezien, wanneer ze temozolomide combineerden met extra hyaluronzuur, vertraagden mesenchymale cellen hun migratie, consistent met hun zwaardere gebruik van oppervlaktereceptoren, terwijl proneurale cellen minder werden beïnvloed. Dit wijst op subtypespecifieke manieren waarop de tumor en zijn micro‑omgeving elkaar kunnen versterken.
Temozolomide duwt cellen richting een hardere staat
De kern van de studie onderzoekt hoe deze verschillende celtoestanden op temozolomide reageren. In de eerste 24 uur remden toenemende geneesmiddeldoses de groei van mesenchymale cellen, maar raakten ze de delingssnelheid van proneurale cellen nauwelijks. Over 72 uur en over een breed dosisbereik volgde de algemene geneesmiddelgevoeligheid (de klassieke IC50‑maat) echter niet eenvoudig het subtype. Toen het team herhaalde klinische doseringsschema's nabootste — behandelen, herstel toestaan en opnieuw behandelen — staken proneurale kweekmodellen eruit: na één blootstelling werden ze minder proliferatief maar duidelijk resistenter tegen een tweede ronde, terwijl mesenchymale kweekmodellen weinig veranderden in hun gevoeligheid. Genexpressieanalyse toonde aan dat nabij‑toxische temozolomidedoses een brede "mesenchymale verschuiving" in alle cellen dreven: paden gekoppeld aan ontsteking en weefselherstructurering stegen, terwijl stamcelgeassocieerde programma's daalden, vooral in aanvankelijk proneurale cellen. Toch behielden deze uit proneurale oorsprong afkomstige cellen relatief hoog stamcelpotentieel, wat suggereert dat ze zich tijdelijk kunnen terugtrekken maar later relapse kunnen aansturen.
Zuurstofniveaus kantelen de balans van resistentie
Reële tumoren zijn ongelijk qua zuurstoftoevoer, en laag‑zuurstofgebieden bevorderen bekend resistentie tegen behandeling. Met behulp van kobaltblakchloride om een hypoxie‑achtig antwoord te activeren, vonden de onderzoekers dat de zuurstofstatus sterk met subtype interageerde. Onder gesimuleerde hypoxie verminderden proneurale cellen hun proliferatie maar verhoogden hun metabole activiteit, en wanneer ze in deze toestand aan temozolomide werden blootgesteld, overleefden ze beter en migreerden ze meer. Mesenchymale cellen daarentegen leken onder hetzelfde hypoxische signaal juist vatbaarder voor het geneesmiddel te worden. Toen het team uittekende hoe hypoxie de werkzaamheid van temozolomide veranderde ten opzichte van de stamcelscore, vielen de kweekmodellen in twee kampen: hoog‑stamachtige, proneurale‑achtige cellen die drugresistenter werden, en laag‑stamachtige, mesenchymale‑achtige cellen die gevoeliger werden.
Wat dit betekent voor patiënten en toekomstige therapieën
Voor een niet‑specialistische lezer is de kernboodschap dat niet alle glioblastomen biologisch hetzelfde zijn, en dat deze verschillen ertoe doen voor hoe tumoren behandeling doorstaan en zich daaraan aanpassen. Tumoren die rijker zijn aan proneurale, stamcelachtige cellen lijken bijzonder goed in staat temozolomide te doorstaan, zich te verschuiven naar een hardere mesenchymale‑achtige staat terwijl ze een kern van veerkrachtige cellen behouden, met name onder laag‑zuurstofomstandigheden. De studie suggereert dat CD44 en andere hyaluronzuurgerelateerde moleculen beter gezien kunnen worden als kenmerken van deze geharde mesenchymale identiteit, niet als simpele stamcelindicatoren. Hoewel gebaseerd op een bescheiden aantal celmodellen en grotendeels correlatief, ondersteunt het werk het gebruik van een eenvoudige proneurale–mesenchymale schaal, plus stamcelmetingen, om glioblastomen te stratifiëren en therapieën te ontwerpen die de meest aanpasbare, relapse‑drijvende cellen vooraf kunnen tegenwerken of uitschakelen.
Bronvermelding: Rancati, S., Campolungo, M., Dalmolin, D.G. et al. Molecular subtypes and the (in vitro) response of glioblastoma to temozolomide. BJC Rep 4, 24 (2026). https://doi.org/10.1038/s44276-026-00228-8
Trefwoorden: glioblastoom, resistentie tegen temozolomide, kankerstamcellen, tumorhypoxie, moleculaire subtypen