Clear Sky Science · it
Sottotipi molecolari e la risposta (in vitro) del glioblastoma al temozolomide
Perché questo studio sul cancro cerebrale è importante
Il glioblastoma è la forma di tumore cerebrale più comune e letale negli adulti, e perfino il farmaco standard attuale, il temozolomide, in genere regala solo alcuni mesi di vita in più. Questo studio pone una domanda di immediata rilevanza per pazienti e clinici: la «personalità» molecolare di un glioblastoma può aiutare a prevedere la risposta al trattamento, e spiegare perché alcuni tumori diventano così rapidamente resistenti ai farmaci?
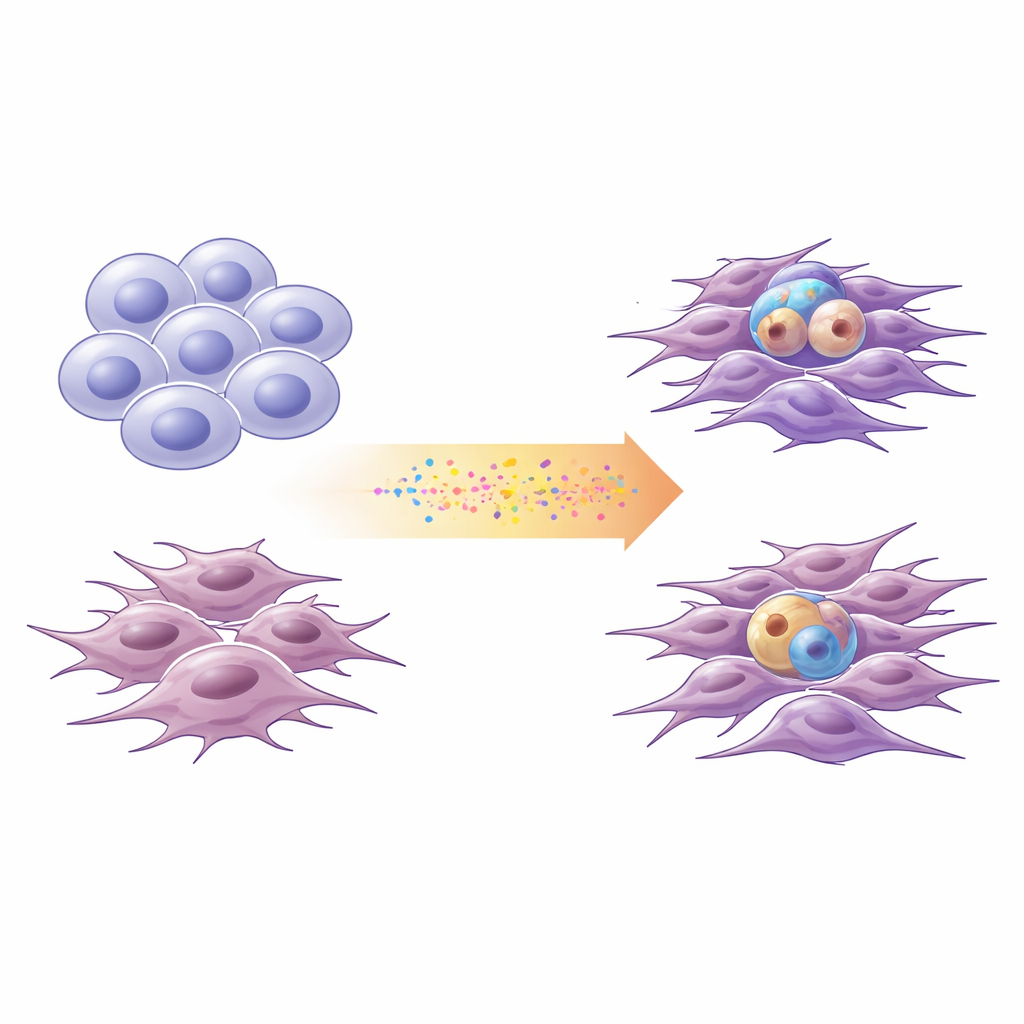
Due principali varianti del glioblastoma
I ricercatori descrivono sempre più spesso le cellule di glioblastoma lungo uno spettro che va tra due stati generali. Le cellule «proneurali» somigliano a cellule nervose immature: si dividono in modo simile a cellule staminali e possono generare discendenti diversi. Le cellule «mesenchimali» appaiono più come sopravvissute stressate e indurite: sono più mobili, invasive e associate all’infiammazione. Usando cellule derivate recentemente da quattro pazienti, insieme a una linea cellulare standard di laboratorio, il gruppo ha profilato le alterazioni del DNA e l’attività genica per collocare ogni coltura su questo asse proneurale–mesenchimale. Hanno confermato che questa scala semplificata a due stati cattura gran parte della diversità trascrizionale osservata in ampi dataset pubblici sul glioblastoma.
Comportamento simile a cellule staminali e il rompicapo CD44
Proprietà simili a quelle staminali — come la capacità di crescere come sfere in sospensione e di rigenerare una popolazione mista — sono spesso ritenute responsabili della resistenza alle terapie. Gli autori hanno quantificato un programma di «stemness» a quattro geni pubblicato e hanno trovato un pattern sorprendente: le cellule all’estremità proneurale dello spettro mostravano costantemente punteggi di stemness più elevati, mentre le cellule mesenchimali aveva punteggi inferiori. Allo stesso tempo, hanno riesaminato una molecola di superficie controversa, CD44, talvolta indicata come marcatore di cellule staminali. Nella loro esperienza, livelli più alti di CD44 si associavano allo stato mesenchimale e a una stemness inferiore, non il contrario, sia nelle loro colture sia in dataset indipendenti. Quando hanno separato fisicamente cellule a basso CD44 e ad alto CD44 da una coltura proneurale, il gruppo a basso CD44 si comportava più da cellule staminali — più plastiche e in grado di ripopolare la miscela originale — mentre il gruppo ad alto CD44 appariva più differenziato e di tipo mesenchimale.
Come le cellule tumorali comunicano con l’ambiente circostante
CD44 è noto principalmente come recettore dell’acido ialuronico, un componente ricco di zuccheri della matrice extracellulare cerebrale. Il team ha ampliato la propria indagine includendo molte proteine leganti l’acido ialuronico. Hanno scoperto che le cellule mesenchimali erano arricchite in recettori di superficie che possono agganciarsi e internalizzare questa matrice, mentre le cellule proneurali producevano più componenti costitutivi della matrice che contribuiscono a modellare una nicchia protettiva. Funzionalmente, quando hanno combinato il temozolomide con acido ialuronico aggiuntivo, le cellule mesenchimali rallentavano la migrazione, coerente con il loro maggiore uso di recettori di superficie, mentre le cellule proneurali risultavano meno influenzate. Questo indica modalità specifiche di sottotipo con cui il tumore e il microambiente possono rinforzarsi a vicenda.
Il temozolomide spinge le cellule verso uno stato più duro
Il nucleo dello studio affronta come questi diversi stati cellulari rispondono al temozolomide. Nelle prime 24 ore, dosi crescenti di farmaco riducevano la crescita delle cellule mesenchimali, ma incidevano appena sul tasso di divisione delle cellule proneurali. Su 72 ore e su un ampio intervallo di dosi, la sensibilità complessiva al farmaco (la classica misura IC50) non seguiva semplicemente il sottotipo. Tuttavia, quando il gruppo ha simulato dosaggi clinici ripetuti — trattando, permettendo il recupero e poi trattando di nuovo — le colture proneurali sono emerse in modo distinto: dopo una esposizione divenivano meno proliferative ma marcamente più resistenti a un secondo ciclo, mentre le colture mesenchimali mostravano pochi cambiamenti nella sensibilità. L’analisi dell’espressione genica ha mostrato che dosi di temozolomide prossime alla tossicità inducevano un ampio «spostamento mesenchimale» in tutte le cellule: aumentavano le vie legate all’infiammazione e al rimodellamento tissutale, mentre i programmi associati alla stemness calavano, specialmente nelle cellule inizialmente proneurali. Eppure queste cellule di origine proneurale conservavano un potenziale relativamente alto di tipo staminale, suggerendo che possono contrarsi temporaneamente ma in seguito alimentare la recidiva.
I livelli di ossigeno inclinano l’equilibrio della resistenza
I tumori reali presentano distribuzione irregolare dell’ossigeno, e le aree a basso ossigeno sono note per favorire la resistenza al trattamento. Usando il cloruro di cobalto per indurre una risposta simile all’ipossia, i ricercatori hanno osservato che lo stato di ossigenazione interagiva fortemente con il sottotipo. Sotto ipossia simulata, le cellule proneurali riducevano la proliferazione ma aumentavano l’attività metabolica, e se esposte al temozolomide in questo stato sopravvivevano meglio e migravano di più. Le cellule mesenchimali, al contrario, tendevano a diventare più vulnerabili al farmaco sotto lo stesso segnale ipossico. Quando il gruppo ha tracciato come l’ipossia modificava la potenza del temozolomide rispetto al punteggio di stemness, le colture si raggruppavano in due campi: cellule ad alta stemness, di tipo proneurale, che diventavano più resistenti, e cellule a bassa stemness, di tipo mesenchimale, che diventavano più sensibili.
Cosa significa per i pazienti e le terapie future
Per il lettore non specialista, il messaggio chiave è che non tutti i glioblastomi sono biologicamente uguali, e queste differenze contano per il modo in cui i tumori resistono e si adattano al trattamento. I tumori più ricchi di cellule proneurali, simili a cellule staminali, sembrano particolarmente capaci di sopportare il temozolomide, spostandosi verso uno stato più duro di tipo mesenchimale pur preservando un nucleo di cellule resilienti, specialmente in condizioni di basso ossigeno. Lo studio suggerisce che CD44 e altre molecole legate all’acido ialuronico sono meglio interpretate come segni distintivi di questa identità mesenchimale indurita, non come semplici indicatori di cellule staminali. Pur basato su un numero modesto di modelli cellulari e in gran parte correlative, il lavoro supporta l’uso di una semplice scala proneurale–mesenchimale, insieme a misure di stemness, per stratificare i glioblastomi e progettare terapie che prevengano o disarmino le cellule più adattabili e promotrici di recidiva.
Citazione: Rancati, S., Campolungo, M., Dalmolin, D.G. et al. Molecular subtypes and the (in vitro) response of glioblastoma to temozolomide. BJC Rep 4, 24 (2026). https://doi.org/10.1038/s44276-026-00228-8
Parole chiave: glioblastoma, resistenza al temozolomide, cellule staminali tumorali, ipossia tumorale, sottotipi molecolari