Clear Sky Science · pl
Podtypy molekularne i (in vitro) odpowiedź glejaków na temozolomid
Dlaczego to badanie nowotworu mózgu ma znaczenie
Glejak wielopostaciowy jest najczęstszą i najgroźniejszą postacią raka mózgu u dorosłych, a nawet obecny standard leczenia — temozolomid — zwykle wydłuża życie jedynie o kilka miesięcy. W tym badaniu postawiono pytanie mające bezpośrednie znaczenie dla pacjentów i klinicystów: czy molekularna „osobowość” glejaka może przewidywać jego odpowiedź na leczenie i wyjaśniać, dlaczego niektóre guzy tak szybko stają się oporne na lek?
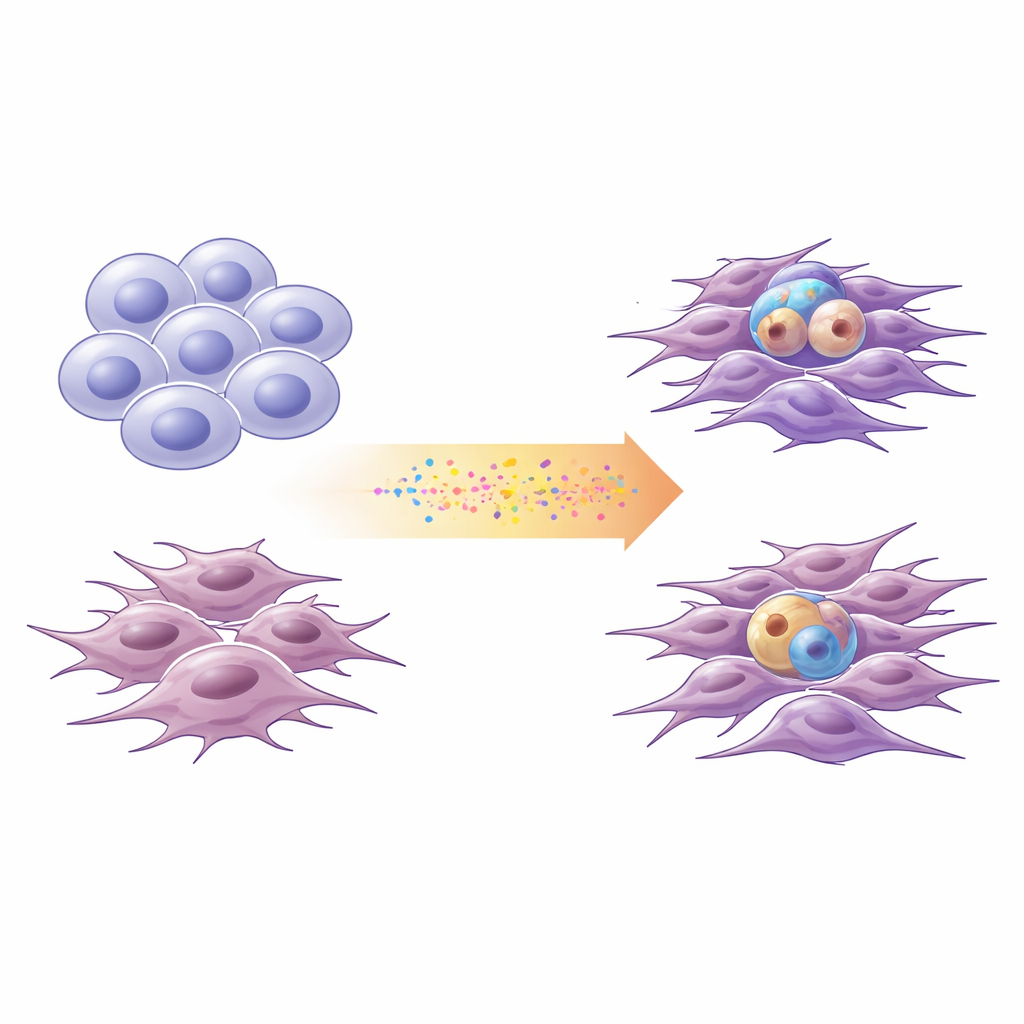
Dwa główne odcienie glejaka
Naukowcy coraz częściej opisują komórki glejaka na kontinuum między dwoma szerokimi stanami. Komórki „proneuralne” przypominają niedojrzałe komórki nerwowe: dzielą się w sposób zbliżony do komórek macierzystych i potrafią dawać różnorodnych potomków. Komórki „mezenchymalne” wyglądają bardziej jak zestresowani, zahartowani przeżywający: są bardziej ruchliwe, inwazyjne i powiązane z zapaleniem. Korzystając z komórek świeżo wyizolowanych od czterech pacjentów oraz z jednej standardowej linii laboratoryjnej, zespół przeanalizował zmiany DNA i aktywność genów, aby umieścić każdą hodowlę na osi proneural–mezenchymal. Potwierdzili, że to uproszczone dwu‑stanowe ujęcie odzwierciedla większość różnorodności transkrypcyjnej obserwowanej w dużych publicznych zbiorach danych dotyczących glejaka.
Zachowanie podobne do komórek macierzystych i zagadka CD44
Cechy przypominające komórki macierzyste — takie jak zdolność do wzrostu jako unoszące się spheroidy i do odtwarzania mieszanej populacji — często obwinia się o oporność na terapię. Autorzy zmierzyli opublikowany program czterech genów związanych ze stemness i znaleźli uderzający wzorzec: komórki na proneuralnym końcu spektrum konsekwentnie wykazywały wyższe wyniki stemness, podczas gdy komórki mezenchymalne miały niższe wyniki. Jednocześnie powrócili do kontrowersyjnej cząsteczki powierzchniowej CD44, czasem uznawanej za marker komórek macierzystych. W ich doświadczeniach wyższe poziomy CD44 korelowały ze stanem mezenchymalnym i z niższym stemness, a nie odwrotnie — zarówno w ich własnych hodowlach, jak i w niezależnych zbiorach danych. Gdy fizycznie rozdzielili komórki o niskim i wysokim poziomie CD44 z hodowli proneuralnej, grupa o niskim CD44 zachowywała się bardziej jak komórki macierzyste — bardziej plastyczna i zdolna do ponownego zasiedlenia pierwotnej mieszanki — podczas gdy grupa o wysokim CD44 wyglądała na bardziej zróżnicowaną i przypominającą komórki mezenchymalne.
Jak komórki guza komunikują się z otoczeniem
CD44 jest najbardziej znane jako receptor dla kwasu hialuronowego, bogatego w cukry składnika zewnątrzkomórkowej macierzy mózgu. Zespół rozszerzył swoje spojrzenie o wiele białek wiążących kwas hialuronowy. Stwierdzili, że komórki mezenchymalne są wzbogacone w receptory powierzchniowe, które mogą przyłączać i internalizować tę macierz, podczas gdy komórki proneuralne wytwarzają więcej składników budujących macierz, które pomagają kształtować ochronne nisze. Funkcjonalnie, gdy połączyli temozolomid z dodatkiem kwasu hialuronowego, komórki mezenchymalne spowolniły migrację, co zgadza się z ich intensywniejszym wykorzystaniem receptorów powierzchniowych, podczas gdy komórki proneuralne były mniej dotknięte. Wskazuje to na specyficzne dla podtypu sposoby, w jakie guz i jego mikrośrodowisko mogą się wzajemnie wzmacniać.
Temozolomid przesuwa komórki w kierunku twardszego stanu
Istota badania dotyczy tego, jak te różne stany komórkowe reagują na temozolomid. W pierwszych 24 godzinach rosnące dawki leku ograniczały wzrost komórek mezenchymalnych, ale ledwie wpływały na tempo podziału komórek proneuralnych. W ciągu 72 godzin i przy szerokim zakresie dawek ogólna wrażliwość na lek (klasyczna miara IC50) nie podążała po prostu za podtypem. Jednak gdy zespół odwzorował powtarzane dawkowanie kliniczne — leczenie, umożliwienie regeneracji, a następnie ponowne leczenie — hodowle proneuralne wyróżniały się: po jednej ekspozycji stały się mniej proliferatywne, ale wyraźnie bardziej oporne na drugą rundę, podczas gdy hodowle mezenchymalne niewiele zmieniały swoją wrażliwość. Analiza ekspresji genów wykazała, że dawki temozolomidu bliskie toksycznym wywoływały szerokie „przejście mezenchymalne” we wszystkich komórkach: wzrastały szlaki związane z zapaleniem i przebudową tkanki, podczas gdy programy związane ze stemness spadały, szczególnie w początkowo proneuralnych komórkach. Mimo to te komórki pochodzące z proneuralnego stanu zachowały stosunkowo wysoką potencję podobną do komórek macierzystych, sugerując, że mogą tymczasowo się skurczyć, a potem napędzać nawroty.
Poziom tlenu przechyla równowagę oporności
Prawdziwe guzy mają niejednorodne zaopatrzenie w tlen, a obszary o niskim natlenieniu sprzyjają oporności na leczenie. Używając chlorku kobaltu do wywołania odpowiedzi podobnej do hipoksji, badacze stwierdzili, że stan tlenowy silnie wchodzi w interakcję z podtypem. Pod symulowaną hipoksją komórki proneuralne zmniejszały proliferację, ale zwiększały aktywność metaboliczną, a gdy w tym stanie wystawia się je na temozolomid, przeżywały lepiej i bardziej migrowały. Komórki mezenchymalne, w przeciwieństwie do tego, miały tendencję do większej wrażliwości na lek przy tym samym sygnale hipoksycznym. Gdy zespół wykreślił, jak hipoksja zmienia siłę działania temozolomidu względem wyniku stemness, hodowle podzieliły się na dwa obozy: o wysokim stemness, przypominające proneuralne, które stawały się bardziej oporne na lek, oraz o niskim stemness, przypominające mezenchymalne, które stawały się bardziej wrażliwe.
Co to oznacza dla pacjentów i przyszłych terapii
Dla czytelnika niebędącego specjalistą kluczowy wniosek jest taki, że nie wszystkie glejaki są biologicznie takie same i te różnice mają znaczenie dla tego, jak guzy przetrwają i zaadaptują się do leczenia. Guzy bogatsze w komórki proneuralne, o właściwościach przypominających komórki macierzyste, wydają się szczególnie zdolne przetrwać terapię temozolomidem, przesuwając się w kierunku twardszego, mezenchymalnego stanu, jednocześnie zachowując rdzeń odpornych komórek, zwłaszcza w warunkach niskiego natlenienia. Badanie sugeruje, że CD44 i inne molekuły związane z kwasem hialuronowym lepiej postrzegać jako cechy tej zahartowanej, mezenchymalnej tożsamości, a nie proste markery komórek macierzystych. Choć oparto je na ograniczonej liczbie modeli komórkowych i w dużej mierze korelacjach, praca wspiera użycie prostej skali proneural–mezenchymal oraz miar stemness do stratyfikacji glejaków i projektowania terapii, które będą uprzedzać lub unieszkodliwiać najbardziej adaptacyjne komórki napędzające nawroty.
Cytowanie: Rancati, S., Campolungo, M., Dalmolin, D.G. et al. Molecular subtypes and the (in vitro) response of glioblastoma to temozolomide. BJC Rep 4, 24 (2026). https://doi.org/10.1038/s44276-026-00228-8
Słowa kluczowe: glejak, oporność na temozolomid, komórki macierzyste nowotworu, hipoksja guza, podtypy molekularne