Clear Sky Science · pt
Subtipos moleculares e a resposta (in vitro) de glioblastoma ao temozolomida
Por que este estudo sobre câncer cerebral importa
O glioblastoma é a forma mais comum e letal de câncer cerebral em adultos, e mesmo o medicamento padrão atual, temozolomida, normalmente só proporciona alguns meses a mais de vida. Este estudo faz uma pergunta de relevância direta para pacientes e clínicos: a “personalidade” molecular de um glioblastoma pode ajudar a prever como ele responderá ao tratamento, e por que alguns tumores se tornam rapidamente resistentes ao fármaco?
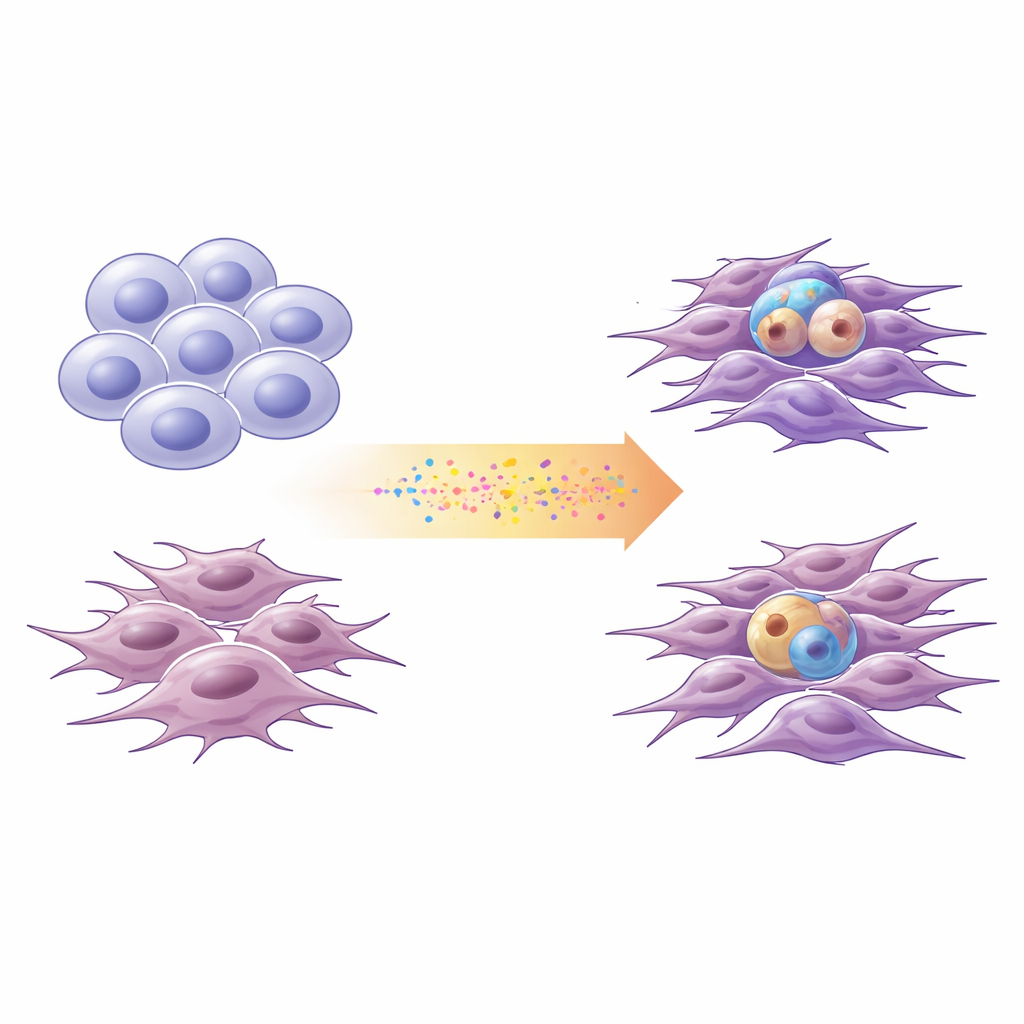
Dois principais perfis de glioblastoma
Pesquisadores descrevem cada vez mais as células de glioblastoma ao longo de um espectro entre dois estados amplos. Células “proneurais” se assemelham a células nervosas imaturas: dividem‑se de maneira semelhante a células‑tronco e podem gerar descendentes diversos. Células “mesenquimais” lembram sobreviventes endurecidos e estressados: são mais móveis, invasivas e associadas à inflamação. Usando células recém‑derivadas de quatro pacientes, além de uma linhagem padrão de laboratório, a equipe perfilou alterações no DNA e atividade gênica para posicionar cada cultura ao longo desse eixo proneural–mesenquimal. Confirmaram que essa escala simplificada de dois estados capturou a maior parte da diversidade transciptômica observada em grandes conjuntos públicos de dados de glioblastoma.
Comportamento semelhante ao de células‑tronco e o enigma do CD44
Propriedades semelhantes às de células‑tronco — como a capacidade de crescer como esferoides suspensos e de regenerar uma população mista — são frequentemente responsabilizadas pela resistência às terapias. Os autores quantificaram um programa de «stemness» publicado com quatro genes e encontraram um padrão marcante: células no extremo proneural do espectro exibiram consistentemente escores de stemness mais altos, enquanto células mesenquimais pontuaram mais baixo. Ao mesmo tempo, revisitaram uma molécula de superfície controversa, CD44, às vezes chamada de marcador de célula‑tronco. Em suas mãos, maior expressão de CD44 acompanhou o estado mesenquimal e menor stemness, não o contrário, tanto em suas próprias culturas quanto em conjuntos de dados independentes. Quando separaram fisicamente células de baixo‑CD44 e alto‑CD44 de uma cultura proneural, o grupo de baixo‑CD44 comportou‑se mais como células‑tronco — mais plástico e capaz de repovoar a mistura original — enquanto o grupo de alto‑CD44 parecia mais diferenciado e do tipo mesenquimal.
Como as células tumorais se comunicam com seu entorno
O CD44 é mais conhecido como um receptor de ácido hialurônico, um componente rico em açúcares da matriz extracelular do cérebro. A equipe ampliou a análise para incluir muitas proteínas que se ligam ao ácido hialurônico. Descobriram que células mesenquimais eram enriquecidas em receptores de superfície capazes de se ligar e internalizar essa matriz, enquanto células proneurais produziam mais componentes construtores da matriz que ajudam a moldar um nicho protetor. Funcionalmente, quando combinaram temozolomida com ácido hialurônico adicional, células mesenquimais reduziram sua migração, coerente com seu uso maior de receptores de superfície, ao passo que células proneurais foram menos afetadas. Isso aponta para maneiras específicas por subtipo em que o tumor e seu microambiente podem reforçar‑se mutuamente.
Temozolomida empurra as células para um estado mais resistente
O cerne do estudo aborda como esses diferentes estados celulares respondem à temozolomida. Nas primeiras 24 horas, doses crescentes de fármaco contiveram o crescimento das células mesenquimais, mas quase não afetaram a taxa de divisão das células proneurais. Ao longo de 72 horas e em uma ampla faixa de doses, a sensibilidade geral ao fármaco (a medida clássica de IC50) não seguiu simplesmente o subtipo. No entanto, quando a equipe imitou a dosagem clínica repetida — tratar, permitir recuperação e então tratar novamente — as culturas proneurais se destacaram: após uma exposição ficaram menos proliferativas, mas marcadamente mais resistentes a uma segunda rodada, enquanto as culturas mesenquimais mudaram pouco em sua sensibilidade. A análise de expressão gênica mostrou que doses de temozolomida próximas do tóxico induziram um amplo “deslocamento mesenquimal” em todas as células: vias ligadas à inflamação e remodelamento tecidual aumentaram, enquanto programas associados à stemness caíram, especialmente em células inicialmente proneurais. Ainda assim, essas células derivadas de proneurais mantiveram potencial relativamente alto similar ao de células‑tronco, sugerindo que podem contrair‑se temporariamente mas depois alimentar recaídas.
Níveis de oxigênio inclinam a balança da resistência
Tumores reais são irregulares no fornecimento de oxigênio, e bolsões de baixo oxigênio são conhecidos por favorecer a resistência ao tratamento. Usando cloreto de cobalto para desencadear uma resposta semelhante à hipóxia, os pesquisadores descobriram que o estado de oxigênio interagia fortemente com o subtipo. Sob hipóxia simulada, células proneurais reduziram a proliferação mas aumentaram a atividade metabólica, e quando expostas à temozolomida nesse estado sobreviveram melhor e migraram mais. Células mesenquimais, em contraste, tenderam a ficar mais vulneráveis ao fármaco sob o mesmo sinal hipóxico. Quando a equipe traçou como a hipóxia alterou a potência da temozolomida em relação ao escore de stemness, as culturas dividiram‑se em dois grupos: células de alto stemness, do tipo proneural, que se tornaram mais resistentes ao fármaco, e células de baixo stemness, do tipo mesenquimal, que se tornaram mais sensíveis.
O que isso significa para pacientes e terapias futuras
Para o leitor leigo, a mensagem-chave é que nem todos os glioblastomas são biologicamente iguais, e essas diferenças importam para como os tumores resistem e se adaptam ao tratamento. Tumores com maior proporção de células proneurais, semelhantes a células‑tronco, parecem especialmente capazes de resistir à temozolomida, deslocando‑se para um estado mais duro, do tipo mesenquimal, enquanto preservam um núcleo de células resilientes, particularmente em condições de baixo oxigênio. O estudo sugere que CD44 e outras moléculas relacionadas ao ácido hialurônico são melhor interpretadas como marcas dessa identidade mesenquimal endurecida, e não como simples bandeiras de células‑tronco. Embora baseado em um número modesto de modelos celulares e em grande parte correlacional, o trabalho apoia o uso de uma escala simples proneural–mesenquimal, junto com medidas de stemness, para estratificar glioblastomas e projetar terapias que prevejam ou desarmem as células mais adaptáveis e promotoras de recaída.
Citação: Rancati, S., Campolungo, M., Dalmolin, D.G. et al. Molecular subtypes and the (in vitro) response of glioblastoma to temozolomide. BJC Rep 4, 24 (2026). https://doi.org/10.1038/s44276-026-00228-8
Palavras-chave: glioblastoma, resistência ao temozolomida, células‑tronco cancerosas, hipóxia tumoral, subtipos moleculares