Clear Sky Science · ar
الأنماط الجزيئية واستجابة الورم الدبقي الخبيث (في المختبر) للتيموزولوميد
لماذا تهم هذه الدراسة لسرطان الدماغ
الورم الدبقي الخبيث هو الشكل الأكثر شيوعًا والأكثر فتكًا من سرطانات الدماغ لدى البالغين، وحتى الدواء القياسي الحالي، التيموزولوميد، عادةً ما يمنح بضعة أشهر إضافية فقط. تطرح هذه الدراسة سؤالًا ذا صلة مباشرة بالمرضى والأطباء: هل يمكن لـ "شخصية" الورم الدبقي الجزيئية أن تساعد في التنبؤ بكيفية استجابته للعلاج، ولماذا تصبح بعض الأورام مقاومة للدواء بسرعة؟
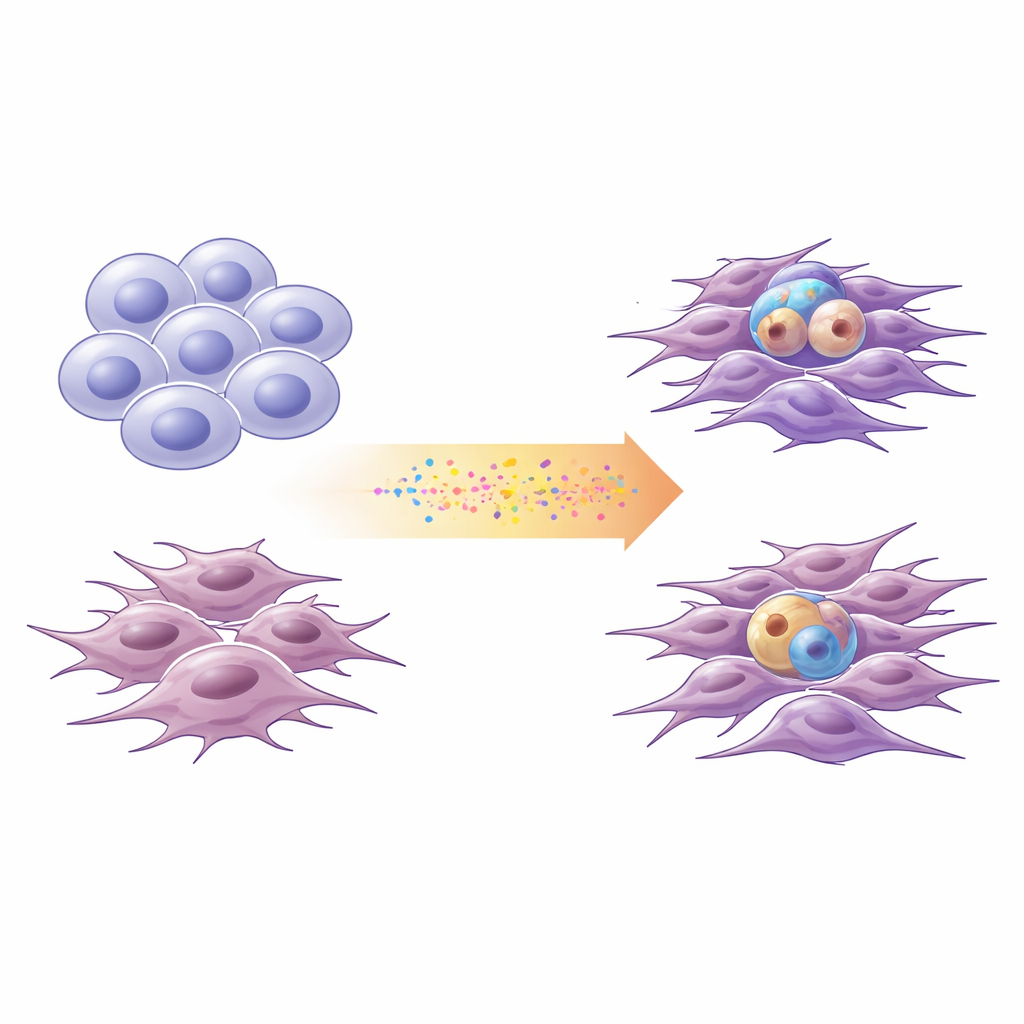
شكلان رئيسيان للورم الدبقي الخبيث
يصف الباحثون خلايا الورم الدبقي الخبيث بشكل متزايد على طيف بين حالتين عامتين. تشبه الخلايا "المستقبلية العصبية" الخلايا العصبية غير الناضجة: تنقسم بطريقة شبيهة بالخلايا الجذعية ويمكنها إنتاج أحفاد متنوعين. تبدو الخلايا "الطباعية الميزنشيمية" أقرب إلى الناجين المتصلبين من الإجهاد: فهي أكثر حركة وغزوًا ومرتبطة بالالتهاب. باستخدام خلايا مُستخلصة حديثًا من أربعة مرضى، بالإضافة إلى سلالة خلوية مختبرية قياسية، قاس الفريق تغيّرات الحمض النووي والنشاط الجيني لوضع كل مزرعة على هذا المحور المستقبلي–الميزنشيمي. وأكدوا أن هذا المقياس المبسط المكوَّن من حالتين يلتقط معظم التنوع النسخي المرصود في مجموعات بيانات عامة كبيرة للورم الدبقي الخبيث.
سلوك شبيه بالجذع وحيرة CD44
غالبًا ما تُلقى خصائص الشبيهة بالجذع—مثل القدرة على النمو على شكل كُرات عائمة وإعادة توليد مجتمع خليوي مختلط—باللوم على المقاومة للعلاج. كمَّن المؤلفون برنامجًا منشورًا مكوّنًا من أربعة جينات لقياس الشبيهة بالجذع ووجدوا نمطًا لافتًا: أظهرت الخلايا عند الطرف المستقبلي طيلة الطيف درجات أعلى من الشبيهة بالجذع، بينما سجلت الخلايا الميزنشيمية درجات أقل. وفي الوقت نفسه أعادوا النظر في جزيء سطحي مثير للجدل، CD44، الذي يُطلق عليه أحيانًا علامة الخلايا الجذعية. في تجاربهم، ارتبطت مستويات أعلى من CD44 بالحالة الميزنشيمية ومع شبيهة جذعية أقل، لا العكس، سواء في مزراعاتهم أو في مجموعات بيانات مستقلة. عندما فصلوا فعليًا خلايا منخفضة CD44 وعالية CD44 من مزرعة ذات طابع مستقبلي، تصرفت مجموعة منخفضة CD44 بشكل أقرب للخلايا الجذعية—أكثر مرونة وقادرة على إعادة تجديد الخليط الأصلي—بينما بدت مجموعة عالية CD44 أكثر تمايزًا وتشبه الطابع الميزنشيمي.
كيف تتواصل خلايا الورم مع محيطها
يشتهر CD44 بكونه مستقبلًا لحمض الهيالورونيك، وهو مكوّن غني بالسكريات من مصفوفة الدماغ خارج الخلوية. وسّع الفريق نظرتهم لتشمل العديد من البروتينات المَربوطة بحمض الهيالورونيك. وجدوا أن الخلايا الميزنشيمية كانت غنية بالمستقبلات السطحية القادرة على الالتصاق وابتلاع هذه المصفوفة، بينما كانت الخلايا المستقبلية تنتج مكونات بناء للمصفوفة تساعد في تشكيل ملاذ وقائي. وظيفيًا، عند دمج التيموزولوميد مع حمض هيالورونيك إضافي، بطأت هجرة الخلايا الميزنشيمية، بما يتوافق مع استخدامها الأكبر للمستقبلات السطحية، بينما تأثرت الخلايا المستقبلية أقل. وتشير هذه النتيجة إلى طرق نوعية يطوِّر بها الورم وميكروبيئته دعماً متبادلاً لكل منهما.
التيموزولوميد يدفع الخلايا نحو حالة أشد
يناقش جوهر الدراسة كيف تستجيب هذه الحالات الخلوية المختلفة للتيموزولوميد. خلال أول 24 ساعة، قلَّلت جرعات دوائية متزايدة نمو الخلايا الميزنشيمية، لكنها لم تؤثر تقريبًا على معدل انقسام الخلايا المستقبلية. على مدى 72 ساعة وعبر نطاق واسع من الجرعات، لم تتبع حساسية الدواء العامة (مقياس IC50 الكلاسيكي) النمط الفرعي بشكل مباشر. ومع ذلك، عندما قلّد الفريق التناول السريري المتكرر—علاج، السماح بالتعافي، ثم العلاج مجددًا—برزت المزارع المستقبلية: بعد تعرض واحد أصبحت أقل تكاثرًا لكن أكثر مقاومة للدورة الثانية بشكل ملحوظ، بينما لم تتغير حساسية المزارع الميزنشيمية كثيرًا. أظهر تحليل التعبير الجيني أن جرعات التيموزولوميد القريبة من السمية حفزت "تحولًا ميزنشيميًا" واسع النطاق في جميع الخلايا: ارتفعت المسارات المرتبطة بالالتهاب وإعادة تشكيل الأنسجة، بينما انخفضت البرامج المرتبطة بالشبيهة بالجذع، وخصوصًا في الخلايا التي كانت مستقبلية في البداية. ومع ذلك احتفظت هذه الخلايا المشتقة من النوع المستقبلي بإمكانات شبيهة بالجذع نسبياً، مما يوحي بأنها قد تنكمش مؤقتًا لكنها لاحقًا تغذي الانتكاس.
مستويات الأكسجين تميل موازين المقاومة
الأورام الحقيقية غير متجانسة في إمدادها بالأكسجين، ومن المعروف أن الجيوب منخفضة الأكسجين تعزز مقاومة العلاج. باستخدام كلوريد الكوبالت لإثارة استجابة تشبه نقص الأكسجة، وجد الباحثون أن حالة الأكسجين تتفاعل بقوة مع النمط الفرعي. تحت نقص أكسجة محاكى، قلَّت تكاثر الخلايا المستقبلية لكنها زادت النشاط الأيضي، وعند تعرضها للتيموزولوميد في هذه الحالة نجت أفضل وهاجرت أكثر. أما الخلايا الميزنشيمية، فكانت تميل إلى أن تصبح أكثر عرضة للدواء تحت نفس إشارة نقص الأكسجة. عندما رسم الفريق كيفية تأثير نقص الأكسجة على فعالية التيموزولوميد مقابل درجة الشبيهة بالجذع، تقسمت المزارع إلى معسكرين: خلايا شديدة الشبيهة بالجذع وتشبه المستقبلية أصبحت أكثر مقاومة للدواء، وخلايا منخفضة الشبيهة بالجذع وتشبه الميزنشيمية أصبحت أكثر حساسية.
ماذا يعني هذا للمرضى والعلاجات المستقبلية
بالنسبة للقارئ العام، الرسالة الأساسية هي أن ليس كل الأورام الدبقية متشابهة بيولوجيًا، وهذه الاختلافات تهم في كيفية تحمل الأورام وتكيّفها مع العلاج. تبدو الأورام الغنية بالخلايا المستقبلية الشبيهة بالجذع قادرة بشكل خاص على تحمل التيموزولوميد، والتحول نحو حالة أشد تشبه الميزنشيمية مع الحفاظ على نواة من الخلايا المقاومة، لا سيما في ظروف انخفاض الأكسجين. تقترح الدراسة أن CD44 وجزيئات أخرى مرتبطة بحمض الهيالورونيك يُفضّل اعتبارها سمات لهوية الميزنشيمية المتصلبة، لا مجرد علامات للخلايا الجذعية. وعلى الرغم من أن النتائج مبنية على عدد محدود من نماذج الخلايا وغالبًا ما تكون ترابطية، فإن العمل يدعم استخدام مقياس بسيط من مستقبلية إلى ميزنشيمية، مع مقاييس الشبيهة بالجذع، لتصنيف الأورام الدبقية وتصميم علاجات تسبق أو تعطل الخلايا الأكثر تكيفًا والمحرِّكة للانتكاس.
الاستشهاد: Rancati, S., Campolungo, M., Dalmolin, D.G. et al. Molecular subtypes and the (in vitro) response of glioblastoma to temozolomide. BJC Rep 4, 24 (2026). https://doi.org/10.1038/s44276-026-00228-8
الكلمات المفتاحية: الورم الدبقي الخبيث, مقاومة التيموزولوميد, خلايا السرطان الجذعية, نقص الأكسجة في الورم, الأنماط الجزيئية