Clear Sky Science · ja
分子サブタイプとテモゾロミドに対する(in vitro)膠芽腫の応答
この脳腫瘍研究が重要な理由
膠芽腫は成人における最も一般的かつ致死性の高い脳腫瘍であり、現行の標準薬であるテモゾロミドでさえ通常はわずか数か月の延命にとどまります。本研究は患者と臨床医に直接関係する問いを投げかけます:膠芽腫の分子上の「性格」は治療への応答を予測できるか、そしてなぜ一部の腫瘍が非常に速く薬剤耐性を獲得するのか、その理由を説明できるか?
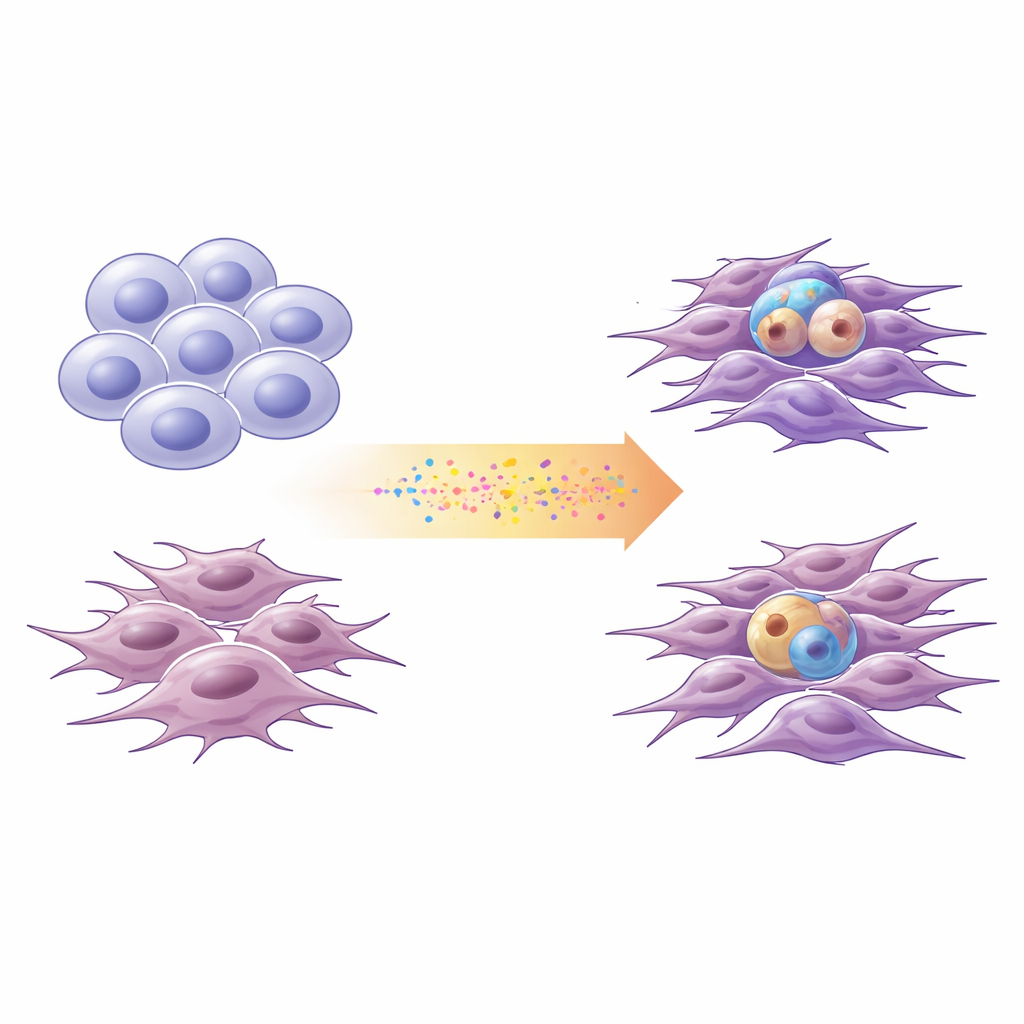
膠芽腫の二つの主要な特徴
研究者たちは膠芽腫細胞を、二つの広い状態の間のスペクトルとして記述することが増えています。「プラウスニューロナル(proneural)」細胞は未熟な神経細胞に似ており、幹様に分裂し多様な子孫を生み出せます。一方「間葉系(mesenchymal)」細胞はよりストレスに強く硬化した生存者のようで、移動性や浸潤性が高く炎症と関連します。研究チームは4人の患者由来の新鮮培養細胞と標準的な細胞株を用い、DNA変化と遺伝子発現を解析して各培養をこのプラウスニューロナル–間葉系軸上に位置づけました。この簡略化した二状態スケールが、大規模な公開膠芽腫データセットで観察される転写の多様性の大部分を捉えていることを確認しました。
幹様の振る舞いとCD44の謎
浮遊する球状体として成長する能力や混合集団を再生する能力など、幹様の特性はしばしば治療抵抗性の原因とされます。著者らは公表された4遺伝子からなる幹性プログラムを定量化し、印象的なパターンを見出しました:スペクトルのプラウスニューロナル側に位置する細胞は一貫して幹性スコアが高く、間葉系細胞は低いスコアを示しました。同時に、表面分子であるCD44(時に幹細胞マーカーと呼ばれる)について再検討しました。彼らの解析では、CD44高発現は間葉系状態と関連し、むしろ幹性は低いという結果が得られ、自分たちの培養系と独立データセットの双方で同様でした。プラウスニューロナル培養から低CD44と高CD44の細胞を物理的に分離すると、低CD44群はより幹様に振る舞い—可塑性が高く元の混合を再生でき—一方高CD44群はより分化し間葉系様に見えました。
腫瘍細胞が周囲とどう対話するか
CD44はヒアルロン酸の受容体として最もよく知られており、ヒアルロン酸は脳の細胞外マトリックスの糖類に富む成分です。研究チームは視野を広げ、ヒアルロン酸結合タンパク質を多く含めて解析しました。間葉系細胞はこのマトリックスに結合して取り込める表面受容体が豊富であるのに対し、プラウスニューロナル細胞は保護的なニッチを形作るマトリックス構成成分を多く作っていることが分かりました。機能的には、テモゾロミドにヒアルロン酸を追加して処理すると、間葉系細胞は移動が遅くなり(表面受容体を積極的に使っていることと一致)、プラウスニューロナル細胞はあまり影響を受けませんでした。これは腫瘍とその微小環境がサブタイプ特異的に互いを強化し得ることを示唆します。
テモゾロミドは細胞をより強靭な状態へ押しやる
研究の核心は、これら異なる細胞状態がテモゾロミドにどう応答するかを扱っています。最初の24時間では、薬剤濃度の増加は間葉系細胞の増殖を抑えましたが、プラウスニューロナル細胞の分裂率にはほとんど影響を与えませんでした。72時間にわたり広い濃度範囲で見ると、古典的な感受性指標(IC50)は単純にサブタイプに従いませんでした。しかし、臨床での反復投与を模倣して—投与、回復、再投与を行うと—プラウスニューロナル培養が際立ちました:一度の曝露後に増殖性は低下するものの、二回目の投与に対して著しく耐性を示すようになったのです。一方、間葉系培養は感受性の変化がほとんどありませんでした。遺伝子発現解析では、ほぼ毒性を示すテモゾロミド濃度が全ての細胞に広範な「間葉系シフト」を駆動することが明らかになりました:炎症や組織改変に関連する経路が上昇し、幹性関連プログラムは低下、特に元がプラウスニューロナルだった細胞で顕著でした。それでもこれらプラウスニューロナル由来細胞は比較的高い幹様ポテンシャルを保持しており、一時的に収縮しても後に再発を駆動することを示唆します。
酸素濃度が耐性のバランスを傾ける
実際の腫瘍は酸素供給が斑であり、低酸素の領域は治療抵抗性を育むことで知られます。コバルト塩化物を用いて低酸素様応答を誘導したところ、酸素状態はサブタイプと強く相互作用しました。低酸素を模した条件下で、プラウスニューロナル細胞は増殖を抑えつつ代謝活性を高め、こうした状態でテモゾロミドに曝されると生存率が上がり移動性も増しました。対照的に間葉系細胞は同じ低酸素シグナルのもとで薬剤に対して脆弱になる傾向がありました。低酸素がテモゾロミドの効力をどのように変えるかを幹性スコアに対してプロットすると、培養は二つの群に分かれました:幹性が高くプラウスニューロナルに類似した細胞は薬剤耐性を高め、幹性が低く間葉系に類似した細胞は感受性を増す、というものです。
患者と将来の治療への含意
一般読者にとっての主要メッセージは、すべての膠芽腫が生物学的に同じではなく、これらの違いが腫瘍が治療に耐え適応する仕方に影響するという点です。プラウスニューロナルで幹様の細胞を多く含む腫瘍は、特に低酸素環境下で、テモゾロミドを耐え抜き間葉系様のより強靭な状態へシフトしつつも、しなやかな細胞のコアを保持して再発を促す能力が高いように見えます。本研究はCD44や他のヒアルロン酸関連分子を、単純な幹細胞マーカーではなくこの硬化した間葉系同一性の目印として見る方が適切だと示唆します。モデル数は限られ関連性は主に相関的ではあるものの、本研究は単純なプラウスニューロナル–間葉系の尺度と幹性指標を用いて膠芽腫を層別化し、最も適応力が高く再発を駆動する細胞を予防・無力化する治療設計を支持する根拠を与えます。
引用: Rancati, S., Campolungo, M., Dalmolin, D.G. et al. Molecular subtypes and the (in vitro) response of glioblastoma to temozolomide. BJC Rep 4, 24 (2026). https://doi.org/10.1038/s44276-026-00228-8
キーワード: 膠芽腫, テモゾロミド耐性, がん幹細胞, 腫瘍低酸素, 分子サブタイプ