Clear Sky Science · ru
Молекулярные подтипы и (in vitro) ответ глиобластомы на темозоломид
Почему это исследование рака мозга важно
Глиобластома — самая распространённая и летальная форма рака мозга у взрослых, и даже стандартный препарат темозоломид обычно даёт лишь дополнительные месяцы жизни. В этом исследовании ставится вопрос, напрямую важный для пациентов и клиницистов: может ли молекулярная «личность» глиобластомы предсказать её ответ на лечение и объяснить, почему некоторые опухоли так быстро становятся резистентными к лекарствам?
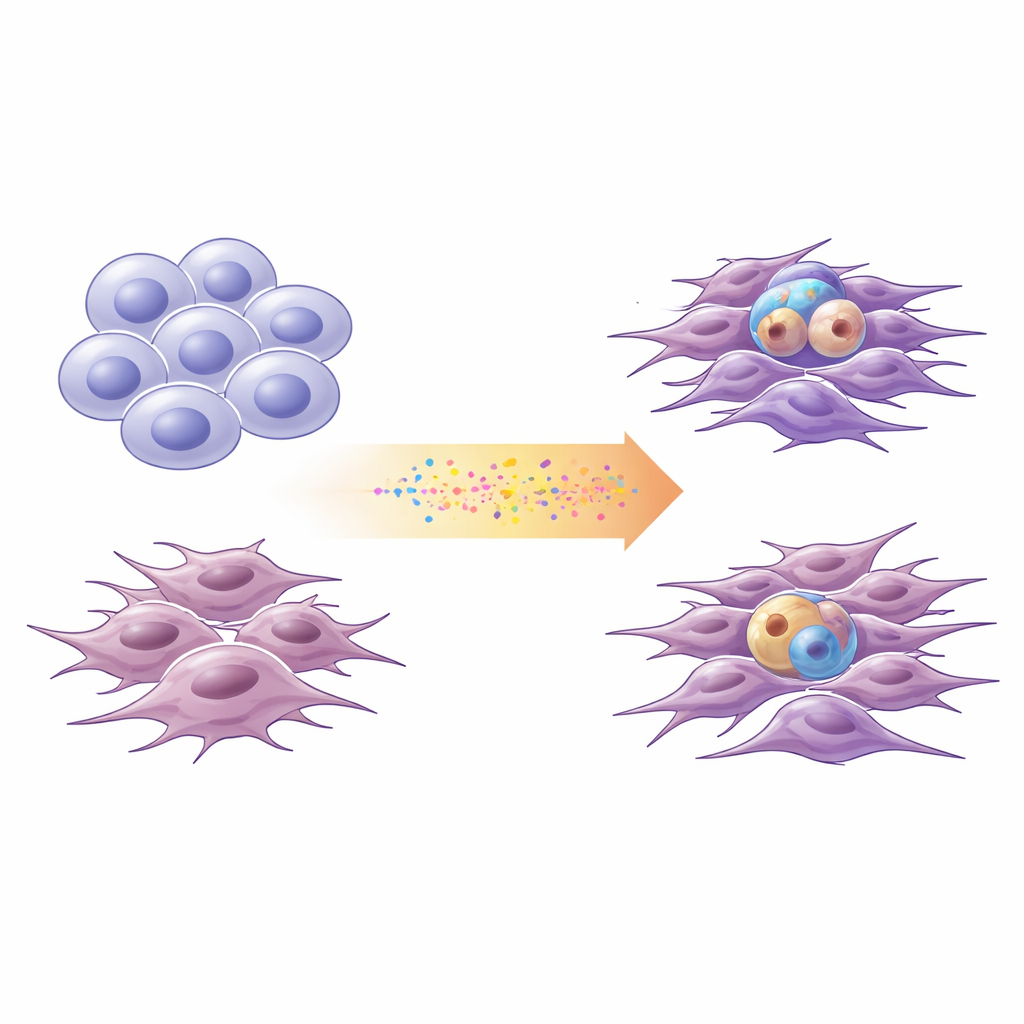
Два основных «вкуса» глиобластомы
Исследователи всё чаще описывают клетки глиобластомы как расположенные на спектре между двумя широкими состояниями. «Праненальные» (proneural) клетки напоминают незрелые нервные клетки: они делятся по‑похожему на стволовые и могут порождать разнообразные потомки. «Мезенхимальные» клетки скорее подобны стрессовым, закалённым выжившим: они более подвижны, инвазивны и связаны с воспалением. Используя клетки, только что полученные от четырёх пациентов, а также стандартную лабораторную линию, команда профилировала изменения ДНК и активность генов, чтобы расположить каждую культуру на оси proneural–mesenchymal. Они подтвердили, что эта упрощённая двухсостоянийная шкала охватывает большую часть транскрипционной разнообразия, наблюдаемого в крупных общедоступных наборах данных по глиобластоме.
Стволоподобное поведение и загадка CD44
Стволоподобные свойства — такие как способность расти в виде свободно плавающих сфероидов и восстанавливать смешанное население клеток — часто обвиняют в терапии‑резистентности. Авторы количественно оценили опубликованную программу «стемнесс» из четырёх генов и обнаружили поразительную закономерность: клетки на proneural‑конце спектра последовательно показывали более высокие показатели стемнесс, тогда как мезенхимальные клетки имели более низкие значения. В то же время они вернулись к спорной поверхностной молекуле CD44, которую иногда называют маркером стволовых клеток. В их руках более высокий уровень CD44 коррелировал с мезенхимальным состоянием и с меньшей стемнесс, а не наоборот, как в их собственных культурах, так и в независимых наборах данных. Когда они физически разделили клетки с низким и высоким CD44 из proneural‑культуры, группа с низким CD44 вела себя больше как стволовые клетки — была более пластичной и могла восстановить исходный состав — тогда как группа с высоким CD44 выглядела более дифференцированной и похожей на мезенхиму.
Как опухолевые клетки «разговаривают» с окружением
CD44 наиболее известен как рецептор для гиалуроновой кислоты, богатого сахарами компонента внеклеточного матрикса мозга. Команда расширила взгляд, включив множество белков, связывающих гиалуроновую кислоту. Они обнаружили, что мезенхимальные клетки обогащены поверхностными рецепторами, которые могут захватывать и поглощать этот матрикс, тогда как proneural‑клетки производят больше компонентов, строящих матрикс и помогающих формировать защитную нишу. Функционально, при комбинировании темозоломида с добавленной гиалуроновой кислотой мезенхимальные клетки замедляли миграцию, что согласуется с их активным использованием поверхностных рецепторов, тогда как proneural‑клетки были менее затронуты. Это указывает на подтип‑специфические способы, которыми опухоль и её микроокружение могут взаимно подкреплять друг друга.
Темозоломид толкает клетки в более жёсткое состояние
Ключевая часть работы касается того, как эти разные клеточные состояния реагируют на темозоломид. В первые 24 часа увеличивающиеся дозы лекарства сдерживали рост мезенхимальных клеток, но практически не влияли на скорость деления proneural‑клеток. На протяжении 72 часов и в широком диапазоне доз общая чувствительность к препарату (классическая мера IC50) не следовала просто за подтипом. Однако когда команда смоделировала повторную клиническую дозировку — лечение, восстановление, затем повторное лечение — proneural‑культуры выделялись: после одного воздействия они становились менее пролиферативными, но заметно более резистентными ко второму раунду, тогда как мезенхимальные культуры почти не меняли чувствительность. Анализ экспрессии генов показал, что близкие к токсическим дозы темозоломида вызывали широкое «мезенхимальное смещение» во всех клетках: возрастали пути, связанные с воспалением и ремоделированием тканей, тогда как программы, ассоциированные со стемнесс, падали, особенно в изначально proneural‑клетках. Тем не менее эти клетки, происходившие из proneural‑состояния, сохраняли относительно высокий стволоподобный потенциал, что намекает на то, что они могут временно сократиться, но затем подпитывать рецидив.
Уровень кислорода смещает баланс резистентности
В реальных опухолях снабжение кислородом бывает неоднородным, и низкооксигенированные участки известны тем, что способствуют устойчивости к лечению. Используя хлорид кобальта для запуска гипоксоподобного ответа, исследователи обнаружили, что состояние кислорода сильно взаимодействует с подтипом. При имитированной гипоксии proneural‑клетки снижали пролиферацию, но увеличивали метаболическую активность, и при воздействии темозоломида в этом состоянии они лучше выживали и сильнее мигрировали. Мезенхимальные клетки, напротив, при той же гипоксической сигнализации, как правило, становились более уязвимыми к препарату. Когда команда нанесла на график, как гипоксия меняет эффективность темозоломида в зависимости от показателя стемнесс, культуры разделились на два лагеря: высокостемнессные, похожие на proneural, которые становились более резистентными, и низкостемнессные, похожие на мезенхиму, которые становились более чувствительными.
Что это значит для пациентов и будущих терапий
Для непрофильного читателя ключевое послание таково: не все глиобластомы биологически одинаковы, и эти различия важны для того, как опухоли переживают и адаптируются к лечению. Опухоли, обогащённые proneural, стволоподобными клетками, особенно способны выдерживать темозоломид, смещаясь в более жёсткое мезенхимальное состояние, при этом сохраняя ядро устойчивых клеток, особенно в условиях сниженного кислорода. Исследование предлагает рассматривать CD44 и другие молекулы, связанные с гиалуроновой кислотой, скорее как маркеры этой закалённой мезенхимальной идентичности, а не как простые флаги стволовых клеток. Несмотря на ограниченное число моделей клеток и в основном корреляционный характер данных, работа поддерживает использование простой шкалы proneural–mesenchymal вместе с показателями стемнесс для стратификации глиобластом и разработки терапий, которые предупреждают или нейтрализуют наиболее адаптивные клетки, ведущие к рецидиву.
Цитирование: Rancati, S., Campolungo, M., Dalmolin, D.G. et al. Molecular subtypes and the (in vitro) response of glioblastoma to temozolomide. BJC Rep 4, 24 (2026). https://doi.org/10.1038/s44276-026-00228-8
Ключевые слова: глиобластома, резистентность к темозоломиду, раковые стволовые клетки, гипоксия опухоли, молекулярные подтипы