Clear Sky Science · tr
Enterobacterales'te plazmid transferini nükleozid analoglarıyla engellemeye yönelik mekanistik bulgular
Neden küçük DNA halkaları bizim için önemli
Antibiyotik direnci genellikle aşırı kullanılan ilaçlar ve inatçı enfeksiyonlarla ilişkilendirilir, fakat bu süperböceklerin yayılmasına yardımcı olan daha az görünür bir aktör daha vardır: bakteriler arasında atlayan küçük DNA halkaları olan plazmidler. Bu çalışma, geniş sonuçları olan pratik bir soruyu gündeme getiriyor: zaten viral enfeksiyonlar için kullandığımız ilaçlar, bağırsak bakterileri arasındaki antibiyotik direnç genlerinin yayılmasını sessizce yavaşlatabilir mi ya da hatta hızlandırabilir mi? Araştırmacılar, antiviral benzeri bazı bileşiklerin iki yaygın hastane patojeninde plazmid transferini nasıl etkilediğini inceleyerek, direncin bakteriyel topluluklar arasında hareket etmesini engellemenin yeni yollarını ortaya koyuyor — aynı zamanda bazı ilaçların kazara sorunu daha da kötüleştirebileceği konusunda uyarıyorlar. 
Direnç genleri nasıl taşınır
Escherichia coli ve Klebsiella pneumoniae içindeki en endişe verici antibiyotik direnç genlerinin birçoğu, kendilerini kopyalayabilen ve konjugasyon adı verilen bir süreçle bir bakteriden diğerine doğrudan geçebilen plazmidlerde bulunur. Bu DNA aktarımı, bakteriler yoğun antibiyotik baskısı altında olmasalar bile direnç genlerinin hastane servislerinde ve insan bağırsağında hızla yayılmasına yardımcı olur. Geleneksel antibiyotikler bakterileri öldürür veya büyümelerini yavaşlatır, ancak bu gen takasını durdurmaz; bu yüzden bilim insanları, bakteriyel büyümeyi büyük ölçüde etkilemeden direnç hatlarını kesmeyi amaçlayan "anti-plazmid" bileşiklerini araştırmaya başladı.
Eski antiviral ilaçlar, yeni roller
Araştırma ekibi, viral veya insan DNA/RNA'sını bozmak üzere tasarlanmış küçük moleküller olan 14 klinik olarak onaylı nükleozid analogunu, plazmidlerin bakteriler arasındaki hareket sıklığını değiştirip değiştirmediğini görmek için test etti. Floresan etiketler ve akış sitometrisi kullanarak, E. coli'de geniş spektrumlu β-laktamaz (birçok penisilin benzeri ilacı parçalayan) genlerini taşıyan bir plazmidin ve K. pneumoniae'de bir karbapenemaz genini taşıyan başka bir plazmidin transferini izlediler. Azidotimidin (AZT), didanosin, stavudin ve trifluoridin dahil olmak üzere birkaç bileşik, bakteriyel büyümeyi yavaşlatmadan plazmid transferini belirgin şekilde azalttı. İlginç biçimde, famsiklovir, zalsitabin, asiklovir ve valasiklovir gibi diğer nükleozid analogları ise test edilen en az bir türde plazmid paylaşımını artırdı. Bu, viral enfeksiyonlar için verilen bazı ilaçların prensipte direnç genlerinin bağırsak mikrobiyomunda daha kolay yayılmasını teşvik edebileceği anlamına geliyor.
Bakteri hücresi içinde neler değişiyor
Bu bileşiklerin nasıl çalıştığını anlamak için araştırmacılar bakteriyel fizyolojinin birkaç temel özelliğine baktılar. İlaçların çoğu hücre zarlarına zarar vermiyor, elektriksel potansiyeli bozmadı veya reaktif oksijen patlamalarına yol açmadı ve genel büyümeyi etkilemedi. Plazmidi teşvik eden bazı bileşikler ATP seviyelerini ılımlı şekilde düşürdü; bu da enerji dengesi ile plazmid transfer makinesinin çalıştırılmasının maliyeti arasında bir bağ olabileceğine işaret ediyor. En güçlü inhibitör olan AZT için ekip RNA dizilemeye yöneldi; bu yöntem bakteriler ilaca maruz kaldığında hangi genlerin yukarıya veya aşağıya doğru değiştiğini gösteriyor. 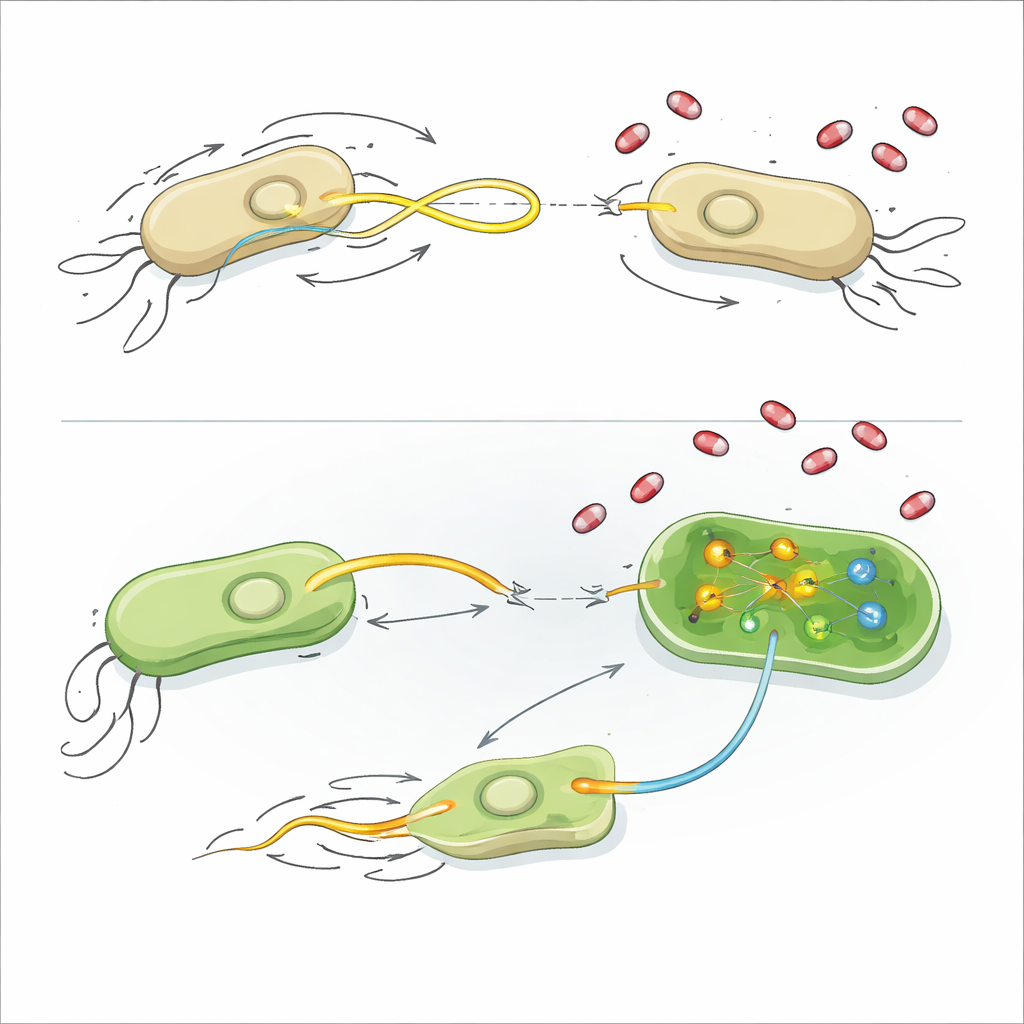
Yüzmeyi yavaşlatma ve onarımı engelleme
E. coli'de AZT, hücrelerin yüzmesini sağlayan dönen kuyruk olan flagellum'u inşa eden ve kontrol eden genleri keskin şekilde bastırdı. Araştırmacılar E. coli'yi yumuşak agar üzerine yerleştirdiklerinde, AZT onların dışa doğru yayılmasını neredeyse tamamen durdurdu; üstelik bakteriler öldürülmüyordu. Anahtar bir flagellar bileşeni genetik olarak devre dışı bırakıldığında plazmid transferinde benzer bir azalma görüldü ve buna AZT eklendiğinde daha fazla düşüş olmadı — bu da azaltılmış hareketliliğin inhibisyonun büyük bir kısmını açıklayabileceğine dair güçlü kanıt sunuyor. K. pneumoniae'de AZT farklı bir yol izledi: DNA hasar onarımıyla ilişkili genleri, merkezi bir SOS yanıt proteini olan RecA dahil olmak üzere açtı ve metiyonin ile onun türevi S-adenosilmetiyonin (SAM) yapımı için gereken genleri kapattı; SAM evrensel bir metil vericisidir. RecA aktivitesini düşüren çinko asetat eklenmesi veya ekstra SAM sağlanması, AZT varlığında plazmid transferini geri getirdi; bu da artmış DNA stresi ve bozulmuş metilasyonun gelen plazmidleri bloke etmeye yardımcı olduğunu gösteriyor.
Dirençle mücadele için bunun anlamı
Bu çalışma, bazı mevcut nükleozid analoglarının bakterileri doğrudan öldürmek yerine direncin yayılmasını etkisiz hale getiren yeni bir ilaç türü için şablon görevi görebileceğini gösteriyor. Özellikle AZT, iki önemli patojende farklı kollar aracılığıyla plazmid konjugasyonunu azaltıyor — bir durumda bakteriyel yüzmeyi durduruyor, diğerinde DNA onarımı ve temel metabolizmayı yeniden şekillendiriyor. Aynı zamanda diğer analogların plazmid transferini artırdığının keşfi, antibiyotik olmayan ilaçların bağırsak mikrobunun gen trafiği üzerinde nasıl etkiler yaptığına dair anlayışın geliştirilmesi gerektiğini vurguluyor. Sonuçta, iyi ayarlanmış plazmid transfer inhibitörleri, antimikrobiyal direncin ilerleyişini yavaşlatmak için araç setimizin bir parçası olabilir ve mevcut antibiyotiklerin ve yeni tedavilerin işe yaraması için zaman kazandırabilir.
Atıf: Alav, I., Ashraf, A., Pordelkhaki, P. et al. Mechanistic insights into plasmid transfer inhibition in Enterobacterales by nucleoside analogues. npj Antimicrob Resist 4, 23 (2026). https://doi.org/10.1038/s44259-026-00197-5
Anahtar kelimeler: antimikrobiyal direnç, plazmid transferi, nükleozid analogları, Escherichia coli, Klebsiella pneumoniae