Clear Sky Science · he
תובנות מכנית על עיכוב העברת פלסמידים ב-Enterobacterales על ידי אנלוגים של נוקלאוזידים
מדוע טבעות DNA קטנות חשובות לנו
עמידות לאנטיביוטיקה אמנם מעוררת בראש ובראשונה אסוציאציות של שימוש יתר בתרופות וזיהומים עקשניים, אך שחקן פחות גלוי מסייע להתפשטות הסופרבקטריות: טבעות DNA קטנות הנקראות פלסמידים שקופצות בין חיידקים. המחקר הזה שואל שאלה מעשית עם השלכות רחבות: האם תרופות שאנו כבר משתמשים בהן לטיפול בזיהומים ויראליים עשויות, בשקט, להאט — או אפילו להאיץ — את התפשטות הגנים לעמידות לאנטיביוטיקה בין חיידקי המעי? באמצעות בדיקה כיצד תרכובות דמו-אנטי-ויראליות משפיעות על העברת פלסמידים בשני פתוגנים נפוצים בבתי חולים, החוקרים מצביעים על דרכים חדשות לחסום את התפשטות העמידות בקהילות חיידקיות — ובאותו זמן מזהירים שכמה תרופות עלולות בטעות להחמיר את הבעיה. 
כיצד גנים לעמידות נוהגים על רכבת
רבים מהגנים המסוכנים ביותר לעמידות לאנטיביוטיקה ב-Escherichia coli וב-Klebsiella pneumoniae יושבים על פלסמידים, שיכולים לשכפל עצמם ולעבור ישירות מחיידק אחד לאחר בתהליך שנקרא קוניוגציה. העברת ה-DNA הזו מאפשרת לעמידות להתפשט במהירות במחלקות בתי חולים ובמיקרוביוטה של המעי, גם כאשר החיידקים אינם נתונים ללחץ אנטיביוטי כבד. מכיוון שאנטיביוטיקה מסורתית הורגת או מאטה חיידקים אך אינה עוצרת את החלפת הגנים הזו, מדענים החלו לחפש תרכובות "נגד-פלסמיד" שמשאירות את צמיחת החיידקים כמעט ללא שינוי אך חותכות את קווי ההעברה שבאמצעותם נעים הגנים לעמידות.
תרופות אנטי-וירליות ישנות, תפקידים חדשים
הצוות בדק 14 אנלוגים של נוקלאוזידים שאושרו לשימוש קליני — מולקולות קטנות שתוכננו במקור להפריע ל-DNA ול-RNA ויראליים או אנושיים — כדי לראות האם הן משנות את תדירות מעבר הפלסמידים בין חיידקים. באמצעות תגיות זרחניות וציטומטריה של זרימה, הם עקבו אחרי העברת פלסמיד אחד הנושא גנים ל-β-לקטמאזות לטווח מורחב (שבורות תרופות רבות ממשפחת הפניצילינים) ב-E. coli, ופלסמיד אחר הנושא גן קרבפנמאז ב-K. pneumoniae. כמה תרכובות, כולל אזידותימידין (AZT), דידנוזין, סטבודין וטריפלורידין, הפחיתו באופן ברור את העברת הפלסמידים מבלי להאט את צמיחת החיידקים. באופן מפתיע, אנלוגים אחרים כמו פמקיציקלוביר, זלסיטבין, אקיקלוביר וולאציקלוביר הגבירו בפועל את שיתוף הפלסמידים לפחות באחד מהמינים שנבדקו. משמעות הדבר היא שחלק מהתרופות הניתנות לזיהומים ויראליים עלולות, עקרונית, לדחוף את הפצת גני העמידות להתקדם ביתר קלות במיקרוביוטת המעי.
מה משתנה בתוך התא החיידקי
כדי להבין כיצד התרכובות הללו פועלות, החוקרים בחנו כמה תכונות בסיסיות של פיזיולוגיה חיידקית. רוב התרופות לא גרמו נזק לממברנות התאים, לא הפריעו בפוטנציאל החשמלי ולא עוררו התפרצויות של חמצון ריאקטיבי, והן השאירו את הצמיחה הכוללת ללא שינוי. חלק מהתרכובות המזינות העברת פלסמידים הורידו במידה מתונה את רמות ה-ATP, המטבע האנרגטי העיקרי של התא, ומרמזות כי מאזן האנרגיה ועלות הפעלת המכשור להעברת הפלסמיד עשויים להיות מקושרים. עבור המדכא החזק ביותר, AZT, הצוות פנה לריצוף RNA, שמראה אילו גנים מוארים או מדוכאים כאשר החיידקים נחשפים לתרופה. 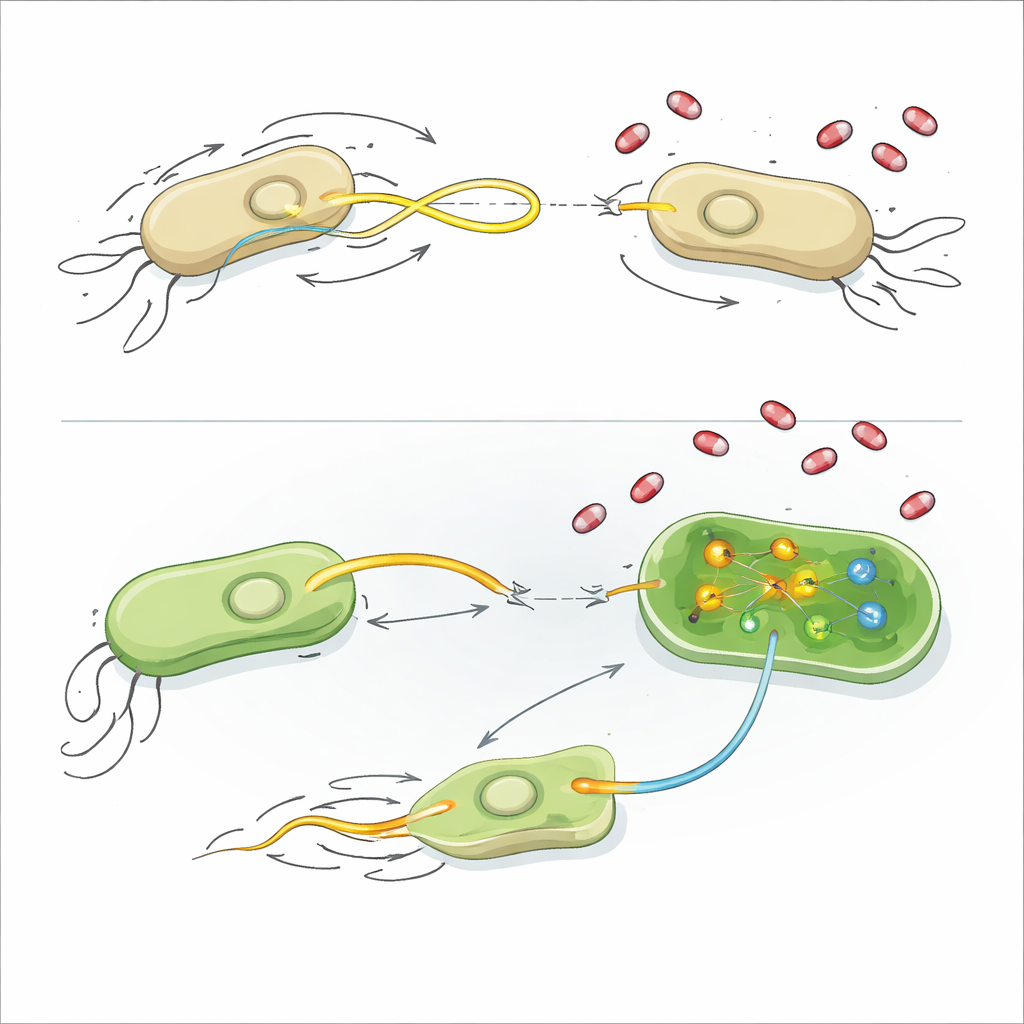
האטת הכנפים וחסימת התיקון
ב-E. coli, AZT דיכא בצורה חדה גנים הבונים ושולטים במבנה השוטון (flagellum), הזנב המסתובב שמאפשר לתאים לשחות. כששם החוקרים את ה-E. coli על אגאר רך, AZT כמעט עצר אותם מפני התפשטות כלפי חוץ, אף על פי שהחיידקים לא נרצחו. ניתוק גנטי של רכיב מפתח בשוטון גרם לאפקט דומה בחיתוך העברת הפלסמידים, והוספת AZT בנוסף לכך לא גרמה לירידה נוספת — עדות חזקה לכך שהפחתת הניידות לבדה יכולה להסביר חלק גדול מהעיכוב. ב-K. pneumoniae, AZT לקח דרך שונה: הוא הופעל גנים המעורבים בתיקון נזקי DNA, כולל חלבון מרכזי בתגובת ה-SOS שנקרא RecA, וכיבה גנים הדרושים לסינתזת חומצת האמינו מתיונין ונגזרתיה S-adenosylmethionine (SAM), תורם מתיל אוניברסלי. הוספת אצטט אבץ, הממתן פעילות של RecA, או אספקת SAM נוספת שיקמה את העברת הפלסמיד בנוכחות AZT, דבר שמעיד על כך שמתח DNA מוגבר והפרעה במתילציה מסייעים לחסום פלסמידים נכנסים.
מה זה אומר למאבק בעמידות
המחקר מראה כי כמה אנלוגים של נוקלאוזידים קיימים יכולים לשמש כתבנית לסוג חדש של תרופות: סוכנים המנטרלים את הפצת העמידות במקום להרוג חיידקים ישירות. AZT, בפרט, מקטין קוניוגציה של פלסמידים בשני פתוגנים עיקריים באמצעות מנופים שונים — עצירת יכולת השחייה בחיידק אחד ועיצוב מחדש של תיקון ה-DNA והמטבוליזם הבסיסי בחיידק האחר. יחד עם זאת, הגילוי שאנלוגים אחרים מגדילים את העברת הפלסמיד מדגיש את הצורך להבין כיצד תרופות שאינן אנטיביוטיות משפיעות על תנועת הגנים במיקרוביוטת המעי. בסופו של דבר, מעכבי העברת פלסמיד מדויקים עלולים להיכנס לערכת הכלים שלנו כדי להאט את צעד העמידות האנטימיקרוביאלית, ולקנות זמן לאנטיביוטיקות הקיימות ולתרופות חדשות לפעול.
ציטוט: Alav, I., Ashraf, A., Pordelkhaki, P. et al. Mechanistic insights into plasmid transfer inhibition in Enterobacterales by nucleoside analogues. npj Antimicrob Resist 4, 23 (2026). https://doi.org/10.1038/s44259-026-00197-5
מילות מפתח: התמחות אנטימיקרוביאלית, העברת פלסמידים, אנלוגים של נוקלאוזידים, Escherichia coli, Klebsiella pneumoniae