Clear Sky Science · nl
Mechanistische inzichten in de remming van plasmidoverdracht in Enterobacterales door nucleoside‑analogen
Waarom kleine DNA‑ringetjes voor ons belangrijk zijn
Antibioticaresistentie roept vaak beelden op van overgebruikte medicijnen en hardnekkige infecties, maar er is een ander, minder zichtbaar mechanisme dat deze superbacteriën helpt verspreiden: kleine DNA‑ringetjes genaamd plasmiden die tussen bacteriën springen. Deze studie onderzoekt een praktisch maar ingrijpend vraagstuk: kunnen medicijnen die we al tegen virussen gebruiken stilletjes de verspreiding van resistentiegenen tussen darmbacteriën vertragen — of zelfs versnellen? Door te onderzoeken hoe bepaalde antiviraal‑achtige verbindingen plasmidoverdracht beïnvloeden in twee veelvoorkomende ziekenhuispathogenen, onthullen de onderzoekers nieuwe manieren om resistentie te blokkeren binnen bacteriële gemeenschappen — en waarschuwen ze ook dat sommige middelen het probleem onbedoeld kunnen verergeren. 
Hoe resistentiegenen meeliften
Veel van de zorgwekkendste resistentiegenen in Escherichia coli en Klebsiella pneumoniae bevinden zich op plasmiden, die zichzelf kunnen kopiëren en rechtstreeks van de ene bacterie naar de andere kunnen overgaan via een proces dat conjugatie heet. Deze DNA‑overdracht helpt resistentie zich razendsnel te verspreiden door ziekenhuiskamers en de menselijke darm, zelfs wanneer bacteriën niet zwaar aan antibiotica worden blootgesteld. Omdat traditionele antibiotica bacteriën doden of hun groei remmen maar deze genenuitwisseling niet tegenhouden, richten wetenschappers zich op zogeheten “anti‑plasmide” verbindingen die de bacteriële groei grotendeels ongemoeid laten terwijl ze de lijnen doorsnijden waarlangs resistentie reist.
Oude antivirale geneesmiddelen, nieuwe rollen
Het team testte 14 klinisch goedgekeurde nucleoside‑analogen — kleine moleculen oorspronkelijk ontworpen om viraal of humaan DNA en RNA te verstoren — om te zien of ze de frequentie van plasmidoverdracht tussen bacteriën veranderden. Met fluorescente labels en flowcytometrie volgden ze de overdracht van een plasmide dat genen draagt voor extended‑spectrum β‑lactamase (dat veel penicillineachtige middelen afbreekt) in E. coli, en een ander plasmide dat een carbapenemasegen draagt in K. pneumoniae. Verschillende verbindingen, waaronder azidothymidine (AZT), didanosine, stavudine en trifluridine, verminderden duidelijk de plasmidoverdracht zonder de bacteriële groei te vertragen. Verrassend genoeg verhoogden andere nucleoside‑analogen, zoals famciclovir, zalcitabine, aciclovir en valaciclovir, de plasmidendeling juist bij ten minste één van de onderzochte soorten. Dat betekent dat sommige middelen die voor virusinfecties worden voorgeschreven in principe resistentiegenen in het darmmicrobioom kunnen stimuleren om zich gemakkelijker te verspreiden.
Wat er binnenin de bacterie verandert
Om te begrijpen hoe deze verbindingen werken, onderzochten de onderzoekers verschillende basisaspecten van bacteriële fysiologie. De meeste middelen beschadigden de celmembranen niet, verstoorden de elektrische potentiaal niet, veroorzaakten geen uitbarstingen van reactieve zuurstofsoorten en lieten de algehele groei onaangetast. Sommige plasmidebevorderende verbindingen verlaagden in geringe mate het ATP‑niveau, de belangrijkste energievaluta van de cel, wat suggereert dat energiebalans en de kosten van het laten werken van de plasmidoverdrachtmachinerie gekoppeld kunnen zijn. Voor de sterkste remmer, AZT, voerde het team RNA‑sequencing uit om te zien welke genen omhoog of omlaag werden gereguleerd wanneer bacteriën met het middel in aanraking kwamen. 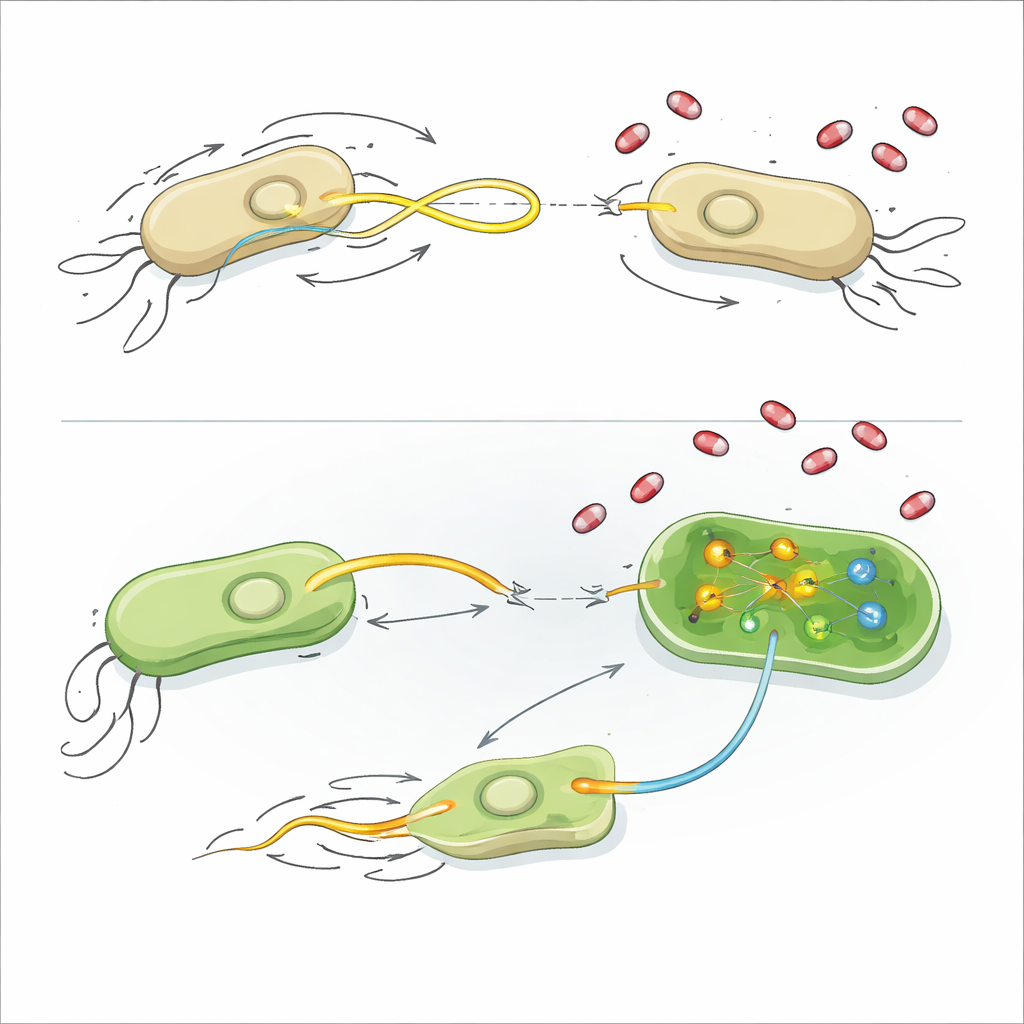
Langzamer zwemmen en blokkeren van herstel
In E. coli zette AZT genen die de flagel opbouwen en reguleren sterk omlaag — de roterende staart waardoor cellen kunnen zwemmen. Wanneer onderzoekers E. coli op zacht agar plaatsten, stopte AZT hun uitwaaiering bijna volledig, hoewel de bacteriën niet werden gedood. Het genetisch uitschakelen van een belangrijk flagelonderdeel had een vergelijkbaar effect op het verminderen van plasmidoverdracht, en het toevoegen van AZT bovenop die mutatie veroorzaakte geen verdere daling — sterk bewijs dat verminderde beweeglijkheid op zichzelf een groot deel van de remming kan verklaren. In K. pneumoniae werkte AZT via een andere route: het schakelde genen in die betrokken zijn bij DNA‑schadeherstel, waaronder een centraal SOS‑responsproteïne genaamd RecA, en schakelde genen uit die nodig zijn voor de aanmaak van het aminozuur methionine en zijn afgeleide S‑adenosylmethionine (SAM), een universele methyldonor. Het toevoegen van acetaatzink, dat RecA‑activiteit dempt, of het aanvullen met extra SAM bracht de plasmidoverdracht in aanwezigheid van AZT beide weer terug, wat erop wijst dat verhoogde DNA‑stress en verstoorde methylatie helpen om binnenkomende plasmiden te blokkeren.
Wat dit betekent voor de strijd tegen resistentie
Dit werk toont aan dat sommige bestaande nucleoside‑analogen als sjablonen kunnen dienen voor een nieuw soort geneesmiddel: middelen die de verspreiding van resistentie ontmantelen in plaats van bacteriën rechtstreeks te doden. AZT beperkt in het bijzonder plasmideconjugatie in twee belangrijke pathogenen via verschillende mechanismen — het remt bacterieel zwemmen in het ene geval en herstructureert DNA‑herstel en basaal metabolisme in het andere. Tegelijkertijd benadrukt de ontdekking dat andere analogen plasmidoverdracht kunnen vergroten de noodzaak om te begrijpen hoe niet‑antibiotische geneesmiddelen het genverkeer in het darmmicrobioom beïnvloeden. Uiteindelijk zouden fijn afgestelde remmers van plasmidoverdracht deel kunnen uitmaken van onze gereedschapskist om de opmars van antimicrobiële resistentie te vertragen, en zo tijd te winnen voor bestaande antibiotica en nieuwe behandelingen.
Bronvermelding: Alav, I., Ashraf, A., Pordelkhaki, P. et al. Mechanistic insights into plasmid transfer inhibition in Enterobacterales by nucleoside analogues. npj Antimicrob Resist 4, 23 (2026). https://doi.org/10.1038/s44259-026-00197-5
Trefwoorden: antimicrobiële resistentie, plasmidoverdracht, nucleoside‑analogen, Escherichia coli, Klebsiella pneumoniae