Clear Sky Science · de
Mechanistische Einblicke in die Hemmung der Plasmidübertragung bei Enterobacterales durch Nukleosidanaloga
Warum winzige DNA-Ringe für uns wichtig sind
Antibiotikaresistenzen wecken meist Assoziationen an übermäßigen Antibiotikagebrauch und hartnäckige Infektionen, aber ein anderer, weniger sichtbarer Faktor fördert die Verbreitung dieser Superkeime: kleine DNA-Ringe namens Plasmide, die zwischen Bakterien springen. Diese Studie stellt eine praktische Frage mit weitreichenden Folgen: Können Arzneimittel, die wir bereits gegen Virusinfektionen einsetzen, unbemerkt die Ausbreitung von Antibiotikaresistenzgenen im Darm verlangsamen oder sogar beschleunigen? Durch die Untersuchung, wie bestimmte antiviralenähnliche Verbindungen die Plasmidübertragung in zwei häufigen Krankenhauspathogenen beeinflussen, decken die Forschenden neue Wege auf, die Ausbreitung von Resistenzen innerhalb bakterieller Gemeinschaften zu blockieren — und warnen zugleich, dass einige Medikamente das Problem ungewollt verschärfen könnten. 
Wie Resistenzgene mitreisen
Viele der besorgniserregendsten Antibiotikaresistenzgene in Escherichia coli und Klebsiella pneumoniae sitzen auf Plasmiden, die sich selbst kopieren und durch einen Prozess namens Konjugation direkt von einem Bakterium auf ein anderes übertragen werden können. Dieser DNA‑Transfer lässt Resistenzen durch Krankenhausstationen und den menschlichen Darm rasen, selbst wenn die Bakterien nicht starkem Antibiotikadruck ausgesetzt sind. Da herkömmliche Antibiotika Bakterien abtöten oder verlangsamen, aber diesen Genaustausch nicht stoppen, suchen Wissenschaftler nach „Anti‑Plasmid“-Verbindungen, die das bakterielle Wachstum weitgehend intakt lassen und zugleich die Kanäle kappen, über die sich Resistenzen ausbreiten.
Alte antivirale Mittel, neue Rollen
Das Team testete 14 klinisch zugelassene Nukleosidanaloga — kleine Moleküle, die ursprünglich entwickelt wurden, um virale oder menschliche DNA und RNA zu stören — um herauszufinden, ob sie die Häufigkeit der Plasmidübertragung zwischen Bakterien verändern. Mithilfe fluoreszenter Markierungen und Durchflusszytometrie verfolgten sie die Übertragung eines Plasmids, das Gene für Extended‑Spectrum‑β‑Lactamase trägt (welche viele penicillinähnliche Wirkstoffe spalten) in E. coli, und eines anderen Plasmids mit einem Carbapenemase‑Gen in K. pneumoniae. Mehrere Verbindungen, darunter Azidothymidin (AZT), Didanosin, Stavudin und Trifluridin, reduzierten die Plasmidübertragung deutlich, ohne das Bakterienwachstum zu bremsen. Überraschenderweise förderten andere Nukleosidanaloga wie Famciclovir, Zalcitabine, Aciclovir und Valaciclovir die Plasmidweitergabe in mindestens einer der getesteten Spezies. Das bedeutet, dass einige für Virusinfektionen eingesetzte Medikamente theoretisch die Verbreitung von Resistenzgenen im Darmmikrobiom erleichtern könnten.
Was sich im Inneren der Bakterienzelle ändert
Um zu verstehen, wie diese Verbindungen wirken, untersuchten die Forschenden mehrere grundlegende Merkmale der bakteriellen Physiologie. Die meisten Wirkstoffe beschädigten nicht die Zellmembranen, störten das elektrische Potential oder lösten keine reaktiven Sauerstoff‑Explosionen aus, und sie veränderten das Gesamtwachstum nicht. Einige der plasmidfördernden Verbindungen senkten leicht die ATP‑Spiegel, die wichtigste Energieeinheit der Zelle, was darauf hindeutet, dass Energiehaushalt und die Kosten für den Betrieb der Plasmidübertragungsmaschinerie verbunden sein könnten. Für den stärksten Inhibitor, AZT, griff das Team zu RNA‑Sequenzierung, die zeigt, welche Gene bei Begegnung mit dem Wirkstoff hoch- oder heruntergeregelt werden. 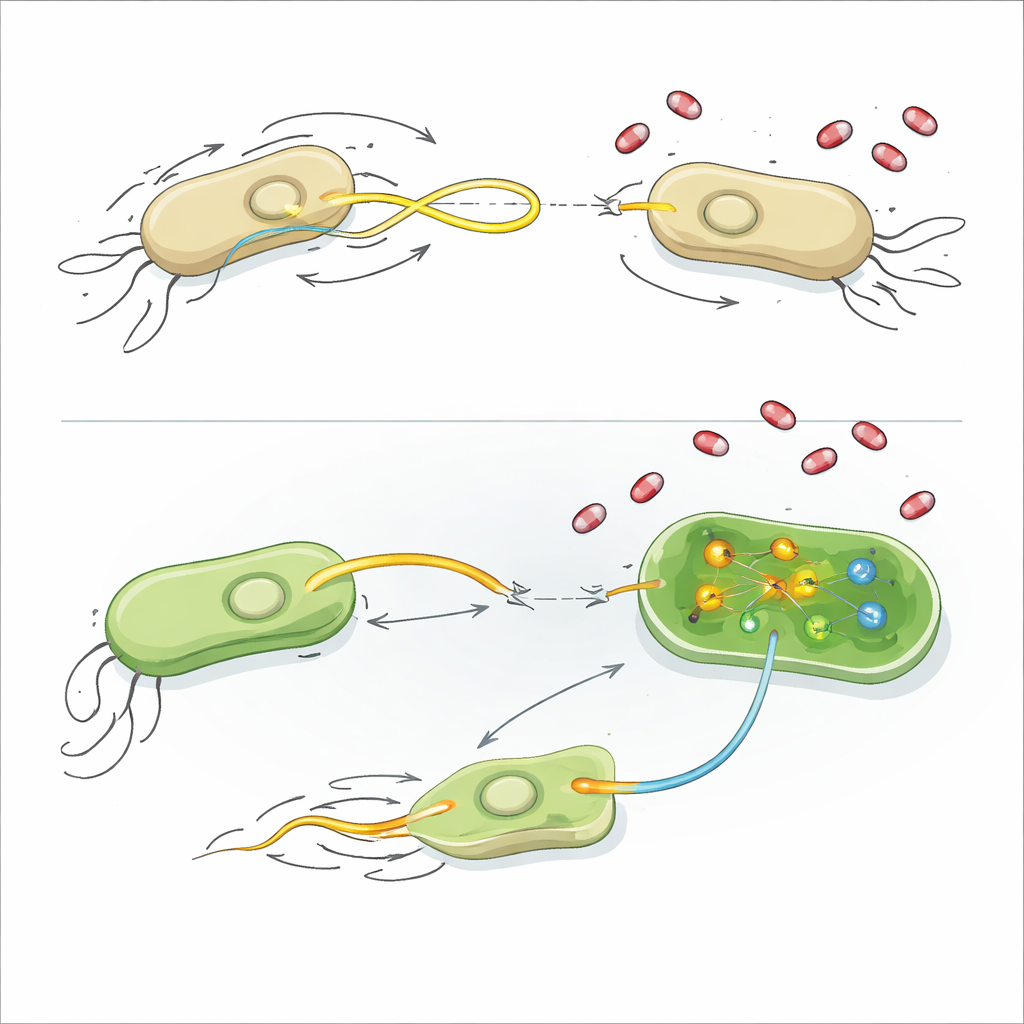
Bewegung drosseln und Reparatur blockieren
Bei E. coli drosselte AZT stark die Gene, die den Flagellumaufbau und dessen Kontrolle steuern — der rotierende Schwanz, mit dem Zellen schwimmen. Auf weichem Agar setzten die Forschenden E. coli aus und AZT verhinderte nahezu vollständig deren Fortbewegung nach außen, obwohl die Bakterien nicht getötet wurden. Das genetische Ausschalten eines zentralen Flagellenbausteins hatte einen ähnlichen Effekt auf die Verringerung der Plasmidübertragung, und die zusätzliche Gabe von AZT führte zu keinem weiteren Rückgang — ein starkes Indiz dafür, dass reduzierte Motilität allein einen Großteil der Hemmung erklären kann. Bei K. pneumoniae schlug AZT einen anderen Weg ein: Es schaltete Gene ein, die an der DNA‑Schadensreparatur beteiligt sind, einschließlich eines zentralen SOS‑Antwortproteins namens RecA, und schaltete Gene aus, die für die Herstellung der Aminosäure Methionin und ihres Derivats S‑Adenosylmethionin (SAM), eines universellen Methylgrenzdonors, benötigt werden. Die Zugabe von Zinkacetat, das die RecA‑Aktivität dämpft, oder die Versorgung mit zusätzlichem SAM stellte die Plasmidübertragung in Gegenwart von AZT wieder her, was darauf hinweist, dass erhöhte DNA‑Stressantworten und gestörte Methylierungswege das Eindringen von Plasmiden blockieren helfen.
Was das für den Kampf gegen Resistenzen bedeutet
Die Arbeit zeigt, dass einige bereits existierende Nukleosidanaloga als Vorbild für eine neue Wirkstoffklasse dienen können: Agenzien, die die Verbreitung von Resistenzen entwaffnen, statt Bakterien direkt abzutöten. Insbesondere AZT bremst die Plasmidkonjugation in zwei wichtigen Krankheitserregern über unterschiedliche Mechanismen — in einem Fall durch Stoppen der bakteriellen Bewegung, im anderen durch Umgestaltung von DNA‑Reparatur und Grundstoffwechsel. Zugleich unterstreicht die Entdeckung, dass andere Analoga die Plasmidübertragung erhöhen, wie wichtig es ist, zu verstehen, wie nicht‑antibiotische Arzneimittel den genetischen Verkehr im Darmmikrobiom beeinflussen. Letztlich könnten fein abgestimmte Inhibitoren der Plasmidübertragung Teil unseres Instrumentariums werden, um den Vormarsch der antimikrobiellen Resistenz zu verlangsamen und Zeit für bestehende Antibiotika und neue Therapien zu gewinnen.
Zitation: Alav, I., Ashraf, A., Pordelkhaki, P. et al. Mechanistic insights into plasmid transfer inhibition in Enterobacterales by nucleoside analogues. npj Antimicrob Resist 4, 23 (2026). https://doi.org/10.1038/s44259-026-00197-5
Schlüsselwörter: antimikrobielle Resistenz, Plasmidübertragung, Nukleosidanaloga, Escherichia coli, Klebsiella pneumoniae