Clear Sky Science · fr
Perspectives mécanistiques sur l’inhibition du transfert de plasmides chez les Enterobacterales par des analogues nucléosidiques
Pourquoi de petits anneaux d’ADN nous concernent
La résistance aux antibiotiques évoque généralement des médicaments surutilisés et des infections tenaces, mais un acteur moins visible facilite la propagation de ces super‑bactéries : de petits anneaux d’ADN appelés plasmides qui sautent d’une bactérie à l’autre. Cette étude pose une question pratique aux implications majeures : des médicaments que nous utilisons déjà contre des infections virales peuvent‑ils discrètement ralentir, ou au contraire accélérer, la diffusion des gènes de résistance entre bactéries intestinales ? En examinant comment certains composés de type antiviraux affectent le transfert de plasmides dans deux agents pathogènes courants en milieu hospitalier, les auteurs mettent au jour de nouvelles façons de bloquer la propagation de la résistance — et alertent aussi sur le fait que certains médicaments pourraient involontairement aggraver le problème. 
Comment les gènes de résistance se déplacent
Beaucoup des gènes de résistance les plus préoccupants chez Escherichia coli et Klebsiella pneumoniae se trouvent sur des plasmides, qui peuvent se répliquer et se transmettre directement d’une bactérie à l’autre par un processus appelé conjugaison. Ce transfert d’ADN permet à la résistance de se répandre rapidement dans les services hospitaliers et dans l’intestin humain, même lorsque les bactéries ne sont pas soumises à une forte pression antibiotique. Parce que les antibiotiques traditionnels tuent ou freinent les bactéries mais n’empêchent pas cet échange de gènes, les scientifiques recherchent des composés « anti‑plasmides » qui laissent la croissance bactérienne globalement intacte tout en coupant les voies par lesquelles la résistance circule.
Des anciens antiviraux, de nouveaux rôles
L’équipe a testé 14 analogues nucléosidiques approuvés cliniquement — de petites molécules conçues à l’origine pour perturber l’ADN et l’ARN viraux ou humains — afin de voir si elles modifiaient la fréquence de transfert des plasmides entre bactéries. En utilisant des marqueurs fluorescents et la cytométrie en flux, ils ont suivi le transfert d’un plasmide portant des gènes codant une β‑lactamase à spectre étendu (qui dégrade de nombreux antibiotiques apparentés à la pénicilline) dans E. coli, et d’un autre plasmide portant un gène de carbapénèmase dans K. pneumoniae. Plusieurs composés, dont l’azidothymidine (AZT), la didanosine, la stavudine et la trifluridine, ont clairement réduit le transfert de plasmides sans ralentir la croissance bactérienne. De façon surprenante, d’autres analogues nucléosidiques, tels que la famciclovir, la zalcitabine, l’aciclovir et la valaciclovir, ont en fait favorisé le partage de plasmides au moins chez l’une des espèces testées. Cela signifie que certains médicaments administrés pour des infections virales pourraient, en principe, faciliter la propagation des gènes de résistance dans le microbiote intestinal.
Ce qui change à l’intérieur de la cellule bactérienne
Pour comprendre le mode d’action de ces composés, les chercheurs ont examiné plusieurs caractéristiques fondamentales de la physiologie bactérienne. La plupart des médicaments n’endommageaient pas les membranes cellulaires, ne perturbaient pas le potentiel électrique, n’entraînaient pas de pics de radicaux réactifs et ne modifiaient pas la croissance globale. Certains des composés favorisant les plasmides réduisaient modestement les niveaux d’ATP, principale monnaie énergétique de la cellule, ce qui laisse penser que l’équilibre énergétique et le coût d’utilisation de la machinerie de transfert des plasmides sont liés. Pour l’inhibiteur le plus puissant, l’AZT, l’équipe a eu recours au séquençage de l’ARN, qui révèle quels gènes sont augmentés ou diminués lorsque les bactéries rencontrent le médicament. 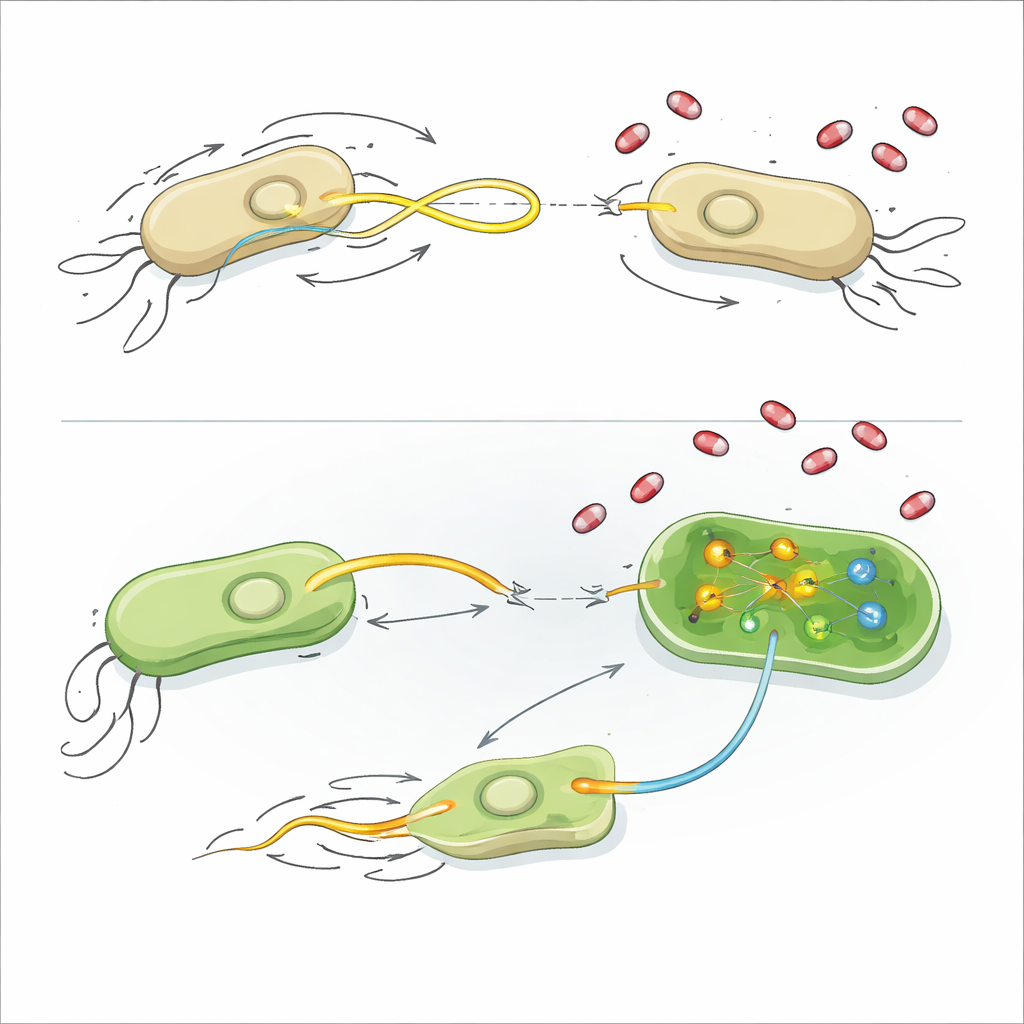
Ralentir la nage et bloquer la réparation
Chez E. coli, l’AZT a fortement diminué l’expression des gènes impliqués dans la construction et le contrôle du flagelle, la queue rotative qui permet aux cellules de nager. Quand les chercheurs ont placé E. coli sur un agar mou, l’AZT a presque entièrement empêché leur diffusion vers l’extérieur, bien que les bactéries n’aient pas été tuées. L’inactivation génétique d’un composant clé du flagelle produisait un effet similaire sur la réduction du transfert de plasmides, et l’ajout d’AZT en plus de cette mutation n’a pas entraîné de baisse supplémentaire — preuve solide que la diminution de la motilité explique à elle seule une grande partie de l’inhibition. Chez K. pneumoniae, l’AZT a emprunté une voie différente : il a activé des gènes impliqués dans la réparation de l’ADN, y compris une protéine centrale de la réponse SOS appelée RecA, et a réprimé des gènes nécessaires à la synthèse de l’acide aminé méthionine et de son dérivé S‑adénosylméthionine (SAM), donneur universel de groupes méthyle. L’ajout d’acétate de zinc, qui atténue l’activité de RecA, ou l’apport de SAM supplémentaire a tous deux restauré le transfert de plasmides en présence d’AZT, indiquant qu’un stress accru sur l’ADN et une méthylation perturbée contribuent à bloquer l’arrivée des plasmides.
Ce que cela signifie pour la lutte contre la résistance
Ce travail montre que certains analogues nucléosidiques existants peuvent servir de modèles pour une nouvelle classe de médicaments : des agents qui désarment la propagation de la résistance plutôt que de tuer les bactéries. L’AZT, en particulier, freine la conjugaison de plasmides chez deux pathogènes majeurs par des leviers différents — en empêchant la nage bactérienne dans un cas et en remodelant la réparation de l’ADN et le métabolisme de base dans l’autre. Dans le même temps, la découverte que d’autres analogues augmentent le transfert de plasmides souligne la nécessité de comprendre comment des médicaments non antibiotiques influencent le trafic des gènes au sein du microbiote intestinal. À terme, des inhibiteurs du transfert de plasmides finement ajustés pourraient faire partie de notre boîte à outils pour ralentir la progression de la résistance aux antimicrobiens, gagnant du temps pour que les antibiotiques existants et les nouveaux traitements restent efficaces.
Citation: Alav, I., Ashraf, A., Pordelkhaki, P. et al. Mechanistic insights into plasmid transfer inhibition in Enterobacterales by nucleoside analogues. npj Antimicrob Resist 4, 23 (2026). https://doi.org/10.1038/s44259-026-00197-5
Mots-clés: résistance aux antimicrobiens, transfert de plasmides, analogues nucléosidiques, Escherichia coli, Klebsiella pneumoniae