Clear Sky Science · ru
Механистические сведения о подавлении передачи плазмид в Enterobacterales нуклеозидными аналогами
Почему для нас важны крошечные кольца ДНК
Антибиотикорезистентность обычно ассоциируется с чрезмерным применением лекарств и упорными инфекциями, но есть и другой, менее заметный фактор, который помогает этим супербактериям распространяться: маленькие кольца ДНК, называемые плазмидами, которые перескакивают между бактериями. В этом исследовании поставлен практический вопрос с серьёзными последствиями: могут ли препараты, которые мы уже используем против вирусов, тихо замедлять или даже ускорять распространение генов устойчивости к антибиотикам между кишечными бактериями? Изучая, как определённые соединения, похожие на антивирусные, влияют на передачу плазмид у двух распространённых госпитальных патогенов, авторы обнаруживают новые пути блокировки распространения устойчивости в бактериальных сообществах — и одновременно предупреждают, что некоторые лекарства могут непреднамеренно усугубить проблему. 
Как гены устойчивости находят попутчиков
Многие из самых тревожных генов устойчивости к антибиотикам у Escherichia coli и Klebsiella pneumoniae расположены на плазмидах, которые могут копироваться и передаваться непосредственно от одной бактерии к другой в процессе, называемом конъюгацией. Эта передача ДНК помогает устойчивости стремительно распространяться по больничным палатам и кишечнику человека, даже когда бактерии не находятся под сильным давлением антибиотиков. Поскольку традиционные антибиотики убивают или замедляют рост бактерий, но не останавливают этот обмен генами, учёные начали искать «антиплазмидные» соединения, которые сохраняют рост бактерий в основном без изменений, но прерывают пути, по которым распространяется устойчивость.
Старые противовирусные препараты — новые роли
Команда протестировала 14 клинически одобренных нуклеозидных аналогов — малых молекул, изначально разработанных для разрушения вирусной или человеческой ДНК и РНК — чтобы выяснить, меняют ли они частоту перемещения плазмид между бактериями. С помощью флуоресцентных меток и проточной цитометрии они отслеживали перенос одной плазмиды, несущей гены расширенного спектра бета-лактамаз (которые разрушают многие пенициллиноподобные препараты) в E. coli, и другой плазмиды с геном карбапенемазы в K. pneumoniae. Несколько соединений, включая зидовудин (AZT), диданозин, ставудин и трифлуридин, явно снижали передачу плазмид при отсутствии торможения роста бактерий. Удивительно, но другие нуклеозидные аналоги, такие как фамцикловир, залцитабин, ацикловир и валацикловир, фактически усиливали обмен плазмидами хотя бы в одном из исследованных видов. Это означает, что некоторые препараты, назначаемые при вирусных инфекциях, теоретически могут способствовать более лёгкому распространению генов устойчивости в микробиоте кишечника.
Что меняется внутри бактериальной клетки
Чтобы понять механизм действия этих соединений, исследователи изучили несколько базовых характеристик бактериальной физиологии. Большинство лекарств не повреждали клеточные мембраны, не нарушали электрический потенциал и не вызывали вспышек реактивных форм кислорода, и в целом не меняли темп роста. Некоторые соединения, продвигающие плазмиды, умеренно снижали уровень АТФ — основного энергетического ресурса клетки, что указывает на связь между энергетическим балансом и затратами на работу аппарата передачи плазмид. Для наиболее сильного ингибитора, AZT, команда обратилась к РНК-секвенированию, которое показывает, какие гены повышают или понижают экспрессию при контакте бактерий с препаратом. 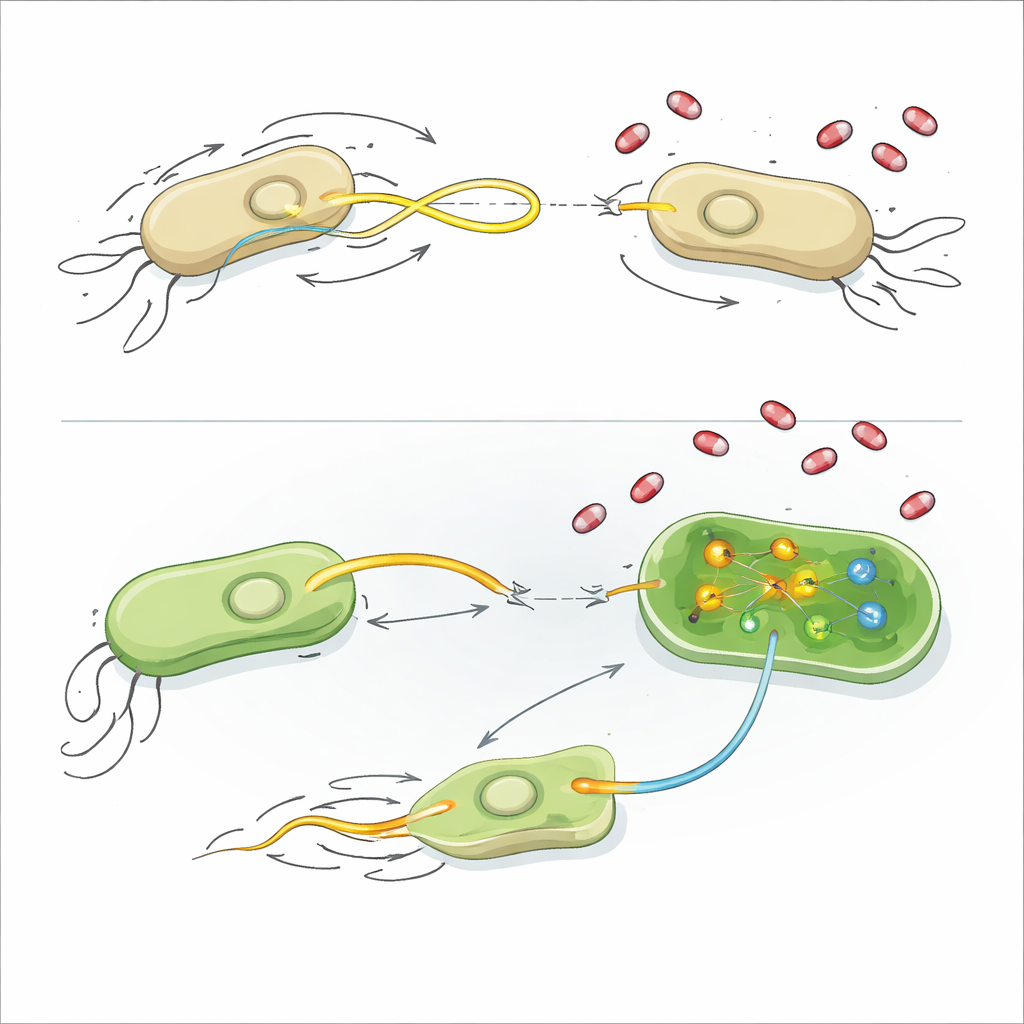
Замедление плавания и блокировка ремонта
В E. coli AZT резко понижал экспрессию генов, ответственных за построение и регуляцию жгутика — вращающегося хвоста, который позволяет клеткам передвигаться. Когда исследователи поместили E. coli на мягкий агар, AZT почти полностью остановил их разрастание по поверхности, несмотря на то что бактерии не погибали. Генетическое выключение ключевой части жгутика приводило к схожему снижению передачи плазмид, и добавление AZT к такому штамму не вызывало дальнейшего падения — это сильное свидетельство того, что снижение подвижности само по себе объясняет большую часть ингибирования. В K. pneumoniae AZT действовал иначе: он включал гены, участвующие в ремонте повреждений ДНК, в том числе центральный белок SOS-ответа RecA, и выключал гены, необходимые для синтеза аминокислоты метионина и её производного S-аденозилметионина (SAM), универсального донора метильных групп. Добавление ацетата цинка, который подавляет активность RecA, или дополнительного SAM восстанавливало передачу плазмид в присутствии AZT, что указывает на то, что усиление ДНК-стресса и нарушение метилирования помогают блокировать внедрение плазмид.
Что это значит для борьбы с устойчивостью
Эта работа показывает, что некоторые существующие нуклеозидные аналоги могут послужить основой для нового класса препаратов: агентов, которые нейтрализуют распространение устойчивости, не убивая бактерии напрямую. В частности, AZT сокращает конъюгацию плазмид у двух основных патогенов через разные механизмы — в одном случае останавливая бактериальное «плавание», в другом перестраивая систему ремонта ДНК и базовый метаболизм. В то же время обнаружение, что другие аналоги усиливают передачу плазмид, подчёркивает необходимость изучать, как неабиаотические препараты влияют на генетический трафик в кишечной микробиоте. В конечном счёте тонко настроенные ингибиторы передачи плазмид могут стать частью нашего арсенала для замедления марша антимикробной устойчивости, выигрывая время для существующих антибиотиков и новых методов лечения.»
Цитирование: Alav, I., Ashraf, A., Pordelkhaki, P. et al. Mechanistic insights into plasmid transfer inhibition in Enterobacterales by nucleoside analogues. npj Antimicrob Resist 4, 23 (2026). https://doi.org/10.1038/s44259-026-00197-5
Ключевые слова: антибактериальная устойчивость, передача плазмид, нуклеозидные аналоги, Escherichia coli, Klebsiella pneumoniae