Clear Sky Science · pl
Wgląd mechanistyczny w hamowanie transferu plazmidów u Enterobacterales przez analogi nukleozydów
Dlaczego małe pierścienie DNA są dla nas ważne
Oporność na antybiotyki zwykle kojarzy się z nadużywaniem leków i uporczywymi infekcjami, ale istnieje inny, mniej widoczny czynnik ułatwiający rozprzestrzenianie się tych nadmiernie odpornych bakterii: małe pierścienie DNA zwane plazmidami, które przemieszczają się między bakteriami. Badanie stawia praktyczne pytanie o dalekosiężnych konsekwencjach: czy leki stosowane dotąd przeciw wirusom mogą po cichu spowalniać albo wręcz przyspieszać rozprzestrzenianie się genów oporności między bakteriami jelitowymi? Analizując, jak niektóre związki przypominające leki antywirusowe wpływają na transfer plazmidów u dwóch powszechnych patogenów szpitalnych, autorzy odkrywają nowe sposoby blokowania przenoszenia oporności przez społeczności bakteryjne — jednocześnie ostrzegając, że niektóre leki mogą przypadkowo pogarszać problem. 
Jak geny oporności podróżują
Wiele z najbardziej niepokojących genów oporności u Escherichia coli i Klebsiella pneumoniae znajduje się na plazmidach, które potrafią się replikować i przekazywać bezpośrednio z jednej bakterii do drugiej w procesie nazywanym koniugacją. Ten przekaz DNA pozwala oporności rozprzestrzeniać się po oddziałach szpitalnych i w jelicie człowieka, nawet gdy bakterie nie są silnie eksponowane na antybiotyki. Ponieważ tradycyjne antybiotyki zabijają lub hamują wzrost bakterii, ale nie zatrzymują tego wymiany genów, naukowcy zaczęli szukać „anty-plazmidowych” związków, które pozostawiają wzrost bakterii w dużej mierze nienaruszony, a jednocześnie przecinają linie, wzdłuż których rozchodzi się oporność.
Stare leki antywirusowe, nowe role
Zespół przetestował 14 klinicznie zatwierdzonych analogów nukleozydów — małych cząsteczek pierwotnie zaprojektowanych do zaburzania wirusowego lub ludzkiego DNA i RNA — aby sprawdzić, czy zmieniają one częstość transferu plazmidów między bakteriami. Za pomocą znakowania fluorescencyjnego i cytometrii przepływowej śledzono transfer jednego plazmidu niosącego geny dla β-laktamazy o rozszerzonym spektrum (która rozkłada wiele leków podobnych do penicyliny) w E. coli oraz innego plazmidu przenoszącego gen karbapenemazy w K. pneumoniae. Kilka związków, w tym azidotymidyna (AZT), didanozyna, stawudyna i tryflurydyna, wyraźnie zmniejszyło transfer plazmidów bez spowalniania wzrostu bakterii. Zaskakująco, inne analogi nukleozydów, takie jak famcyklowir, zalkitabina, acyklowir i walacyklowir, w co najmniej jednym z badanych gatunków faktycznie zwiększały wymianę plazmidów. Oznacza to, że niektóre leki stosowane w zakażeniach wirusowych mogłyby w praktyce ułatwiać rozprzestrzenianie się genów oporności w mikrobiomie jelitowym.
Co zmienia się wewnątrz komórki bakteryjnej
Aby zrozumieć mechanizmy działania tych związków, badacze przyjrzeli się kilku podstawowym cechom fizjologii bakteryjnej. Większość leków nie uszkadzała błon komórkowych, nie zaburzała potencjału elektrycznego ani nie wywoływała skoków reaktywnych form tlenu, a ogólny wzrost pozostawał niezmieniony. Niektóre ze związków promujących plazmidy nieznacznie obniżały poziomy ATP, głównego nośnika energii w komórce, co sugeruje, że bilans energetyczny i koszt uruchomienia mechanizmów transferu plazmidu mogą być powiązane. Dla najsilniejszego inhibitora, AZT, zespół zastosował sekwencjonowanie RNA, które pokazuje, które geny są w górę lub w dół regulowane po zetknięciu bakterii z lekiem. 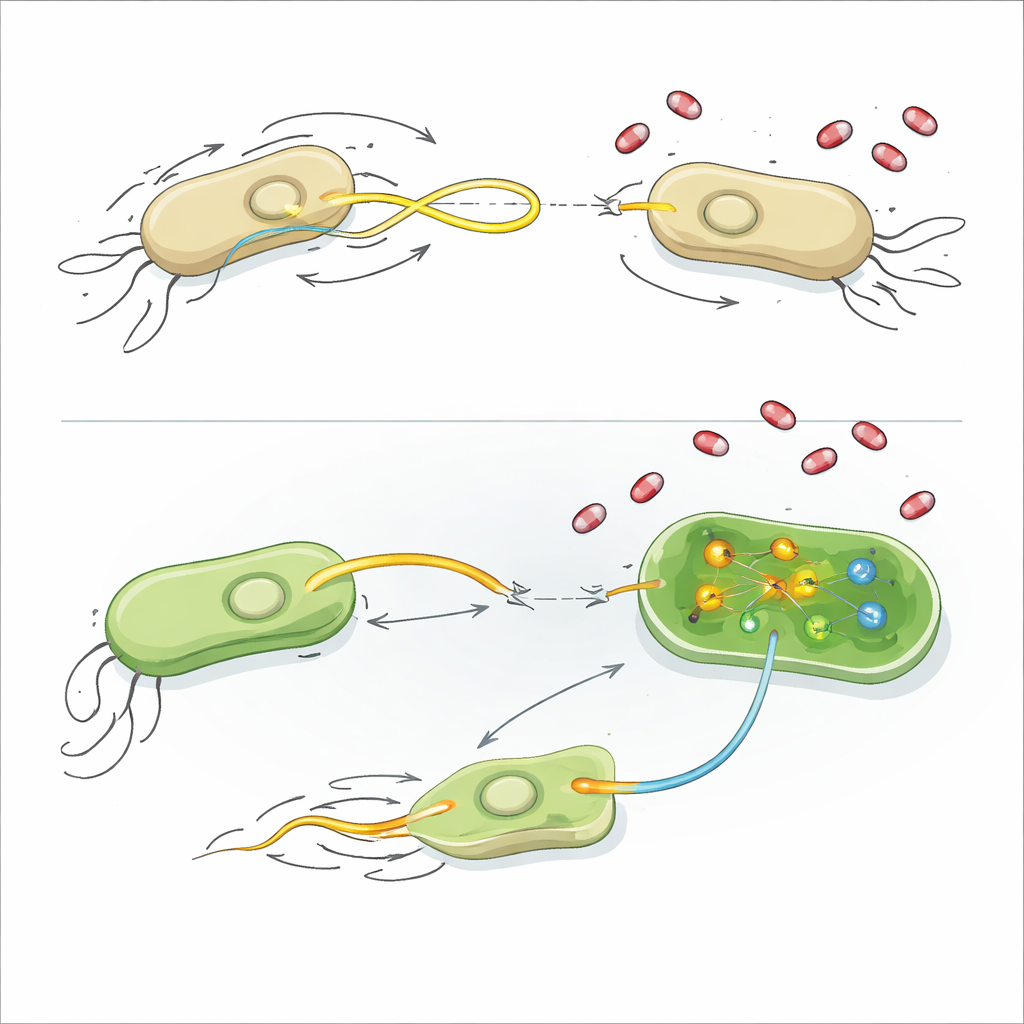
Spowolnienie pływania i blokada naprawy
W E. coli AZT wyraźnie obniżył ekspresję genów budujących i kontrolujących rzęskę, wirujący ogonek umożliwiający komórkom pływanie. Gdy badacze umieścili E. coli na miękkim agarze, AZT niemal całkowicie zatrzymał ich rozprzestrzenianie się, mimo że bakterie nie były zabijane. Genetyczne unieruchomienie kluczowego elementu rzęski miało podobny efekt w ograniczaniu transferu plazmidów, a dodanie AZT nie spowodowało dalszego spadku — to mocny dowód, że zmniejszona ruchliwość sama w sobie może wyjaśniać dużą część hamowania. W K. pneumoniae AZT zadziałał inną drogą: aktywował geny zaangażowane w naprawę uszkodzeń DNA, w tym centralny białkowy element odpowiedzi SOS zwany RecA, oraz wyciszał geny potrzebne do syntezy aminokwasu metioniny i jego pochodnej S-adenozylometioniny (SAM), uniwersalnego dawcy grup metylowych. Dodanie octanu cynku, który tłumi aktywność RecA, lub uzupełnienie SAM przywróciło transfer plazmidów w obecności AZT, co wskazuje, że nasilony stres DNA i zaburzona metylacja pomagają blokować przychodzące plazmidy.
Co to oznacza w walce z opornością
Praca pokazuje, że niektóre istniejące analogi nukleozydów mogą służyć jako wzorce dla nowego typu leków: środków unieszkodliwiających rozprzestrzenianie się oporności zamiast bezpośredniego zabijania bakterii. AZT w szczególności ogranicza koniugację plazmidów u dwóch głównych patogenów poprzez różne mechanizmy — zatrzymując pływanie bakterii w jednym przypadku i przekształcając naprawę DNA oraz podstawowy metabolizm w drugim. Jednocześnie odkrycie, że inne analogi zwiększają transfer plazmidów, podkreśla potrzebę zrozumienia, jak leki niebędące antybiotykami wpływają na ruch genów w mikrobiomie jelitowym. Ostatecznie precyzyjnie dobrane inhibitory transferu plazmidów mogłyby stać się elementem naszego zestawu narzędzi do spowalniania marszu oporności na środki przeciwdrobnoustrojowe, zyskując czas dla istniejących antybiotyków i nowych terapii, aby mogły działać.
Cytowanie: Alav, I., Ashraf, A., Pordelkhaki, P. et al. Mechanistic insights into plasmid transfer inhibition in Enterobacterales by nucleoside analogues. npj Antimicrob Resist 4, 23 (2026). https://doi.org/10.1038/s44259-026-00197-5
Słowa kluczowe: oporność na antybiotyki, transfer plazmidów, analogi nukleozydów, Escherichia coli, Klebsiella pneumoniae