Clear Sky Science · it
Approfondimenti meccanicistici sull’inibizione del trasferimento plasmidico negli Enterobacterales da parte di analoghi nucleosidici
Perché ci interessano piccoli anelli di DNA
La resistenza agli antibiotici richiama solitamente alla mente farmaci usati eccessivamente e infezioni ostinate, ma un altro attore, meno visibile, favorisce la diffusione di questi supermicrorganismi: piccoli anelli di DNA chiamati plasmidi che saltano da un batterio all’altro. Questo studio affronta una domanda pratica dalle grandi implicazioni: i farmaci che già usiamo per le infezioni virali possono, silenziosamente, rallentare o addirittura accelerare la diffusione dei geni di resistenza tra i batteri intestinali? Indagando come alcuni composti simili ad antivirali influenzano il trasferimento plasmidico in due patogeni comuni negli ospedali, i ricercatori individuano nuove strategie per bloccare lo spostamento della resistenza nelle comunità batteriche — e avvertono anche che alcuni farmaci potrebbero involontariamente peggiorare il problema. 
Come i geni di resistenza si fanno un passaggio
Molti dei geni di resistenza agli antibiotici più preoccupanti in Escherichia coli e Klebsiella pneumoniae si trovano su plasmidi, che possono auto-replicarsi e trasferirsi direttamente da un batterio all’altro tramite un processo chiamato coniugazione. Questo scambio di DNA facilita la rapida diffusione della resistenza nei reparti ospedalieri e nell’intestino umano, anche quando i batteri non sono sottoposti a forte pressione antibiotica. Poiché gli antibiotici tradizionali uccidono o rallentano i batteri ma non bloccano questo scambio genico, gli scienziati hanno iniziato a cercare composti “anti-plasmidici” che lascino sostanzialmente intatta la crescita batterica tagliando però le vie attraverso cui la resistenza si propaga.
Vecchi farmaci antivirali, nuovi ruoli
Il gruppo ha testato 14 analoghi nucleosidici approvati clinicamente — piccole molecole originariamente progettate per interferire con il DNA e l’RNA virali o umani — per verificare se modificassero la frequenza di trasferimento plasmidico tra batteri. Usando marcatori fluorescenti e citometria a flusso, hanno seguito il trasferimento di un plasmide che porta geni per una β-lattamasi a spettro esteso (che degrada molti farmaci tipo penicillina) in E. coli, e di un altro plasmide che porta un gene per carbapenemasi in K. pneumoniae. Diversi composti, tra cui azidotimidina (AZT), didanosina, stavudina e trifluridina, hanno chiaramente ridotto il trasferimento plasmidico senza rallentare la crescita batterica. Sorprendentemente, altri analoghi nucleosidici, come famciclovir, zalcitabina, aciclovir e valaciclovir, hanno effettivamente aumentato la condivisione dei plasmidi in almeno una delle specie testate. Ciò significa che alcuni farmaci somministrati per infezioni virali potrebbero, in teoria, spingere i geni di resistenza a diffondersi più facilmente nel microbioma intestinale.
Cosa cambia dentro la cellula batterica
Per capire come agiscono questi composti, i ricercatori hanno esaminato diverse caratteristiche di base della fisiologia batterica. La maggior parte dei farmaci non ha danneggiato le membrane cellulari, non ha perturbato il potenziale elettrico né ha scatenato esplosioni di specie reattive dell’ossigeno, e ha lasciato invariata la crescita complessiva. Alcuni dei composti che promuovono i plasmidi hanno leggermente ridotto i livelli di ATP, la principale valuta energetica della cellula, suggerendo che l’equilibrio energetico e il costo di attivare la macchina del trasferimento plasmidico possano essere collegati. Per l’inibitore più potente, l’AZT, il team ha ricorso al sequenziamento dell’RNA, che rivela quali geni sono up- o down-regolati quando i batteri incontrano il farmaco. 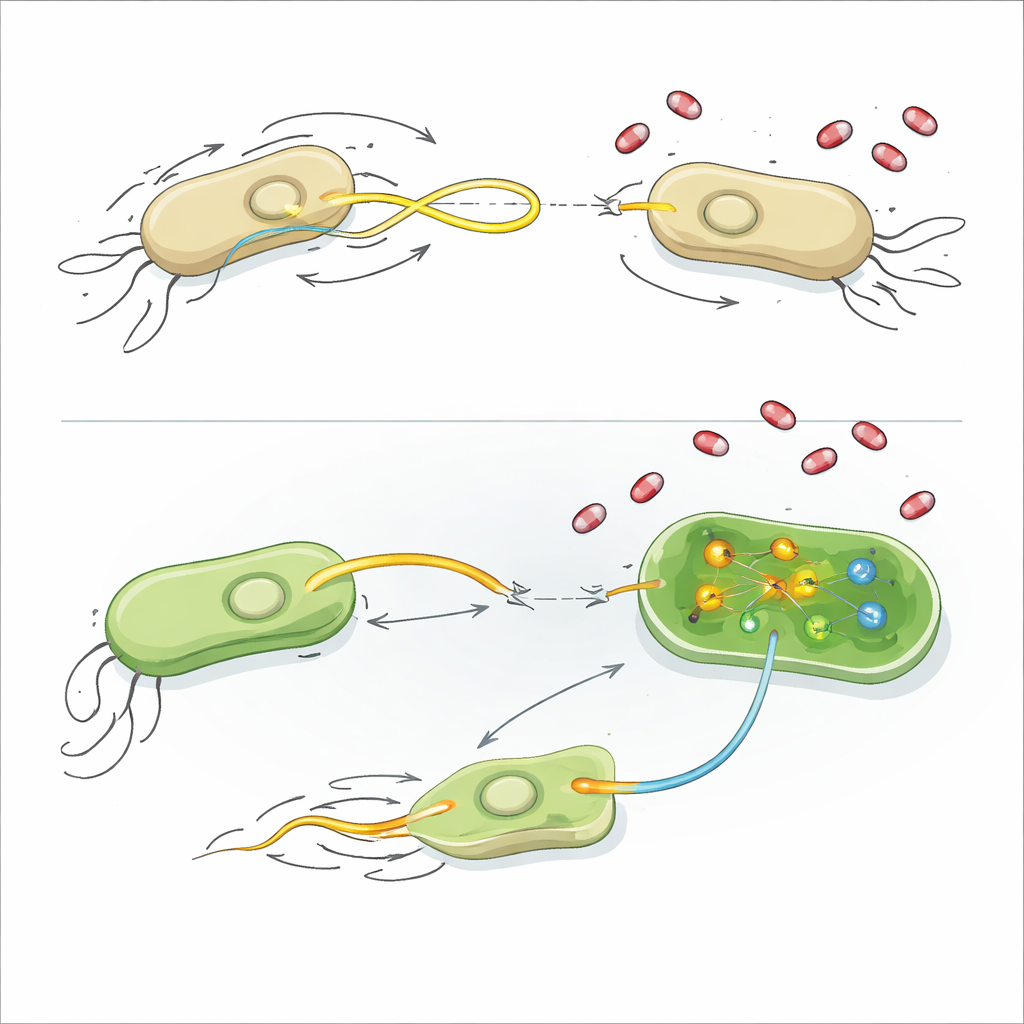
Rallentare il nuoto e bloccare la riparazione
In E. coli, l’AZT ha fortemente down-regolato geni coinvolti nella costruzione e nel controllo del flagello, la coda rotante che permette alle cellule di nuotare. Quando i ricercatori posizionarono E. coli su agar morbido, l’AZT ne fermò quasi completamente la dispersione verso l’esterno, anche se i batteri non venivano uccisi. Disabilitare geneticamente una componente chiave del flagello ebbe un effetto simile nel ridurre il trasferimento plasmidico, e aggiungere AZT a questo background non provocò ulteriori cali — una prova solida che la ridotta mobilità da sola può spiegare gran parte dell’inibizione. In K. pneumoniae, l’AZT seguì una strada diversa: attivò geni coinvolti nella riparazione del DNA, incluso una proteina centrale della risposta SOS chiamata RecA, e down-regolò geni necessari alla sintesi della metionina e del suo derivato S-adenosilmetionina (SAM), un donatore universale di gruppi metile. L’aggiunta di acetato di zinco, che attenua l’attività di RecA, o la fornitura di SAM supplementare ripristinò il trasferimento plasmidico in presenza di AZT, indicando che lo stress del DNA aumentato e la metilazione alterata contribuiscono a bloccare i plasmidi in arrivo.
Quali implicazioni per la lotta alla resistenza
Questo lavoro dimostra che alcuni analoghi nucleosidici esistenti possono fungere da modelli per un nuovo tipo di farmaco: agenti che disarmano la diffusione della resistenza piuttosto che uccidere direttamente i batteri. L’AZT, in particolare, limita la coniugazione plasmidica in due importanti patogeni tramite leve diverse — fermando il movimento batterico in un caso e rimodellando la riparazione del DNA e il metabolismo di base nell’altro. Allo stesso tempo, la scoperta che altri analoghi aumentano il trasferimento plasmidico sottolinea la necessità di comprendere come i farmaci non antibiotici influenzino il traffico genico microbico nell’intestino. In ultima analisi, inibitori finemente tarati del trasferimento plasmidico potrebbero entrare a far parte del nostro arsenale per rallentare la marcia della resistenza antimicrobica, acquistando tempo perché gli antibiotici esistenti e i nuovi trattamenti continuino a funzionare.
Citazione: Alav, I., Ashraf, A., Pordelkhaki, P. et al. Mechanistic insights into plasmid transfer inhibition in Enterobacterales by nucleoside analogues. npj Antimicrob Resist 4, 23 (2026). https://doi.org/10.1038/s44259-026-00197-5
Parole chiave: resistenza antimicrobica, trasferimento plasmidico, analoghi nucleosidici, Escherichia coli, Klebsiella pneumoniae