Clear Sky Science · es
Perspectivas mecanísticas sobre la inhibición de la transferencia de plásmidos en Enterobacterales por análogos de nucleósidos
Por qué nos importan los pequeños anillos de ADN
La resistencia a los antibióticos suele evocar fármacos sobreutilizados e infecciones persistentes, pero hay otro actor, menos visible, que facilita la propagación de estos supergérmenes: pequeños anillos de ADN llamados plásmidos que saltan entre bacterias. Este estudio plantea una pregunta práctica con grandes implicaciones: ¿pueden fármacos que ya usamos contra infecciones virales frenar inadvertidamente, o incluso acelerar, la difusión de genes de resistencia entre las bacterias intestinales? Al investigar cómo ciertos compuestos similares a antivirales afectan la transferencia de plásmidos en dos patógenos hospitalarios comunes, los investigadores descubren nuevas formas de bloquear el movimiento de la resistencia a través de comunidades bacterianas —y también advierten que algunos medicamentos podrían empeorar el problema sin querer. 
Cómo viajan los genes de resistencia
Muchos de los genes de resistencia a antibióticos más preocupantes en Escherichia coli y Klebsiella pneumoniae se encuentran en plásmidos, que pueden replicarse y transferirse directamente de una bacteria a otra en un proceso llamado conjugación. Este intercambio de ADN ayuda a que la resistencia se propague rápidamente por las salas de hospital y el intestino humano, incluso cuando las bacterias no están sometidas a una fuerte presión antibiótica. Dado que los antibióticos tradicionales matan o ralentizan a las bacterias pero no impiden este intercambio génico, los científicos han empezado a buscar compuestos “anti-plásmido” que dejen el crecimiento bacteriano en gran medida intacto mientras cortan las vías por las que viaja la resistencia.
Antiguos antivirales, nuevos papeles
El equipo evaluó 14 análogos de nucleósidos aprobados clínicamente —pequeñas moléculas diseñadas originalmente para alterar el ADN y ARN viral o humano— para ver si modificaban la frecuencia con la que los plásmidos se movían entre bacterias. Usando etiquetas fluorescentes y citometría de flujo, siguieron la transferencia de un plásmido que lleva genes de β-lactamasa de espectro extendido (que degrada muchos fármacos tipo penicilina) en E. coli, y de otro plásmido que porta un gen de carbapenemasa en K. pneumoniae. Varios compuestos, incluidos azidotimidina (AZT), didanosina, estavudina y trifluridina, redujeron claramente la transferencia de plásmidos sin ralentizar el crecimiento bacteriano. Sorprendentemente, otros análogos de nucleósidos, como famciclovir, zalcitabina, aciclovir y valaciclovir, de hecho aumentaron el intercambio de plásmidos en al menos una de las especies probadas. Eso significa que algunos medicamentos administrados por infecciones virales podrían, en principio, facilitar la propagación de genes de resistencia en el microbioma intestinal.
Qué cambia dentro de la célula bacteriana
Para entender cómo actúan estos compuestos, los investigadores examinaron varias características básicas de la fisiología bacteriana. La mayoría de los fármacos no dañaron las membranas celulares, no alteraron el potencial eléctrico ni desencadenaron ráfagas de especies reactivas de oxígeno, y dejaron el crecimiento general sin cambios. Algunos de los compuestos que promovieron plásmidos redujeron modestamente los niveles de ATP, la principal moneda energética de la célula, lo que sugiere que el equilibrio energético y el coste de operar la maquinaria de transferencia de plásmidos pueden estar relacionados. Para el inhibidor más potente, AZT, el equipo recurrió a la secuenciación de ARN, que muestra qué genes se activan o reprimen cuando las bacterias se exponen al fármaco. 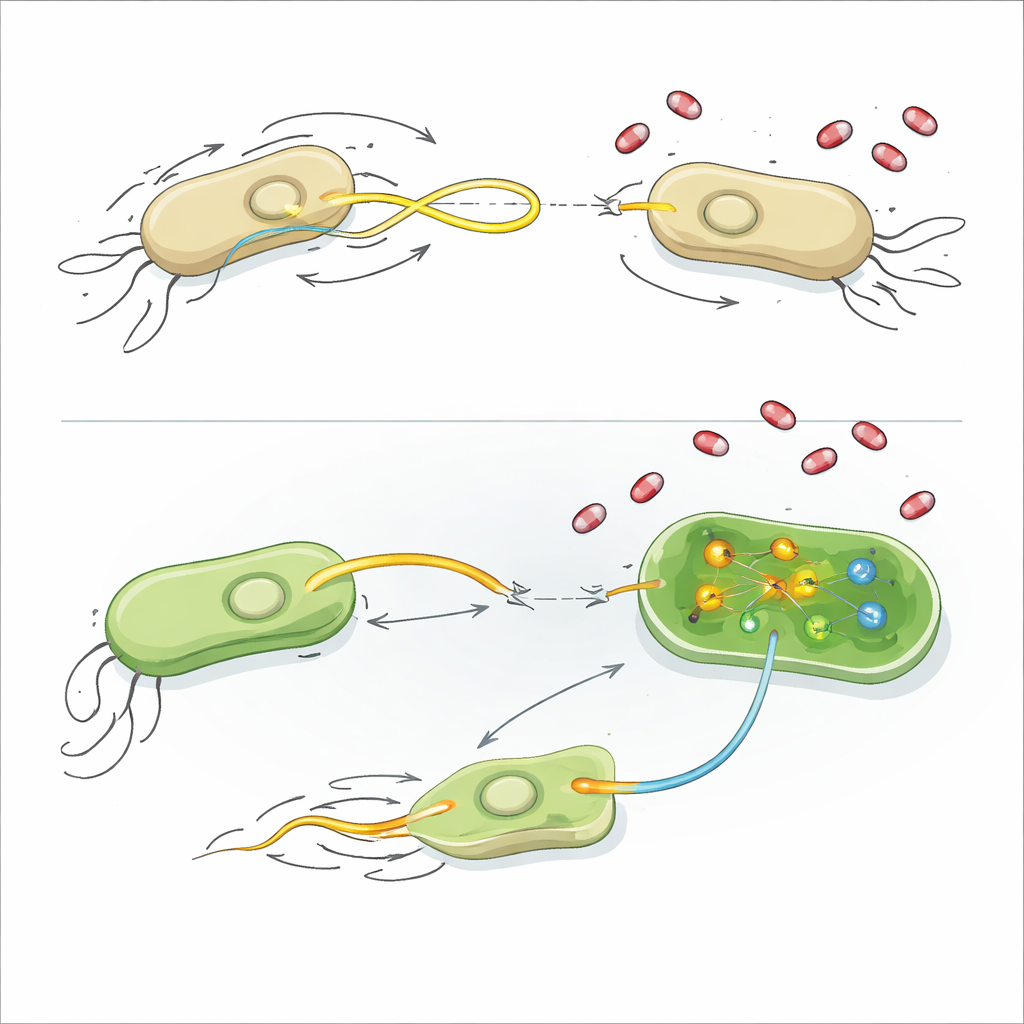
Reducir la natación y bloquear la reparación
En E. coli, AZT rebajó drásticamente los genes que construyen y controlan el flagelo, la cola giratoria que permite a las células nadar. Cuando los investigadores colocaron E. coli en agar blando, AZT casi dejó de permitir que se expandieran hacia fuera, aunque las bacterias no estaban siendo eliminadas. Inactivar genéticamente una parte clave del flagelo tuvo un efecto similar en la reducción de la transferencia de plásmidos, y añadir AZT además de esa mutación no ocasionó una caída adicional —evidencia sólida de que la motilidad reducida por sí sola puede explicar gran parte de la inhibición. En K. pneumoniae, AZT siguió una vía distinta: activó genes implicados en la reparación del ADN, incluido un proteína central de la respuesta SOS llamada RecA, y reprimió genes necesarios para sintetizar el aminoácido metionina y su derivado S-adenosilmetionina (SAM), un donante universal de grupos metilo. Añadir acetato de zinc, que atenúa la actividad de RecA, o suministrar SAM extra restauró la transferencia de plásmidos en presencia de AZT, lo que indica que el aumento del estrés sobre el ADN y la alteración de la metilación contribuyen a bloquear la entrada de plásmidos.
Qué significa esto para combatir la resistencia
Este trabajo muestra que algunos análogos de nucleósidos existentes pueden servir de plantilla para un nuevo tipo de fármaco: agentes que desarman la propagación de la resistencia en lugar de matar a las bacterias de forma directa. AZT, en particular, frena la conjugación de plásmidos en dos patógenos importantes mediante palancas diferentes —deteniendo la motilidad bacteriana en un caso y reconfigurando la reparación del ADN y el metabolismo básico en el otro. Al mismo tiempo, el hallazgo de que otros análogos aumentan la transferencia de plásmidos subraya la necesidad de comprender cómo los fármacos no antibióticos influyen en el tráfico genético del microbioma intestinal. En última instancia, los inhibidores de transferencia de plásmidos afinados podrían formar parte de nuestra caja de herramientas para frenar el avance de la resistencia a los antimicrobianos, ganando tiempo para que los antibióticos existentes y los nuevos tratamientos sigan siendo eficaces.
Cita: Alav, I., Ashraf, A., Pordelkhaki, P. et al. Mechanistic insights into plasmid transfer inhibition in Enterobacterales by nucleoside analogues. npj Antimicrob Resist 4, 23 (2026). https://doi.org/10.1038/s44259-026-00197-5
Palabras clave: resistencia a los antimicrobianos, transferencia de plásmidos, análogos de nucleósidos, Escherichia coli, Klebsiella pneumoniae