Clear Sky Science · tr
G-katriplex kaynaklı replikasyon stresi ile ilişkili nadir genetik hastalıklar
DNA Düğümleri Nadiren Görülen Hastalıklara Nasıl Yol Açar
Genetik materyalimiz genellikle düzgün, kıvrılan bir merdiven olarak tasvir edilir. Ancak birçok noktada DNA, G‑katriplex adı verilen kompakt düğümler halinde katlanabilir. Bu olağandışı şekiller, genomumuzun önemli düzenleyici bölgelerinde ve kromozom uçlarına yakın yerlerde özellikle yaygındır. Bu derleme, bu tür düğümlerin DNA’nın kopyalanmasını nasıl yavaşlattığını veya durdurduğunu, bunun “replikasyon stresi” yaratarak kromozomlara zarar verdiğini ve büyüme sorunları, bağışıklık kusurları, erken yaşlanma ve kanser riski gibi belirtilerle ortaya çıkan şaşırtıcı bir dizi nadir kalıtsal hastalığa nasıl katkıda bulunduğunu açıklar.
Genomumuzdaki Olağandışı DNA Şekilleri
G‑katriplexler, G (guanin) açısından zengin DNA dizilerinde oluşur. Olağan eşleşmenin dışında, dört guanin düz “plakalar” halinde istiflenip kararlı bir kolon oluşturabilir. Modern haritalama teknikleri, bu potansiyel bölgelerin insan genomu boyunca yüzbinlerce kez bulunduğunu; özellikle gen anahtarlarında (promoterler), kodlanmayan RNA bölgelerinde ve kromozomların koruyucu kapakları olan telomerlerde yoğunlaştığını gösteriyor. Hücrelerde ayrıca bu yapıları tanıyan veya stabilize eden proteinler de bulunur. Bunların birleşimi, G‑katriplexlerin nadir merak konuları değil, genlerin açılma biçimini, DNA üzerindeki kimyasal işaretlerin yerleşimini ve telomerlerin sürdürülmesini şekillendiren yinelenen özellikler olduğunu düşündürür.
DNA Kopyalanması Yoluna Taş Konduğunda
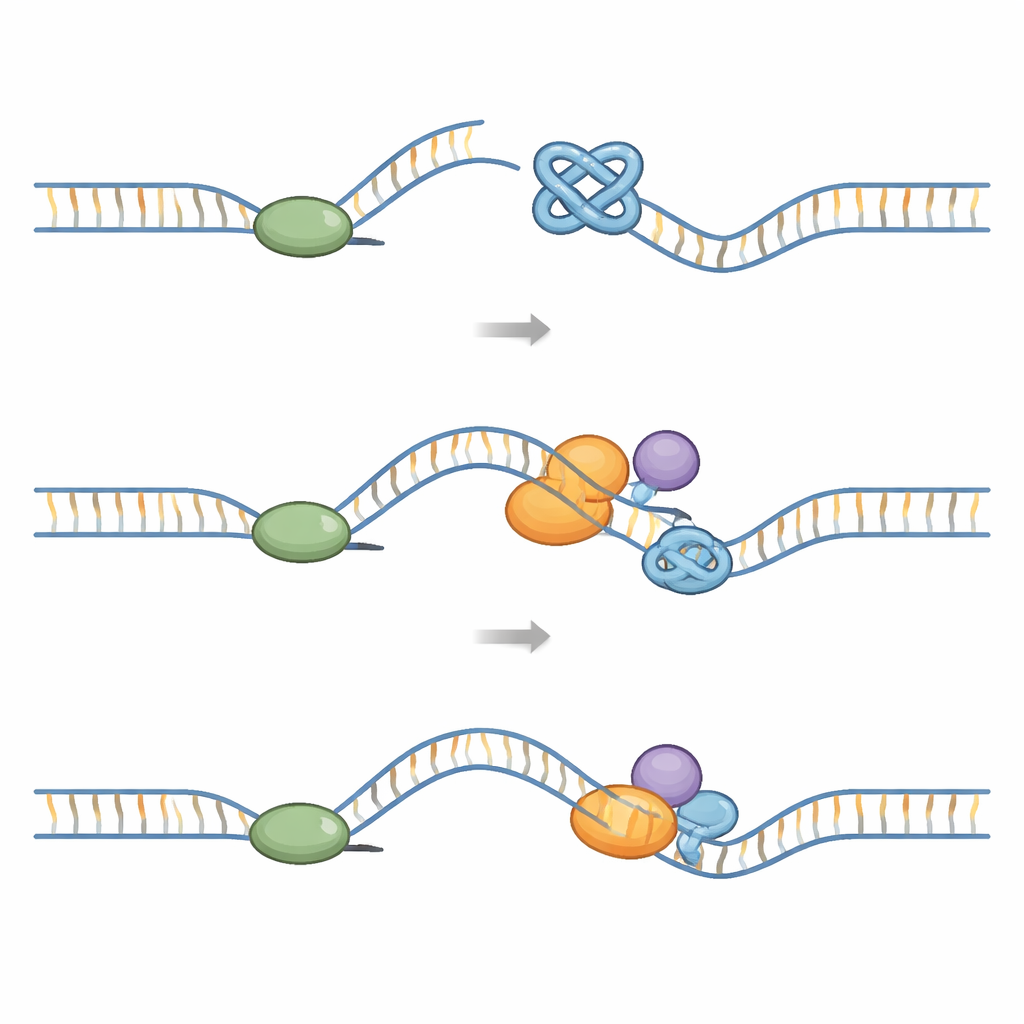
Her hücre bölünmesinde büyük bir “replizom” makinesi tüm genomu kopyalamak zorundadır. Bu makine, DNA’yı açan halka biçimli bir helikaz ve yeni zincirleri oluşturan polimerazları içerir. G‑katriplexler mekanik bir zorluk oluşturur: sıradan DNA’dan ayırmak onlar için daha zordur. Yapısal çalışmalar, replizom G‑katriplexle karşılaştığında düğümün helikaz halkasının içine sıkışıp hareketini engelleyebileceğini gösterir. Diğer deneyler, açığa çıkmış şablon zincir üzerinde oluşan G‑katriplexlerin polimerazı tıkayarak helikaz ile polimerazın birbirinden ayrılmasına yol açabileceğini ortaya koyar. Bu engeller temizlenmezse, DNA’yı kopyalayan çatal kırılabilir; bu da DNA çift zincir kırıklarına, kromozom yeniden düzenlenmelerine ve özellikle telomerlerde kırılgan bölgelere yol açar.
G‑Katriplex Düğümlerini Çözen Uzman Enzimler
Hücreler, G‑katriplexlerin kalıcı hasara yol açmasını önlemek için bir dizi “yardımcı” enzyme güvenir. DNA boyunca ilerleyip onu açan küçük motorlar olan birkaç helikaz ailesi özellikle önemlidir. BLM, WRN, RECQL4 ve RECQL1 gibi RecQ aile helikazları G‑katriplexleri, telomerlerdeki olanlar da dahil olmak üzere, tanıyıp çözülebilir. İkinci bir grup olan demir-kükürt (Fe–S) helikazları—FANCJ, RTEL1 ve DDX11 gibi—ve DNA2 ile PIF1 gibi enzimler de G‑katriplexleri sökebilir veya parçalara ayırabilir. Bazıları bireysel guaninleri veya belirli G‑katriplex şekillerini yakalayan özel cepler veya kama benzeri yapılar geliştirmiştir; bu sayede bu düğümleri adım adım çözerken DNA-bağlayıcı proteinler ve replikasyon faktörleriyle koordinasyon sağlayabilirler. HLTF gibi DNA translokazları ve DHX36 gibi G‑katriplex/R‑loop helikazları gibi diğer yeniden şekillendiriciler ise tıkanmış çataları yeniden düzenler veya replizomun engelleri aşmasına yardımcı olarak kopyalamanın tamamlanmasını sağlar.
Hatalı DNA Yardımcılarının Nadir Bozukluklara Nasıl Yol Açtığı
Bu G‑katriplex işleyici proteinler daha geniş onarım ve stres yanıtı rollerinde de görev yaptıkları için, genlerindeki kalıtsal mutasyonlar kendine özgü nadir hastalıklara yol açar. BLM’deki kusurlar, büyüme geriliği, bağışıklık bozuklukları ve yüksek kanser risimi ile karakterize Bloom sendromuna neden olur. WRN’deki mutasyonlar erken katarakt, diyabet ve kemik kaybı ile seyreden Werner sendromuna yol açar; bu, erken yaşlanma biçimidir. RTEL1’deki değişiklikler, kemik iliği yetmezliği ve çok kısa telomerlerle karakterize diskeratozis konjenita ve Hoyeraal–Hreidarsson sendromu gibi telomerle ilişkili bozuklukların temelini oluşturur. FANCJ ve BRCA2 mutasyonları Fanconi anemisi ve yüksek kanser duyarlılığı ile ilişkilendirilirken, DDX11 mutasyonları mikrosefali ve kardeş kromozomlar arasındaki kohezyon kusurlarıyla karakterize Warsaw Breakage Sendromu’na yol açar. Bu durumların birçoğunda hücrelerde G‑katriplex birikimi, tıkanmış replikasyon çataları, kırılgan telomerler ve kromozomal kırıklar gözlenir—bunların hepsi G‑katriplex kaynaklı replikasyon stresinin ayırt edici işaretleridir.
Nadir Genetik Bozukluklardan Yeni Tedavilere
Yazarlar, G‑katriplexlerin DNA yapısı, replikasyon ve hastalıklar arasında bir kavşakta yer aldığını savunuyor. Uygun şekilde kontrol edildiklerinde genleri ve telomerleri düzenlemeye yardımcı olabilirler; kontrol dışı kaldıklarında ise genomu zedeleyen ve nadir sendromlara, nörodejenerasyona ve muhtemelen yaşlanmanın bazı yönlerine katkıda bulunan yol bloklarına dönüşürler. Farklı enzimlerin belirli G‑katriplex şekillerini nasıl tanıdığını ve çözdüğünü tam olarak anlamak iki fırsat sunar: nadir replikasyon‑stres bozukluklarının tanısını iyileştirmek ve hedefe yönelik tedaviler tasarlamak. Bir tarafta, bazı erken klinik denemelerin önerdiği gibi zayıf onarım sistemine sahip tümör hücrelerini seçici olarak öldürmek için G‑katriplexleri stabilize eden ilaçlar var. Diğer tarafta, CRISPR kılavuzlu proteinler gibi gelişen stratejiler, bir gün belirli bölgelerde G‑katriplex oluşumunu ayarlayarak hatalı gen kontrolünü düzeltebilir. Her iki durumda da DNA’yı yalnızca bir çift sarmal olarak değil, dinamik yapıların bir peyzajı olarak görmek bu hastalıkları anlamak ve nihayetinde tedavi etmek için anahtardır.
Atıf: Herr, L.M., Mukhopadhyay, S., Anderson, O.M. et al. Rare genetic diseases associated with G-quadruplex-induced replication stress. Commun Biol 9, 522 (2026). https://doi.org/10.1038/s42003-026-09966-4
Anahtar kelimeler: G-katriplex DNA, replikasyon stresi, nadir genetik hastalıklar, DNA helikazları, telomer kararsızlığı