Clear Sky Science · pt
Doenças genéticas raras associadas ao estresse de replicação induzido por G-quadruplex
Quando nós no DNA levam a doenças raras
Normalmente imaginamos nosso material genético como uma escada torcida e lisa. Mas em muitos trechos o DNA pode se dobrar em nós compactos chamados G‑quadruplexos. Essas formas incomuns são especialmente frequentes em regiões importantes de controle do genoma e próximas às extremidades dos cromossomos. Esta revisão explica como esses nós podem desacelerar ou interromper a cópia do DNA, gerando “estresse de replicação” que danifica cromossomos e contribui para uma gama surpreendente de doenças hereditárias raras que frequentemente envolvem problemas de crescimento, defeitos imunes, envelhecimento prematuro e risco aumentado de câncer.
Formas incomuns de DNA em nosso genoma
G‑quadruplexos se formam em trechos de DNA ricos na letra G (guanina). Em vez de se emparelhar do modo habitual, quatro guaninas podem se empilhar em “placas” planas que se acumulam em uma coluna estável. Técnicas modernas de mapeamento revelam centenas de milhares desses sítios potenciais espalhados pelo genoma humano, especialmente em chaves de genes (promotores), regiões não traduzidas do RNA e nas capas protetoras dos cromossomos chamadas telômeros. As células também contêm proteínas que reconhecem ou estabilizam essas estruturas. Em conjunto, isso sugere que os G‑quadruplexos não são curiosidades raras, mas características recorrentes que ajudam a moldar como os genes são ativados, como marcas químicas são colocadas no DNA e como os telômeros são mantidos.
Quando a cópia do DNA encontra um obstáculo
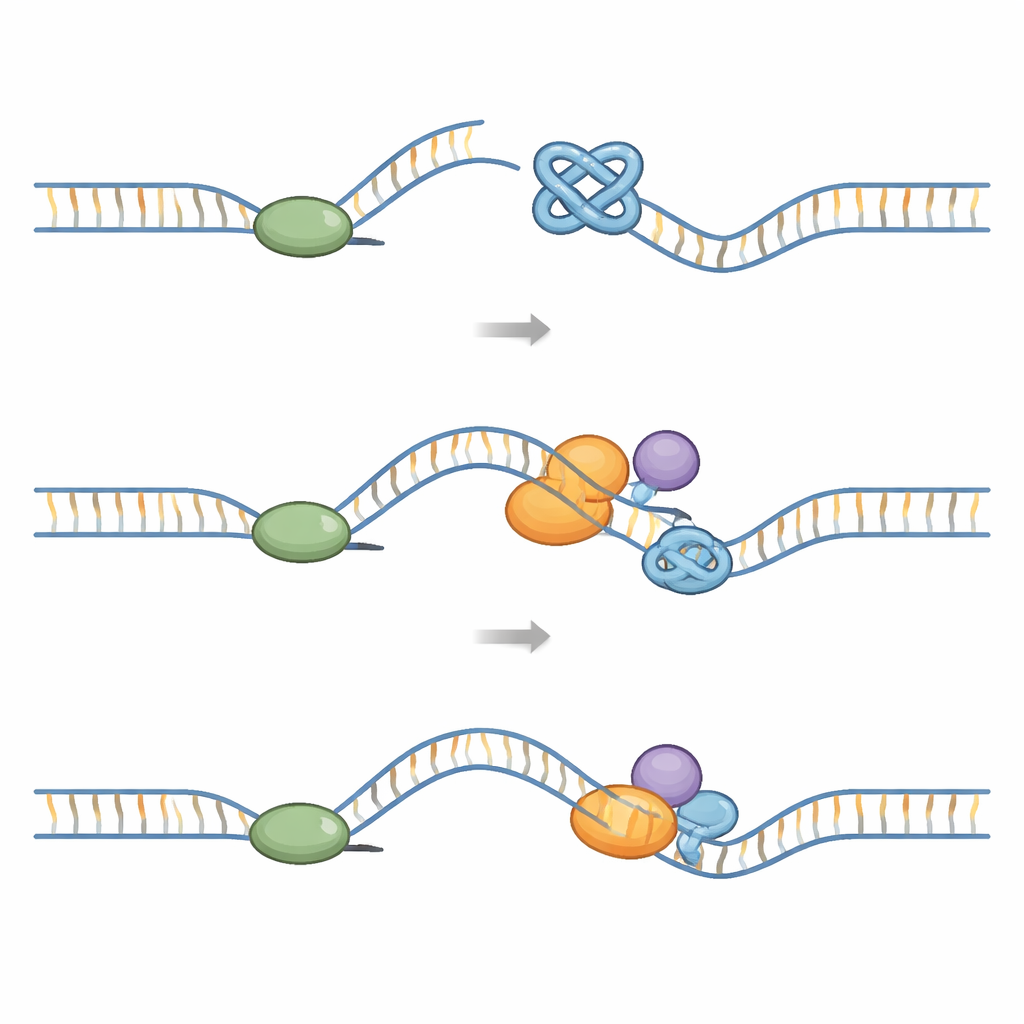
Cada vez que uma célula se divide, uma grande máquina chamada “replissoma” precisa duplicar todo o genoma. Essa máquina inclui uma helicase em forma de anel que abre o DNA e polimerases que constroem as novas fitas. G‑quadruplexos representam um desafio mecânico: são mais difíceis de separar que o DNA ordinário. Estudos estruturais mostram que, quando o replissoma encontra um G‑quadruplex, o nó pode alojar‑se dentro do anel da helicase e bloquear seu movimento. Outros experimentos revelam que G‑quadruplexos formados na fita molde exposta podem paralisar a própria polimerase e fazer com que helicase e polimerase se desacoplem. Se esses bloqueios não forem removidos, o garfo de replicação pode quebrar, levando a quebras de fita dupla no DNA, rearranjos cromossômicos e sítios frágeis, especialmente nos telômeros.
Enzimas especializadas que desfazem nós de G‑quadruplex
As células dependem de uma rede de enzimas “auxiliares” para evitar que os G‑quadruplexos causem danos duradouros. Várias famílias de helicases — minúscimos motores que percorrem o DNA e o desenrolam — são particularmente importantes. Helicases da família RecQ, como BLM, WRN, RECQL4 e RECQL1, podem reconhecer e desdobrar G‑quadruplexos, inclusive os dos telômeros. Um segundo grupo, as helicases contendo ferro‑enxofre (Fe–S) como FANCJ, RTEL1 e DDX11, e enzimas como DNA2 e PIF1, também desmontam G‑quadruplexos ou os clivam. Algumas evoluíram bolsos ou cunhas especiais que agarram guaninas individuais ou formas específicas de G‑quadruplex, permitindo que os desembrulhem passo a passo enquanto coordenam com proteínas ligadoras de DNA e fatores de replicação. Outros remodeladores, como a translocase de DNA HLTF e a helicase de G‑quadruplex/R‑loop DHX36, remodelam forquilhas estagnadas ou ajudam o replissoma a contornar obstáculos para que a cópia seja concluída.
Como auxiliares defeituosos do DNA causam distúrbios raros
Porque essas proteínas que lidam com G‑quadruplexos também atuam em funções mais amplas de reparo e resposta ao estresse, mutações hereditárias em seus genes dão origem a doenças raras distintas. Defeitos em BLM causam a síndrome de Bloom, marcada por deficiência de crescimento, problemas imunológicos e alto risco de câncer. Mutações em WRN levam à síndrome de Werner, uma forma de envelhecimento prematuro com catarata precoce, diabetes e perda óssea. Alterações em RTEL1 são a base de distúrbios relacionados a telômeros, como a disceratose congênita e a síndrome de Hoyeraal–Hreidarsson, que apresentam falência medular e telômeros muito curtos. Mutações em FANCJ e BRCA2 estão associadas à anemia de Fanconi e forte suscetibilidade ao câncer, enquanto mutações em DDX11 causam a Síndrome de Quebra de Varsóvia, com microcefalia e defeitos de coesão entre cromossomos irmãos. Em muitas dessas condições, as células mostram acúmulo de G‑quadruplexos, garfos de replicação estagnados, telômeros frágeis e quebras cromossômicas — todos sinais do estresse de replicação induzido por G‑quadruplex.
Das doenças genéticas raras a novos tratamentos
Os autores defendem que os G‑quadruplexos estão no cruzamento entre estrutura do DNA, replicação e doença. Quando controlados adequadamente, podem ajudar a regular genes e telômeros; quando não, tornam‑se obstáculos que danificam o genoma e contribuem para síndromes raras, neurodegeneração e possivelmente aspectos do envelhecimento. Entender exatamente como diferentes enzimas reconhecem e resolvem formas específicas de G‑quadruplex oferece duas oportunidades: melhorar o diagnóstico de distúrbios raros de estresse de replicação e projetar terapias direcionadas. De um lado estão drogas que estabilizam G‑quadruplexos para matar seletivamente células tumorais com sistemas de reparo frágeis, como sugerem alguns ensaios clínicos iniciais. Do outro, surgem estratégias — como proteínas guiadas por CRISPR — que podem um dia modular a formação de G‑quadruplex em locais escolhidos para corrigir controle gênico defeituoso. Em ambos os casos, ver o DNA não apenas como uma dupla hélice, mas como uma paisagem de estruturas dinâmicas é fundamental para compreender e, eventualmente, tratar essas doenças.
Citação: Herr, L.M., Mukhopadhyay, S., Anderson, O.M. et al. Rare genetic diseases associated with G-quadruplex-induced replication stress. Commun Biol 9, 522 (2026). https://doi.org/10.1038/s42003-026-09966-4
Palavras-chave: DNA G-quadruplex, estresse de replicação, doenças genéticas raras, helicases de DNA, instabilidade de telômeros