Clear Sky Science · ja
G四重鎖による複製ストレスに関連する希少な遺伝性疾患
DNAのもつれが希少疾患を引き起こすとき
遺伝情報は通常、滑らかにねじれたはしご状の構造として描かれます。しかし多くの箇所でDNAはG‑四重鎖と呼ばれる緊密なもつれ構造に折りたたまれることがあります。これらの異常な形はゲノムの重要な制御領域や染色体末端の近くに特に多く見られます。本レビューは、このようなもつれがDNAの複製を遅らせたり停止させたりして「複製ストレス」を生み、染色体を損傷し、成長障害、免疫不全、早期老化、がんのリスクを伴うという意外な範囲の希少な遺伝性疾患に寄与する仕組みを説明します。
ゲノムに現れる異様なDNA形状
G‑四重鎖はグアニン(G)が豊富に並ぶDNAの領域で形成されます。通常の塩基対とは異なり、四つのグアニンが平らな「板」を作り、それが積み重なって安定な柱状構造を成します。近年のマッピング技術は、このような潜在的部位がヒトゲノムの数十万箇所に散らばっていることを示しており、特に遺伝子のスイッチ(プロモーター)、未翻訳領域、そして染色体末端の保護キャップであるテロメアに集中しています。細胞内にはこれらの構造を認識したり安定化したりするタンパク質も存在します。これらを総合すると、G‑四重鎖は珍しい奇形ではなく、遺伝子の発現制御、DNA上の化学的マーキングの形成、テロメアの維持といった生物学的機能を形作る繰り返し現れる特徴であることが示唆されます。
複製が行き止まりに遭遇するとき
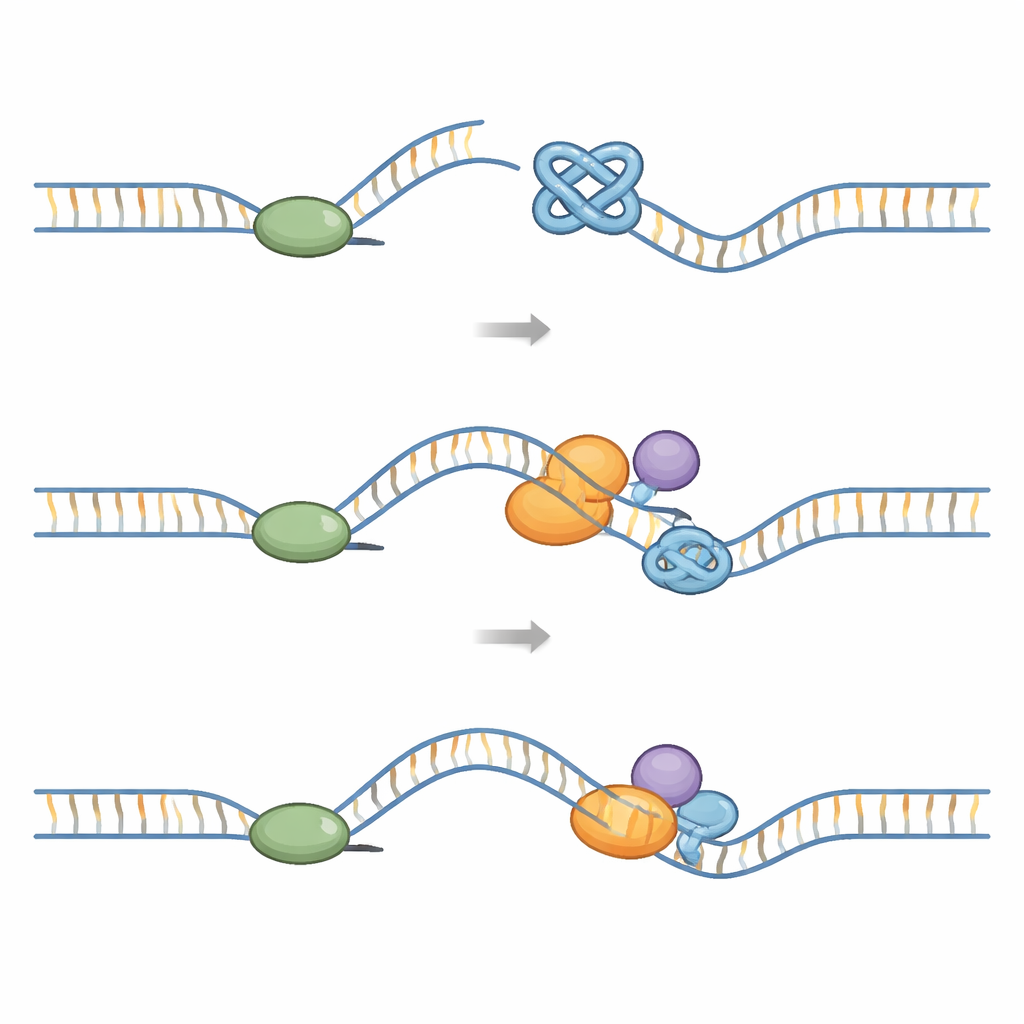
細胞が分裂するたびに、大きな「レプリソーム」機械がゲノム全体を複製しなければなりません。この機械はDNAを開くリング状のヘリカーゼや新しい鎖を合成するポリメラーゼを含みます。G‑四重鎖は機械的な障害を引き起こします:通常の二本鎖よりも分解しにくいのです。構造解析は、レプリソームがG‑四重鎖に遭遇すると、そのもつれがヘリカーゼのリング内に嵌り込んで移動を阻害することを示しています。他の実験からは、露出した鋳型鎖上に形成されたG‑四重鎖がポリメラーゼ自体を停滞させ、ヘリカーゼとポリメラーゼが連携を失うことが明らかになっています。これらの障害が除去されないと、複製フォークが切断され、二本鎖切断、染色体再配列、脆弱部位の出現、特にテロメアでの問題につながります。
G‑四重鎖のもつれをほどく専門酵素
細胞はG‑四重鎖が持続的な障害を引き起こさないように「補助」酵素のネットワークに依存しています。ヘリカーゼのいくつかのファミリー—DNAに沿って移動してほどく小さなモーター—が特に重要です。RecQファミリーのヘリカーゼ(BLM、WRN、RECQL4、RECQL1など)はG‑四重鎖、特にテロメア上のそれを認識して展開できます。第二のグループとして、鉄硫黄(Fe–S)ヘリカーゼ(FANCJ、RTEL1、DDX11など)やDNA2、PIF1といった酵素もG‑四重鎖を解体したり切り離したりします。これらの中には、個々のグアニンや特定のG‑四重鎖形状をつかむ特異なポケットや楔状構造を進化させたものがあり、DNA結合タンパク質や複製因子と調整しながら段階的にもつれを剥がしていきます。さらに、DNAトランスロケーゼHLTFやG‑四重鎖/RループヘリカーゼDHX36のようなリモデラーは、停滞したフォークを再構築したり、レプリソームが障害を回避して複製を完了できるよう支援します。
補助因子の障害がもたらす希少疾患
これらのG‑四重鎖処理タンパク質は、より広い修復およびストレス応答の役割も果たすため、これらの遺伝子に生じる遺伝性変異は特徴的な希少疾患を引き起こします。BLMの欠損はブルーム症候群を招き、成長障害、免疫問題、高いがん感受性を特徴とします。WRNの変異はワーナー症候群を引き起こし、早発白内障、糖尿病、骨減少を伴う早期老化の一形態です。RTEL1の変化は血球形成不全や非常に短いテロメアを特徴とするジスケラトーシス・コングニタ(dyskeratosis congenita)やホイエラール–フレイダルソン症候群(Hoyeraal–Hreidarsson syndrome)などのテロメア関連疾患の基盤になります。FANCJやBRCA2の変異はファンコニ貧血や高いがん感受性と関連し、DDX11の変異は小頭症や姉妹染色体間のコヒージョン欠損を伴うワルシャワ切断症候群(Warsaw Breakage Syndrome)を引き起こします。これら多くの疾患では、細胞内にG‑四重鎖の蓄積、停滞した複製フォーク、脆弱なテロメア、染色体切断の増加が観察され、いずれもG‑四重鎖誘導性複製ストレスの印です。
希少遺伝疾患から新たな治療へ
著者らは、G‑四重鎖がDNA構造、複製、疾患の交差点に位置すると論じています。適切に制御されればそれらは遺伝子やテロメアの制御に寄与しますが、制御を失うとゲノムを損なう障害となり、希少症候群、神経変性、さらには老化の一部に寄与します。異なる酵素がどのように特定のG‑四重鎖形状を認識・解決するかを正確に理解することは、希少な複製ストレス疾患の診断改善と標的治療設計の二つの機会を提供します。一方では、修復能力の弱い腫瘍細胞を選択的に殺すためにG‑四重鎖を安定化する薬剤があり、いくつかは初期の臨床試験で示唆されています。他方では、CRISPR誘導タンパク質のような新たな戦略が、将来的に選択した部位でのG‑四重鎖形成を調節して誤った遺伝子制御を修正する可能性があります。いずれの場合も、DNAを単なる二重らせんとしてではなく動的な構造の風景として捉えることが、これらの疾患を理解し、最終的に治療する鍵となります。
引用: Herr, L.M., Mukhopadhyay, S., Anderson, O.M. et al. Rare genetic diseases associated with G-quadruplex-induced replication stress. Commun Biol 9, 522 (2026). https://doi.org/10.1038/s42003-026-09966-4
キーワード: G四重鎖DNA, 複製ストレス, 希少遺伝疾患, DNAヘリカーゼ, テロメア不安定性