Clear Sky Science · fr
MALADIES GÉNÉTIQUES RARES ASSOCIÉES AU STRESS DE RÉPLICATION INDUIT PAR LES G‑QUADRUPLEX
Quand les nœuds d’ADN entraînent des maladies rares
Notre matériel génétique est généralement représenté comme une échelle torsadée et régulière. Mais à de nombreux endroits, l’ADN peut se replier en nœuds compacts appelés G‑quadruplexes. Ces formes inhabituelles sont particulièrement fréquentes dans des régions de contrôle importantes du génome et près des extrémités des chromosomes. Cette revue explique comment ces nœuds peuvent ralentir ou bloquer la copie de l’ADN, créant un « stress de réplication » qui endommage les chromosomes et contribue à une gamme surprenante de maladies héréditaires rares, souvent caractérisées par des problèmes de croissance, des déficits immunitaires, un vieillissement prématuré et un risque accru de cancer.
Formes d’ADN inhabituelles dans notre génome
Les G‑quadruplexes se forment dans des segments d’ADN riches en G (guanine). Au lieu de s’apparier de la façon habituelle, quatre guanines peuvent s’empiler en « plaques » plates qui s’imbriquent pour former une colonne stable. Les techniques de cartographie modernes mettent en évidence des centaines de milliers de sites potentiels de ce type disséminés dans le génome humain, notamment dans les commutateurs de gènes (promoteurs), les régions non traduites des ARN et les capuchons protecteurs des chromosomes appelés télomères. Les cellules contiennent aussi des protéines qui reconnaissent ou stabilisent ces structures. Ensemble, ces éléments suggèrent que les G‑quadruplexes ne sont pas de rares curiosités mais des caractéristiques récurrentes qui contribuent à façonner l’activation des gènes, le marquage chimique de l’ADN et le maintien des télomères.
Quand la copie de l’ADN se heurte à un obstacle
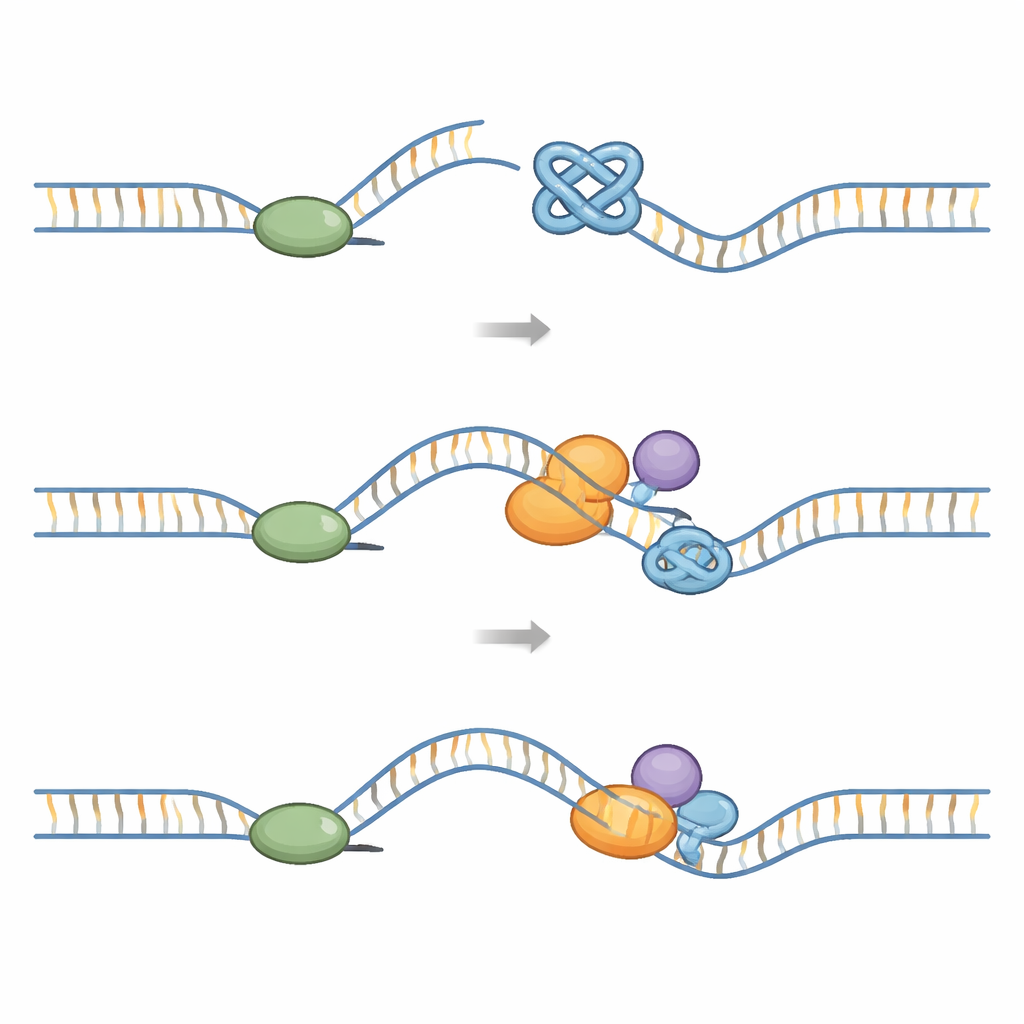
Chaque fois qu’une cellule se divise, une grande machine appelée « replisome » doit dupliquer l’intégralité du génome. Cette machine comprend une hélicase en forme d’anneau qui ouvre l’ADN et des polymérases qui synthétisent les nouveaux brins. Les G‑quadruplexes constituent un défi mécanique : ils sont plus difficiles à défaire que l’ADN ordinaire. Des études structurales montrent que lorsque le replisome rencontre un G‑quadruplex, le nœud peut se coincer à l’intérieur de l’anneau de l’hélicase et bloquer son déplacement. D’autres expériences révèlent que les G‑quadruplexes formés sur le brin matrice exposé peuvent arrêter la polymérase elle‑même et provoquer le découplage de l’hélicase et de la polymérase. Si ces blocages ne sont pas levés, la fourche de réplication peut se casser, entraînant des cassures double brin de l’ADN, des réarrangements chromosomiques et des sites fragiles, en particulier aux télomères.
Enzymes spécialisées qui dénouent les G‑quadruplexes
Les cellules s’appuient sur un réseau d’enzymes « assistantes » pour empêcher que les G‑quadruplexes ne causent des dommages durables. Plusieurs familles d’hélicases — de petites « moteurs » qui se déplacent le long de l’ADN et le déroulent — sont particulièrement importantes. Les hélicases de la famille RecQ, telles que BLM, WRN, RECQL4 et RECQL1, peuvent reconnaître et déplier les G‑quadruplexes, y compris ceux présents aux télomères. Un deuxième groupe, les hélicases fer‑soufre (Fe–S) comme FANCJ, RTEL1 et DDX11, ainsi que des enzymes telles que DNA2 et PIF1, démontent également les G‑quadruplexes ou les découpent. Certaines ont évolué des poches ou des cliquets spéciaux qui saisissent des guanines individuelles ou des formes particulières de G‑quadruplex, leur permettant de dérouler ces nœuds pas à pas tout en se coordonnant avec des protéines fixatrices d’ADN et des facteurs de réplication. D’autres remodelleurs, comme la translocase d’ADN HLTF et l’hélicase G‑quadruplex/R‑boucle DHX36, réagencent les fourches bloquées ou aident le replisome à contourner les obstacles afin que la réplication puisse se terminer.
Comment des aides défectueuses de l’ADN provoquent des troubles rares
Parce que ces protéines chargées de gérer les G‑quadruplex interviennent aussi dans des rôles plus larges de réparation et de réponse au stress, des mutations héréditaires dans leurs gènes entraînent des maladies rares caractéristiques. Les défauts de BLM provoquent le syndrome de Bloom, marqué par un retard de croissance, des problèmes immunitaires et un fort risque de cancer. Des mutations de WRN conduisent au syndrome de Werner, une forme de vieillissement prématuré avec cataractes précoces, diabète et perte osseuse. Des altérations de RTEL1 sont à l’origine de troubles liés aux télomères tels que la dyskératose congénitale et le syndrome de Hoyeraal–Hreidarsson, qui se manifestent par une insuffisance médullaire et des télomères très courts. Les mutations de FANCJ et BRCA2 sont associées à l’anémie de Fanconi et à une forte susceptibilité au cancer, tandis que des mutations de DDX11 provoquent le syndrome de rupture de Varsovie avec microcéphalie et défauts de cohésion entre chromosomes sœurs. Dans nombre de ces affections, les cellules présentent une accumulation de G‑quadruplexes, des fourches de réplication bloquées, des télomères fragiles et des cassures chromosomiques — autant de signes du stress de réplication induit par les G‑quadruplexes.
Des troubles génétiques rares aux nouvelles thérapies
Les auteurs soutiennent que les G‑quadruplexes se situent à la croisée de la structure de l’ADN, de la réplication et de la maladie. Lorsqu’ils sont correctement contrôlés, ils peuvent aider à réguler les gènes et les télomères ; lorsqu’ils ne le sont pas, ils deviennent des obstacles qui endommagent le génome et contribuent à des syndromes rares, à la neurodégénérescence et possiblement à certains aspects du vieillissement. Comprendre exactement comment différentes enzymes reconnaissent et résolvent des formes spécifiques de G‑quadruplex offre deux perspectives : améliorer le diagnostic des troubles rares liés au stress de réplication et concevoir des thérapies ciblées. D’un côté, des médicaments qui stabilisent les G‑quadruplexes pour tuer sélectivement les cellules tumorales aux systèmes de réparation affaiblis, comme le suggèrent certains essais cliniques précoces. De l’autre, des stratégies émergentes — telles que des protéines guidées par CRISPR — qui pourraient un jour moduler la formation de G‑quadruplex à des sites choisis pour corriger un contrôle génique défaillant. Dans les deux cas, envisager l’ADN non seulement comme une double hélice mais comme un paysage de structures dynamiques est essentiel pour comprendre, et éventuellement traiter, ces maladies.
Citation: Herr, L.M., Mukhopadhyay, S., Anderson, O.M. et al. Rare genetic diseases associated with G-quadruplex-induced replication stress. Commun Biol 9, 522 (2026). https://doi.org/10.1038/s42003-026-09966-4
Mots-clés: ADN en G‑quadruplex, stress de réplication, maladies génétiques rares, hélicases de l’ADN, instabilité des télomères