Clear Sky Science · nl
Zeldzame genetische ziekten geassocieerd met door G‑quadruplex veroorzaakte replicatiestress
Wanneer DNA‑knopen leiden tot zeldzame ziekten
Ons genetisch materiaal wordt vaak voorgesteld als een glad, gedraaid ladderpatroon. Maar op veel plaatsen kan DNA zich vouwen tot compacte knopen die G‑quadruplexen worden genoemd. Deze ongewone vormen komen vooral voor in belangrijke regelgebieden van ons genoom en nabij de uiteinden van chromosomen. Deze overzichtsartikel legt uit hoe zulke knopen het kopiëren van DNA kunnen vertragen of stilleggen, waardoor er “replicatiestress” ontstaat die chromosomen beschadigt en bijdraagt aan een verrassend scala aan zeldzame, erfelijke ziekten die vaak groeiproblemen, immuundefecten, voortijdige veroudering en een verhoogd kankerrisico omvatten.
Ongebruikelijke DNA‑vormen in ons genoom
G‑quadruplexen ontstaan in reeksen DNA die rijk zijn aan de letter G (guanine). In plaats van op de gebruikelijke manier te paren, kunnen vier guanines stapelen tot platte “schijven” die zich opstapelen tot een stabiele kolom. Moderne maptechnieken tonen honderden duizenden van deze potentiële plekken verspreid over het menselijk genoom, vooral in genregelaars (promoters), niet‑vertaalde delen van RNA en de beschermende uiteinden van chromosomen die telomeren worden genoemd. Cellen bevatten ook eiwitten die deze structuren herkennen of stabiliseren. Samen suggereert dit dat G‑quadruplexen geen zeldzame curiositeiten zijn maar terugkerende elementen die mede bepalen hoe genen worden aangeschakeld, hoe chemische markeringen op DNA worden aangebracht en hoe telomeren worden behouden.
Wanneer DNA‑duplicatie op een blokkade stuit
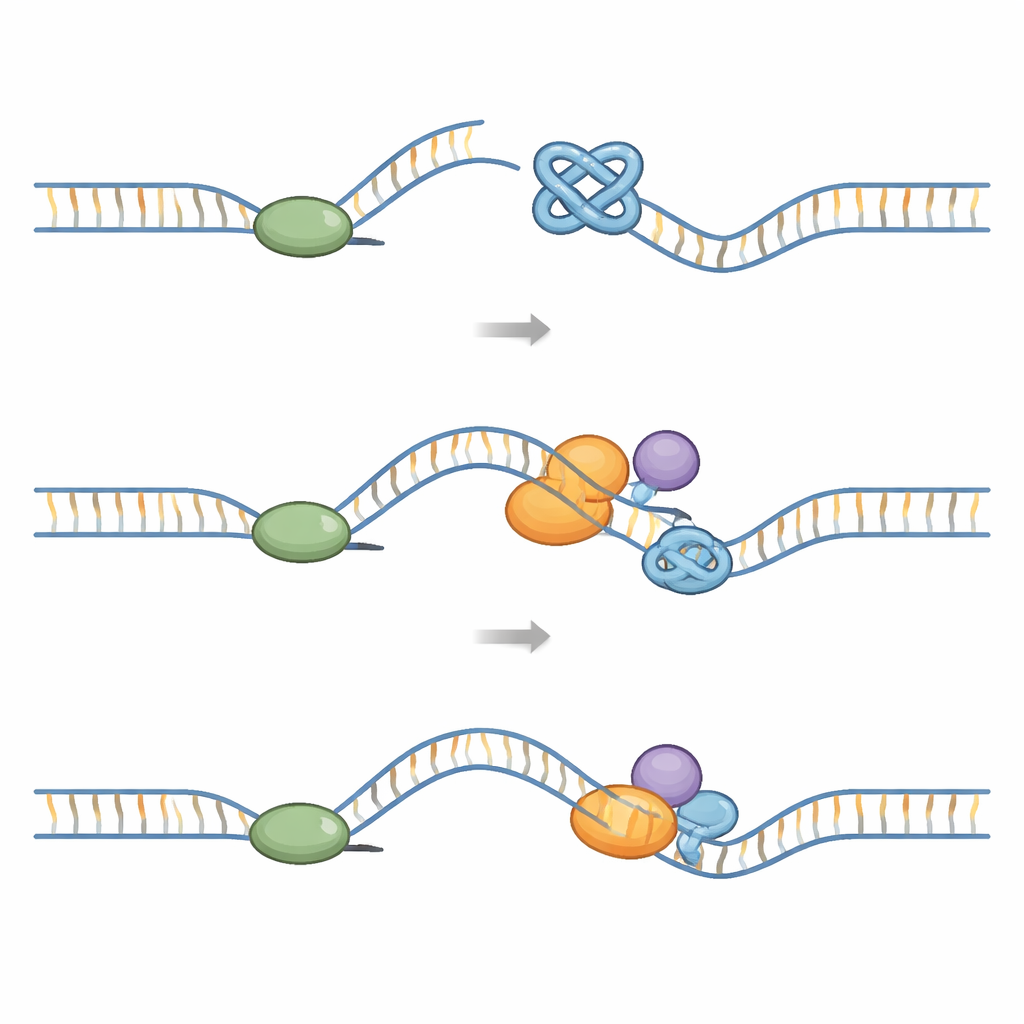
Elke keer dat een cel zich deelt, moet een groot “replisoom”‑machinerie het volledige genoom dupliceren. Deze machine bevat een ringvormige helikase die het DNA opent en polymerases die nieuwe strengen bouwen. G‑quadruplexen vormen een mechanische uitdaging: ze zijn moeilijker uit elkaar te trekken dan gewoon DNA. Structurele studies tonen dat wanneer het replisoom een G‑quadruplex tegenkomt, de knoop in de helikasering kan vastlopen en de voortgang blokkeert. Andere experimenten laten zien dat G‑quadruplexen die op de blootliggende matrijsstreng worden gevormd de polymerase zelf kunnen doen vastlopen en ervoor kunnen zorgen dat helikase en polymerase ontkoppeld raken. Als deze blokkades niet worden verwijderd, kan de vork die DNA kopieert breken, wat leidt tot dubbelstrengsbreuken in DNA, chromosomale herschikkingen en fragiele plekken, vooral bij telomeren.
Specialistische enzymen die G‑quadruplex‑knopen ontwarren
Cellen zijn afhankelijk van een netwerk van “hulp”enzymen om te voorkomen dat G‑quadruplexen blijvende schade veroorzaken. Verschillende families helikases — kleine motoren die langs DNA reizen en het ontwinden — zijn bijzonder belangrijk. RecQ‑familie helikases zoals BLM, WRN, RECQL4 en RECQL1 kunnen G‑quadruplexen herkennen en uitvouwen, inclusief die op telomeren. Een tweede groep, de ijzer‑zwavel (Fe–S) helikases zoals FANCJ, RTEL1 en DDX11, en enzymen zoals DNA2 en PIF1, breken G‑quadruplexen af of knippen ze uiteen. Sommigen hebben speciale holtes of wiggen ontwikkeld die individuele guanines of specifieke G‑quadruplexvormen grijpen, waardoor ze deze knopen stap voor stap kunnen losschillen terwijl ze coördineren met DNA‑bindende eiwitten en replicatiefactoren. Andere herschikkers, zoals de DNA‑translocase HLTF en de G‑quadruplex/R‑loop helikase DHX36, hervormen vastgelopen vorken of helpen het replisoom obstakels te omzeilen zodat de replicatie kan worden voltooid.
Hoe defecte DNA‑helpers zeldzame aandoeningen veroorzaken
Aangezien deze G‑quadruplex‑verwerkende eiwitten ook een rol spelen in bredere herstel‑ en stressreacties, leiden erfelijke mutaties in hun genen tot kenmerkende zeldzame ziekten. Defecten in BLM veroorzaken Bloom‑syndroom, gekenmerkt door groeiachterstand, immuunproblemen en een hoog kankerrisico. Mutaties in WRN leiden tot het Werner‑syndroom, een vorm van voortijdige veroudering met vroege staar, diabetes en botverlies. Veranderingen in RTEL1 liggen ten grondslag aan telomeergerelateerde aandoeningen zoals dyskeratosis congenita en het Hoyeraal–Hreidarsson‑syndroom, die beenmergfalen en zeer korte telomeren vertonen. FANCJ‑ en BRCA2‑mutaties zijn gekoppeld aan Fanconi‑anemie en sterke vatbaarheid voor kanker, terwijl DDX11‑mutaties het Warsaw Breakage‑syndroom veroorzaken met microcefalie en cohesion‑defecten tussen zusterchromosomen. In veel van deze aandoeningen tonen cellen een ophoping van G‑quadruplexen, vastgelopen replicatievorken, fragiele telomeren en chromosomale breuken — allemaal kenmerken van door G‑quadruplexen geïnduceerde replicatiestress.
Van zeldzame genetische aandoeningen naar nieuwe behandelingen
De auteurs betogen dat G‑quadruplexen op een kruispunt liggen tussen DNA‑structuur, replicatie en ziekte. Wanneer ze goed worden gecontroleerd, kunnen ze helpen genen en telomeren te reguleren; wanneer dat niet het geval is, worden ze blokkades die het genoom beschadigen en bijdragen aan zeldzame syndromen, neurodegeneratie en mogelijk aspecten van veroudering. Preciseren hoe verschillende enzymen specifieke G‑quadruplexvormen herkennen en oplossen biedt twee kansen: het verbeteren van de diagnose van zeldzame replicatiestress‑aandoeningen en het ontwerpen van gerichte therapieën. Enerzijds zijn er geneesmiddelen die G‑quadruplexen stabiliseren om tumorcellen met zwakke reparatiesystemen selectief te doden, zoals sommige vroege klinische onderzoeken suggereren. Anderzijds zijn er opkomende strategieën — zoals CRISPR‑geleide eiwitten — die op termijn de vorming van G‑quadruplexen op gekozen locaties zouden kunnen bijstellen om foutieve genregulatie te corrigeren. In beide gevallen is het zien van DNA niet alleen als een dubbele helix maar als een landschap van dynamische structuren cruciaal om deze ziekten te begrijpen en uiteindelijk te behandelen.
Bronvermelding: Herr, L.M., Mukhopadhyay, S., Anderson, O.M. et al. Rare genetic diseases associated with G-quadruplex-induced replication stress. Commun Biol 9, 522 (2026). https://doi.org/10.1038/s42003-026-09966-4
Trefwoorden: G‑quadruplex DNA, replicatiestress, zeldzame genetische ziekten, DNA‑helikases, telomeerinstabiliteit