Clear Sky Science · ar
أمراض وراثية نادرة مرتبطة بضغوط النسخ الناتجة عن تكوّن رباعيات G
عندما تؤدي تشابكات الحمض النووي إلى أمراض نادرة
عادةً ما يُصوَّر مادتنا الوراثية كدرج ملتف وسلس. لكن في أماكن كثيرة يمكن أن يطوي الحمض النووي نفسه إلى عقيدات مدمجة تُسمى رباعيات G. هذه الأشكال غير المألوفة شائعة خصوصاً في مناطق الضبط المهمة من جينومنا وبالقرب من أطراف الكروموسومات. تشرح هذه المراجعة كيف أن مثل هذه التشابكات يمكن أن تبطئ أو تعرقل عملية نسخ الحمض النووي، محدثةً «ضغط نسخ» يضر الكروموسومات ويسهم في طيف مفاجئ من الأمراض الوراثية النادرة التي غالباً ما تترافق مع مشاكل في النمو، واضطرابات مناعية، والشيخوخة المبكرة، وزيادة مخاطر السرطان.
أشكال حمض نووي غير مألوفة في جينومنا
تتشكل رباعيات G في مقاطع من الحمض النووي غنية بالحرف G (الجوانين). بدلاً من الاقتران بالطريقة الاعتيادية، يمكن لأربع قواعد جوانين أن تتكدس على شكل «صفائح» مسطحة تتراكم لتكوّن عموداً مستقراً. تُظهر تقنيات الخرائط الحديثة مئات الآلاف من هذه المواقع المحتملة متناثرة عبر الجينوم البشري، وخصوصاً في مفاتيح الجينات (المحفزات)، والمناطق غير المترجمة من الرنا، والغطاء الواقي على الكروموسومات المسمى التيلومير. تحتوي الخلايا أيضاً على بروتينات تتعرف على هذه البنى أو تُثبّتها. يشير هذا مجتمِعاً إلى أن رباعيات G ليست ظواهر نادرة غريبة بل خواص متكررة تسهم في تشكيل كيفية تشغيل الجينات، وكيف تُوضَع العلامات الكيميائية على الحمض النووي، وكيف تُحافَظ التيلوميرات.
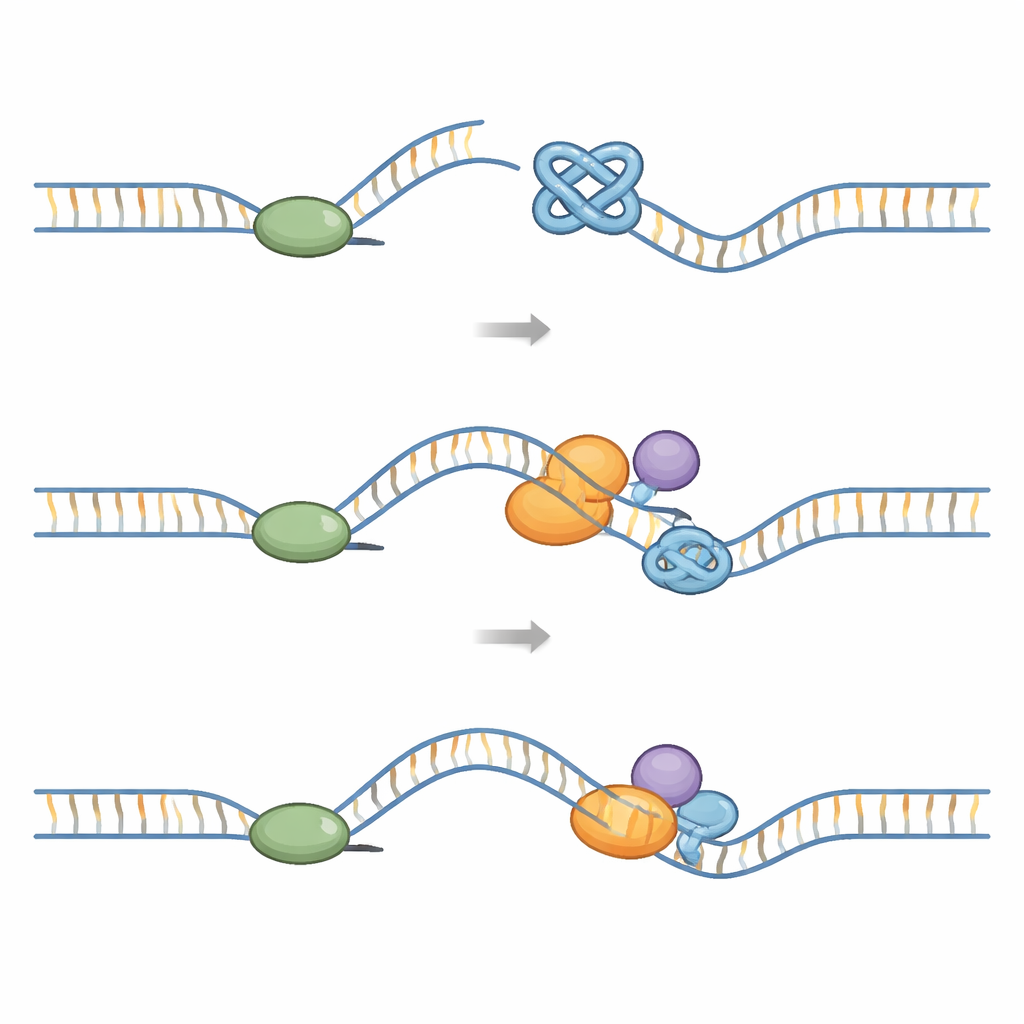
عندما تواجه آلية النسخ حاجزاً
في كل مرة تنقسم فيها خلية، يجب على آلة كبيرة تُدعى «المجمع النسخي» أن تduplicate entire the genome. تتضمن هذه الآلة هيليكاز حلقي الشكل يفتح الحمض النووي وبوليميرازات تبني الخيوط الجديدة. تشكّل رباعيات G تحدياً ميكانيكياً: فهي أصعب فكّاً من الحمض النووي العادي. تُظهر الدراسات الهيكلية أنه عندما يلتقي المجمع النسخي برابعية G، يمكن أن تحشر التشابك داخل حلقة الهيليكاز وتمنع حركته. تكشف تجارب أخرى أن رباعيات G المتشكلة على الشريط القالب المعرض يمكن أن توقف عمل البوليميراز نفسه وتتسبب في انفصال عمل الهيليكاز عن البوليميراز. إذا لم تُزَل هذه العوائق، قد ينكسر شوكة النسخ، ما يؤدي إلى كسور مزدوجة في الحمض النووي، وإعادة ترتيب الكروموسومات، ومواقع هشة، خاصةً عند التيلوميرات.
إنزيمات متخصصة تفك تشابكات رباعيات G
تعتمد الخلايا على شبكة من الإنزيمات «المساعدة» لمنع رباعيات G من إحداث أذى دائم. عدة عائلات من الهيليكازات — محركات صغيرة تسير على طول الحمض النووي وتفكه — لها أهمية خاصة. تُدرك هيليكازات عائلة RecQ مثل BLM وWRN وRECQL4 وRECQL1 رباعيات G وتفككها، بما في ذلك تلك الموجودة عند التيلوميرات. مجموعة ثانية، هيليكازات الحديد–الكبريت (Fe–S) مثل FANCJ وRTEL1 وDDX11، وإنزيمات مثل DNA2 وPIF1، تُحلّل أيضاً رباعيات G أو تقصّها. بعضها طوّر جيوباً أو أسافين خاصة تمسك الجوانين الفردية أو أشكال رباعيات G معينة، مما يسمح لها بتقشير هذه التشابكات خطوة بخطوة بينما تنسق عملها مع بروتينات رابطة للحمض النووي وعوامل النسخ. مُعيدات تشكيل أخرى، مثل ناقل الحمض النووي HLTF وهيليكاز رباعيات G/R‑لوب DHX36، تعيد تشكيل شوكات عالقة أو تساعد المجمع النسخي على تجاوز العقبات حتى يكتمل النسخ.
كيف تؤدي معينات الحمض النووي المعيبة إلى اضطرابات نادرة
لأن بروتينات التعامل مع رباعيات G تؤدي أيضاً أدواراً أوسع في الإصلاح والاستجابة للضغط، تؤدي الطفرات الموروثة في جيناتها إلى أمراض نادرة مميزة. التَعَطُّل في BLM يسبب متلازمة بلوم، المميزة بقِصَر في النمو ومشاكل مناعية وخطر عالٍ للإصابة بالسرطان. الطفرات في WRN تؤدي إلى متلازمة ورنر، شكل من أشكال الشيخوخة المبكرة مع إعتام عدسة مبكر ومرض السكري وفقدان العظم. التغيرات في RTEL1 تقف وراء اضطرابات متعلقة بالتيلومير مثل خلل التقرن الوراثي ومتلازمة هويرال‑هرايدارسون، والتي تتميّز بفشل نخاع العظم وتيلوميرات قصيرة جداً. ترتبط طفرات FANCJ وBRCA2 بفقر الدم الفانكوني وزيادة قوية في قابلية السرطان، بينما تسبب طفرات DDX11 متلازمة وارسو بريكِيج مع صغر الرأس وعيوب في التماسك بين الكروموسومات الشقيقة. في العديد من هذه الحالات تُظهر الخلايا تراكم رباعيات G، وشوكات نسخ متوقفة، وتيلوميرات هشة، وكسور كروموسومية — كلّها علامات لِضَغط النسخ الناتج عن رباعيات G.
من الاضطرابات الوراثية النادرة إلى علاجات جديدة
يجادل المؤلفون بأن رباعيات G تقع عند مفترق طرق بين بنية الحمض النووي والنسخ والمرض. عندما تُتحكم بها بشكل مناسب فقد تساعد في تنظيم الجينات والتيلوميرات؛ وعندما لا تُتحكم تصبح عقبات تُلحق ضرراً بالجينوم وتُسهم في متلازمات نادرة، والتنكس العصبي، وربما جوانب من الشيخوخة. إن فهم الكيفية الدقيقة التي تتعرف بها إنزيمات مختلفة على أشكال رباعيات G وتفكها يقدم فرصتين: تحسين تشخيص اضطرابات ضغط النسخ النادرة وتصميم علاجات موجهة. من جهة توجد أدوية تعمل على تثبيت رباعيات G لقتل الخلايا الورمية انتقائياً ذات أنظمة إصلاح ضعيفة، كما تشير بعض التجارب السريرية المبكرة. ومن جهة أخرى تظهر استراتيجيات ناشئة — مثل بروتينات موجهة بواسطة CRISPR — قد تتيح يومًا ما ضبط تشكل رباعيات G في مواقع مختارة لتصحيح خلل في تنظيم الجينات. في كلتا الحالتين، إن النظر إلى الحمض النووي ليس مجرد لولب مزدوج بل كمنظر من البنى الديناميكية هو المفتاح لفهم هذه الأمراض وفي النهاية معالجتها.
الاستشهاد: Herr, L.M., Mukhopadhyay, S., Anderson, O.M. et al. Rare genetic diseases associated with G-quadruplex-induced replication stress. Commun Biol 9, 522 (2026). https://doi.org/10.1038/s42003-026-09966-4
الكلمات المفتاحية: حمض نووي رباعي الـG, ضغط النسخ, أمراض وراثية نادرة, هيليكازات الحمض النووي, عدم استقرار التيلومير