Clear Sky Science · ru
Редкие генетические заболевания, связанные со стрессом репликации, индуцированным G‑квадруплексами
Когда спутывание ДНК ведёт к редким заболеваниям
Наша генетическая материя обычно представляется как плавная скрученная лестница. Но во многих местах ДНК может складываться в компактные узлы, называемые G‑квадруплексами. Эти необычные формы особенно часто встречаются в важных регуляторных областях генома и рядом с концами хромосом. В этом обзоре поясняется, как такие узлы могут замедлять или останавливать копирование ДНК, создавая «стресс репликации», который повреждает хромосомы и способствует появлению неожиданно большого спектра редких наследственных заболеваний, часто сопровождающихся проблемами роста, нарушениями иммунитета, преждевременным старением и повышенным риском рака.
Необычные формы ДНК в нашем геноме
G‑квадруплексы образуются в участках ДНК, богатых буквой G (гуанин). Вместо обычного спаривания четыре гуанина могут складываться в плоские «пластины», которые накладываются друг на друга в стабильный столб. Современные методы картирования выявляют сотни тысяч таких потенциальных участков по всему человеческому геному, особенно в переключателях генов (промоторах), несписуемых регионах РНК и защитных колпачках хромосом, называемых теломерами. В клетках также присутствуют белки, которые распознают или стабилизируют эти структуры. Всё это указывает на то, что G‑квадруплексы — не редкие диковинки, а повторяющиеся элементы, которые влияют на включение генов, расположение химических меток на ДНК и поддержание теломер.
Когда копирование ДНК натыкается на препятствие
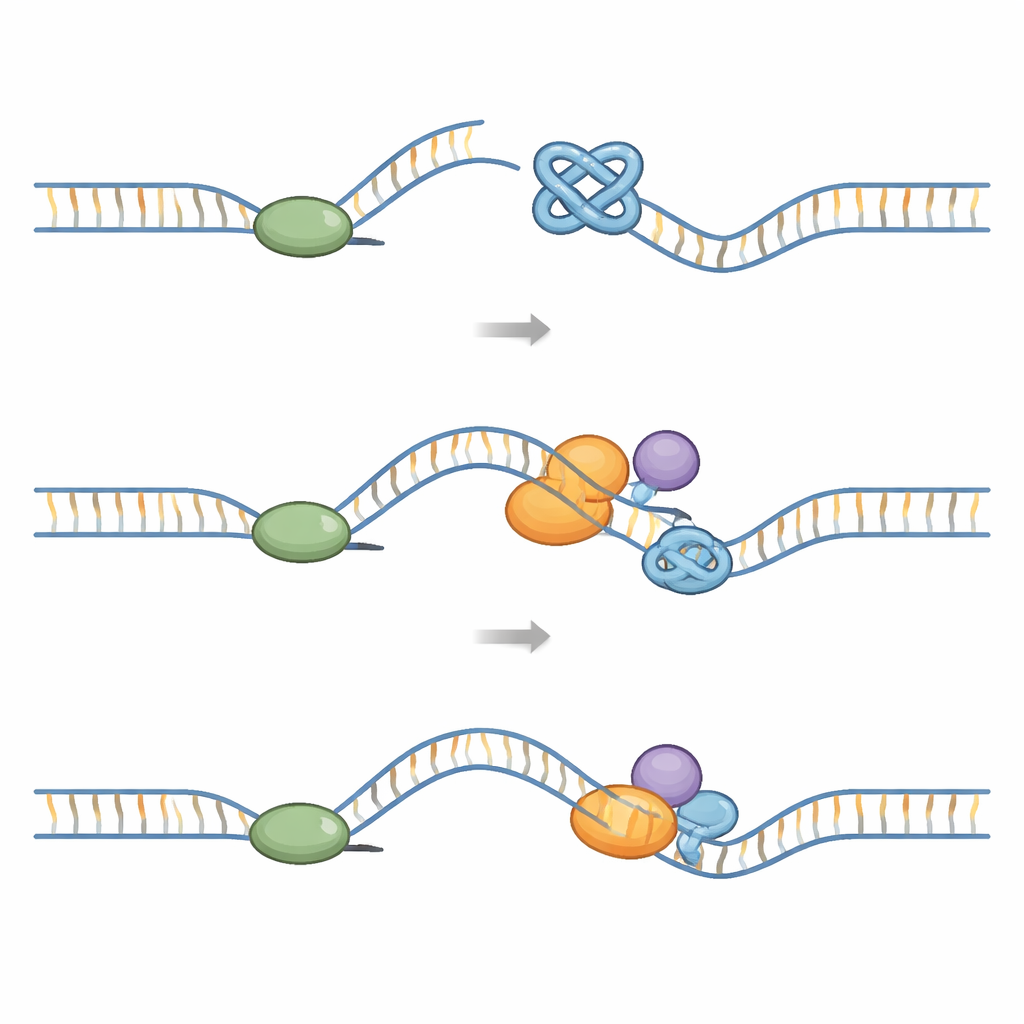
Каждый раз при делении клетки большой комплекс «реплисома» должен продублировать весь геном. Этот комплекс включает кольцевую хеликазу, которая расплетает ДНК, и полимеразы, синтезирующие новые цепи. G‑квадруплексам тяжело противостоять механически: их сложнее разъединить, чем обычную ДНК. Структурные исследования показывают, что когда реплисома встречает G‑квадруплекс, узел может застрять внутри кольца хеликазы и блокировать её движение. Другие эксперименты демонстрируют, что G‑квадруплексы, сформированные на открытой матричной цепи, могут останавливать саму полимеразу и приводить к рассоединению хеликазы и полимеразы. Если такие препятствия не устраняются, вилка репликации может ломаться, что ведёт к разрывам двойных спиралей ДНК, перестройкам хромосом и участкам хрупкости, особенно в теломерах.
Специализированные ферменты, распутывающие G‑квадруплексные узлы
Клетки полагаются на сеть «помогающих» ферментов, чтобы не допустить продолжительного вреда от G‑квадруплексов. Несколько семейств хеликаз — крошечных моторных белков, движущихся вдоль ДНК и расплетающих её — особенно важны. Хеликазы семейства RecQ, такие как BLM, WRN, RECQL4 и RECQL1, способны распознавать и разворачивать G‑квадруплексы, включая те, что находятся в теломерах. Вторая группа — железо‑серные (Fe–S) хеликазы, такие как FANCJ, RTEL1 и DDX11, а также ферменты вроде DNA2 и PIF1 — также разрушает G‑квадруплексы или разрезает их. Некоторые из них эволюционировали с особыми карманами или клиньями, которые захватывают отдельные гуанины или специфические формы G‑квадруплексов, позволяя шаг за шагом расплетать эти узлы в координации с белками, связывающими ДНК, и факторами репликации. Другие ремоделирующие белки, такие как транслоказа ДНК HLTF и хеликаза DHX36, распознающая G‑квадруплексы и R‑петли, перестраивают застрявшие вилки или помогают реплисомам обходить препятствия, чтобы копирование могло завершиться.
Как неисправные «помощники» ДНК вызывают редкие расстройства
Поскольку эти белки, перерабатывающие G‑квадруплекс, также участвуют в более широких путях ремонта и ответе на стресс, наследственные мутации в их генах приводят к характерным редким заболеваниям. Дефекты в BLM вызывают синдром Блума, характеризующийся задержкой роста, проблемами иммунитета и высоким риском рака. Мутации в WRN приводят к синдрому Вернера — форме преждевременного старения с ранней катарактой, диабетом и потерей костной массы. Изменения в RTEL1 лежат в основе заболеваний, связанных с теломерами, таких как дисперкатоз конгенитальный и синдром Хойераал–Хрейдарссона, которые сопровождаются недостаточностью костного мозга и очень короткими теломерами. Мутации в FANCJ и BRCA2 связаны с анемией Фанкони и сильной предрасположенностью к раку, тогда как мутации в DDX11 вызывают Варшавский синдром ломкости с микрокефалией и дефектами когезии между сестринскими хромосомами. Во многих этих состояниях клетки демонстрируют накопление G‑квадруплексов, застрявшие вилки репликации, хрупкие теломеры и хромосомные разрывы — все признаки стресса репликации, вызванного G‑квадруплексами.
От редких генетических нарушений к новым методам лечения
Авторы утверждают, что G‑квадруплексы находятся на перекрёстке структуры ДНК, репликации и заболеваний. При надлежащем контроле они могут помогать в регуляции генов и теломер; при нарушении контроля они становятся преградами, повреждающими геном и способствующими редким синдромам, нейродегенерации и, возможно, аспектам старения. Точное понимание того, как разные ферменты распознают и разрешают специфические формы G‑квадруплексов, открывает две возможности: улучшение диагностики редких расстройств, связанных со стрессом репликации, и разработку целевых терапий. С одной стороны — препараты, стабилизирующие G‑квадруплексы для избирательного уничтожения опухолевых клеток с ослабленными системами ремонта, как показывают первые клинические испытания. С другой — зарождающиеся стратегии, такие как белки, направляемые CRISPR, которые в будущем могли бы управлять формированием G‑квадруплексов в выбранных участках для коррекции нарушенного контроля генов. В обоих случаях важен взгляд на ДНК не только как на двойную спираль, но и как на ландшафт динамичных структур для понимания и, в перспективе, лечения этих заболеваний.
Цитирование: Herr, L.M., Mukhopadhyay, S., Anderson, O.M. et al. Rare genetic diseases associated with G-quadruplex-induced replication stress. Commun Biol 9, 522 (2026). https://doi.org/10.1038/s42003-026-09966-4
Ключевые слова: ДНК G‑квадруплекс, стресс репликации, редкие генетические заболевания, ДНК‑хеликазы, нестабильность теломер