Clear Sky Science · it
Malattie genetiche rare associate allo stress da replicazione indotto dai G-quadruplex
Quando i nodi del DNA portano a malattie rare
Il nostro materiale genetico è solitamente rappresentato come una scala elicoidale liscia. Ma in molti punti il DNA può piegarsi formando nodi compatti chiamati G-quadruplex. Queste forme insolite sono particolarmente comuni nelle regioni di controllo importanti del genoma e vicino alle estremità dei cromosomi. Questa rassegna spiega come tali nodi possano rallentare o arrestare la copia del DNA, creando uno “stress da replicazione” che danneggia i cromosomi e contribuisce a un sorprendente insieme di malattie ereditarie rare che spesso comportano problemi di crescita, difetti immunitari, invecchiamento precoce e rischio di cancro.
Forme insolite del DNA nel nostro genoma
I G-quadruplex si formano in tratti di DNA ricchi della lettera G (guanina). Invece di appaiarsi nel modo abituale, quattro guanine possono impilarsi in “piatti” piani che si sovrappongono a formare una colonna stabile. Le tecniche di mappatura moderne mostrano centinaia di migliaia di questi siti potenziali sparsi nel genoma umano, soprattutto negli interruttori genici (promoter), nelle regioni non tradotte dell’RNA e nelle cappette protettive dei cromosomi chiamate telomeri. Le cellule contengono inoltre proteine che riconoscono o stabilizzano queste strutture. Nel loro insieme, questi dati suggeriscono che i G-quadruplex non sono curiosità rare, ma elementi ricorrenti che contribuiscono a modulare l’attivazione dei geni, il posizionamento di marchi chimici sul DNA e il mantenimento dei telomeri.
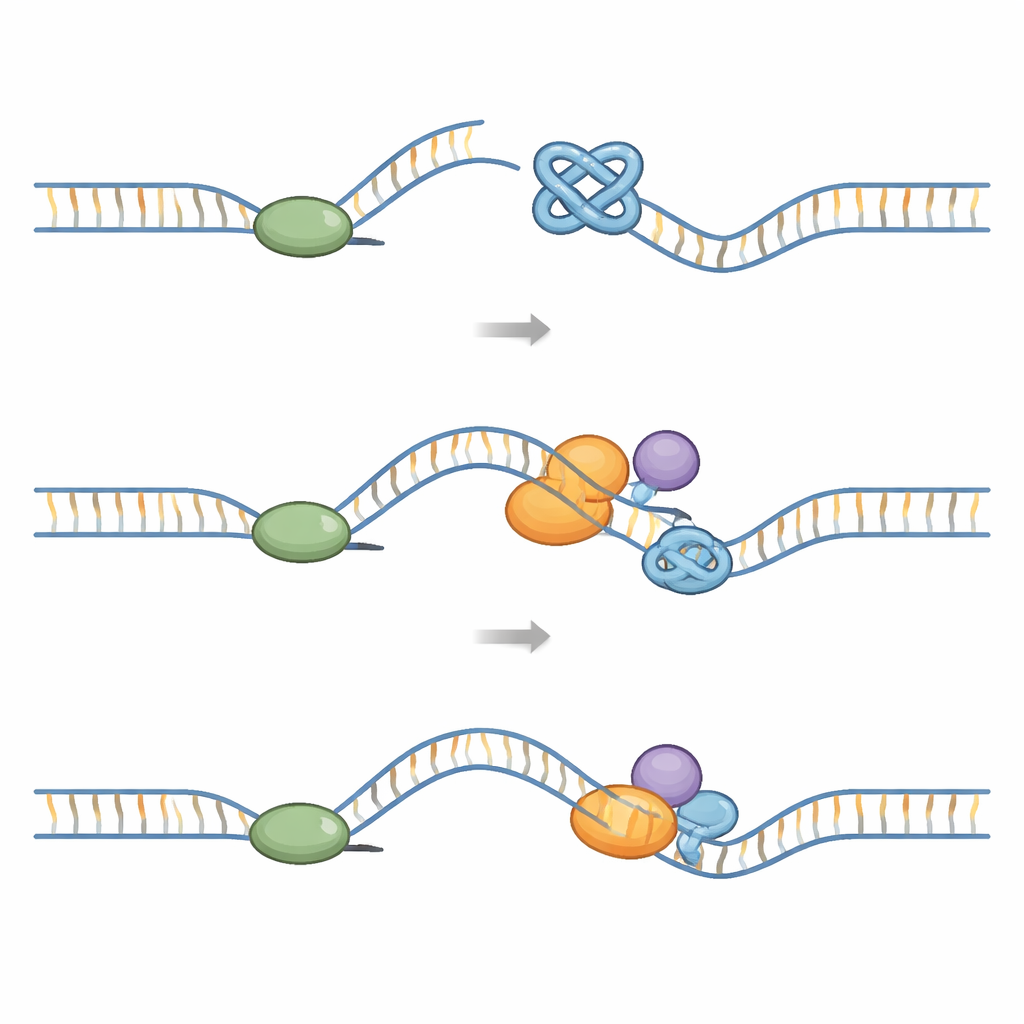
Quando la copia del DNA si imbatte in un ostacolo
Ogni volta che una cellula si divide, una grande macchina chiamata «replisoma» deve duplicare l’intero genoma. Questa macchina include un’elicasi ad anello che apre il DNA e polimerasi che costruiscono i nuovi filamenti. I G-quadruplex rappresentano una sfida meccanica: sono più difficili da separare rispetto al DNA ordinario. Studi strutturali mostrano che quando il replisoma incontra un G-quadruplex, il nodo può incastrarsi all’interno dell’anello dell’elicasi e bloccarne il movimento. Altri esperimenti rivelano che i G-quadruplex formati sul filamento stampo esposto possono arrestare la polimerasi stessa e causare lo scollegamento tra elicasi e polimerasi. Se questi blocchi non vengono rimossi, la forcella di replicazione può rompersi, portando a rotture a doppio filamento del DNA, riarrangiamenti cromosomici e siti fragili, specialmente ai telomeri.
Enzimi specialistici che sciolgono i nodi dei G-quadruplex
Le cellule fanno affidamento su una rete di enzimi «aiutanti» per impedire che i G-quadruplex provochino danni duraturi. Diverse famiglie di elicasi—piccoli motori che scorrono lungo il DNA e lo srotolano—sono particolarmente importanti. Le elicasi della famiglia RecQ come BLM, WRN, RECQL4 e RECQL1 possono riconoscere e disfarsi dei G-quadruplex, compresi quelli ai telomeri. Un secondo gruppo, le elicasi ferro-zolfo (Fe–S) come FANCJ, RTEL1 e DDX11, e enzimi come DNA2 e PIF1, smantellano o frammentano i G-quadruplex. Alcuni hanno evoluto tasche o cunei speciali che afferrano singole guanine o forme specifiche di G-quadruplex, permettendo loro di sfilare questi nodi passo dopo passo coordinandosi con proteine leganti il DNA e fattori di replicazione. Altri rimodellatori, come la translocasi del DNA HLTF e l’elicasi G-quadruplex/R-loop DHX36, rimodellano forcelle bloccate o aiutano il replisoma a aggirare ostacoli in modo che la duplicazione possa completarsi.
Come i problemi con gli «aiutanti» del DNA causano disordini rari
Poiché queste proteine che gestiscono i G-quadruplex svolgono anche ruoli più ampi nella riparazione e nella risposta allo stress, mutazioni ereditarie nei loro geni danno origine a malattie rare distintive. Difetti in BLM causano la sindrome di Bloom, caratterizzata da deficit di crescita, problemi immunitari e alto rischio di cancro. Mutazioni in WRN portano alla sindrome di Werner, una forma di invecchiamento precoce con cataratta precoce, diabete e perdita ossea. Varianti in RTEL1 sono alla base di disordini correlati ai telomeri come la discromatosi congenita e la sindrome di Hoyeraal–Hreidarsson, che presentano insufficienza del midollo osseo e telomeri molto corti. Mutazioni in FANCJ e BRCA2 sono associate all’anemia di Fanconi e a una forte suscettibilità al cancro, mentre mutazioni in DDX11 causano la sindrome da rottura di Varsavia con microcefalia e difetti di coesione tra cromatidi fratelli. In molte di queste condizioni, le cellule mostrano accumulo di G-quadruplex, forcelle di replicazione bloccate, telomeri fragili e rotture cromosomiche—tutti segni distintivi dello stress da replicazione indotto dai G-quadruplex.
Dai disturbi genetici rari a nuove terapie
Gli autori sostengono che i G-quadruplex si trovano all’incrocio tra struttura del DNA, replicazione e malattia. Quando sono controllati correttamente, possono contribuire a regolare geni e telomeri; quando non lo sono, diventano ostacoli che danneggiano il genoma e favoriscono sindromi rare, neurodegenerazione e possibilmente aspetti dell’invecchiamento. Comprendere esattamente come diversi enzimi riconoscano e risolvano forme specifiche di G-quadruplex offre due opportunità: migliorare la diagnosi dei disordini da stress di replicazione rari e progettare terapie mirate. Da un lato ci sono farmaci che stabilizzano i G-quadruplex per uccidere selettivamente le cellule tumorali con sistemi di riparo deboli, come suggeriscono alcuni primi trial clinici. Dall’altro emergono strategie—come proteine guidate da CRISPR—that un giorno potrebbero modulare la formazione di G-quadruplex in siti scelti per correggere un controllo genico difettoso. In entrambi i casi, considerare il DNA non solo come una doppia elica ma come un paesaggio di strutture dinamiche è fondamentale per comprendere, e infine trattare, queste malattie.
Citazione: Herr, L.M., Mukhopadhyay, S., Anderson, O.M. et al. Rare genetic diseases associated with G-quadruplex-induced replication stress. Commun Biol 9, 522 (2026). https://doi.org/10.1038/s42003-026-09966-4
Parole chiave: DNA a G-quadruplex, stress da replicazione, malattie genetiche rare, elicasi del DNA, instabilità dei telomeri