Clear Sky Science · tr
Protein katlanmasının kaba taneli modellenmesi için kuantum tavlamayı araştırmak
Geleceğin ilaçları için neden önemli
Proteinlerin katlandıkları şekiller, vücudumuzdaki işlevlerini—oksijen taşıma gibi görevlerden virüsleri tanımaya kadar—belirler. Bu şekilleri öngörmek ilaç tasarımı için hayati önemdedir, ancak tüm proteinler için doğru tahminler yapmak hâlâ son derece zordur. Bu makale, yeni bir hesaplama donanımı türü olan kuantum tavlayıcıların, günümüzün yapay zekâsı ve klasik süperbilgisayarlarının zorlandığı özellikle güç protein katlanma problemlerini bir gün çözmeye yardımcı olup olamayacağını sorguluyor.
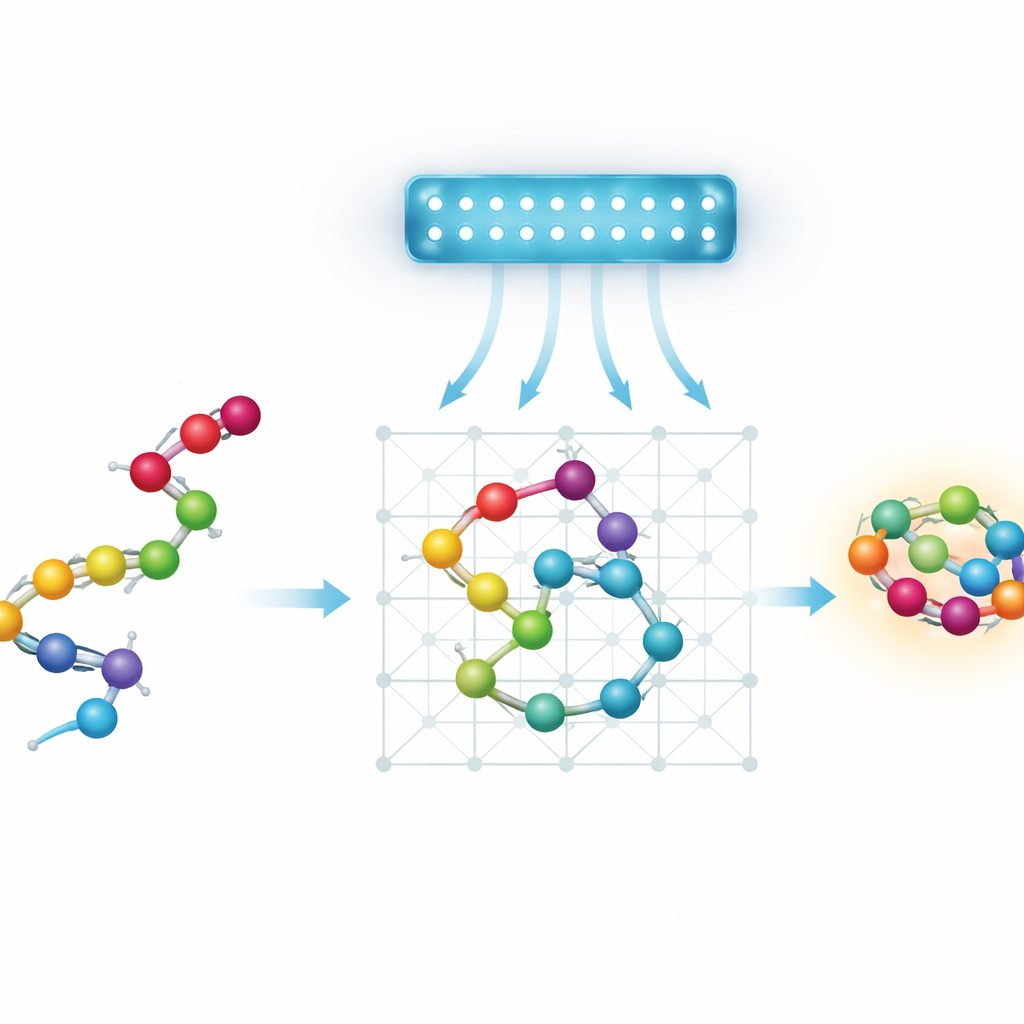
Proteinler, enerji peyzajları ve kestirmeciler arayışı
Özünde protein katlanması devasa bir arama problemidir. Bir amino asit zinciri astronomik sayıda biçime katlanabilir; her birinin kendine özgü bir enerjisi vardır. Doğa genellikle düşük enerjili biçimleri seçer, ancak “enerji peyzajı” engebelidir; derin vadiler dik tepelerle ayrılır. Standart optimizasyon yöntemleri ve fizikten esinlenen simülasyonlar genellikle yerel vadilere takılır ve en iyi biçimi kaçırır. Kuantum tavlama çekici görünür çünkü teoride tünelleme gibi kuantum etkileri, sistemin bu tepelerin üzerinden her zaman tırmanmak yerine bazılarını es geçmesine izin vererek iyi katları daha hızlı bulabileceğini öne sürer.
Kuantum makineleri için proteinleri basitleştirmek
Günümüz kuantum tavlayıcıları boyut ve bağlantı açısından sınırlı olduğu için yazarlar proteinleri basitleştirilmiş, yani kaba taneli modellerle ele alıyor. Her atomu takip etmek yerine her amino asidi ayrık bir ızgarada bir boncuk olarak temsil ediyorlar. Bu düzeni bir kuantum tavlayıcının işleyebileceği matematiksel bir bulmacaya kodlamanın dört yolunu inceliyorlar. İki “dönüş-temelli” model zinciri, ızgarada attığı adımların dizisiyle tanımlar. İki “koordinat-temelli” model ise her boncuğu belirli bir kafes pozisyonuna atar. Her varyant ya standart kübik ızgarada ya da her boncuğun daha az komşusu olduğu daha ekonomik tetrahedral ızgarada düzenlenebilir. Ekip ayrıca, etkileşimleri basit tutarken dönüşümlü boncukları temsil etmek için iki iç içe geçmiş ızgara kullanan yeni bir tetrahedral koordinat-temelli şema tanıtıyor.
Model kalitesini ve problem zorluğunu test etmek
Yazarlar önce ayrıntılı bir “kaynak denetimi” yapıyor: protein uzunluğu arttıkça her modelin kaç ikili değişken (qubit), kaç eş-ilişki ve hangi etkileşim gücü aralığına ihtiyaç duyduğunu. Bazı dönüş-temelli kodlamaların hızla fazla yoğunlaştığını ve çok yüksek sayısal hassasiyet gerektirdiğini gösteriyorlar; bunların ikisi de mevcut donanım için olumsuz özellikler. Önceki önerilmiş bir dönüş-temelli tetrahedral model ise daha derin bir kusuru ortaya koyuyor: yaklaşık on amino asitten daha uzun dizilerde fiziksel olarak imkânsız olan kendi kendine kesişen katlanmaları açıkça düşük enerji çözümleri olarak kabul edebiliyor. Buna karşılık, koordinat-temelli şemalar doğal olarak ikili etkileşimlerle sınırlı kalıyor ve daha düzenli ceza terimleri kullanıyor; bu da gereken sayısal hassasiyeti ılımlı tutuyor ve özellikle tetrahedral ızgarada donanıma haritalamayı daha temiz kılıyor.
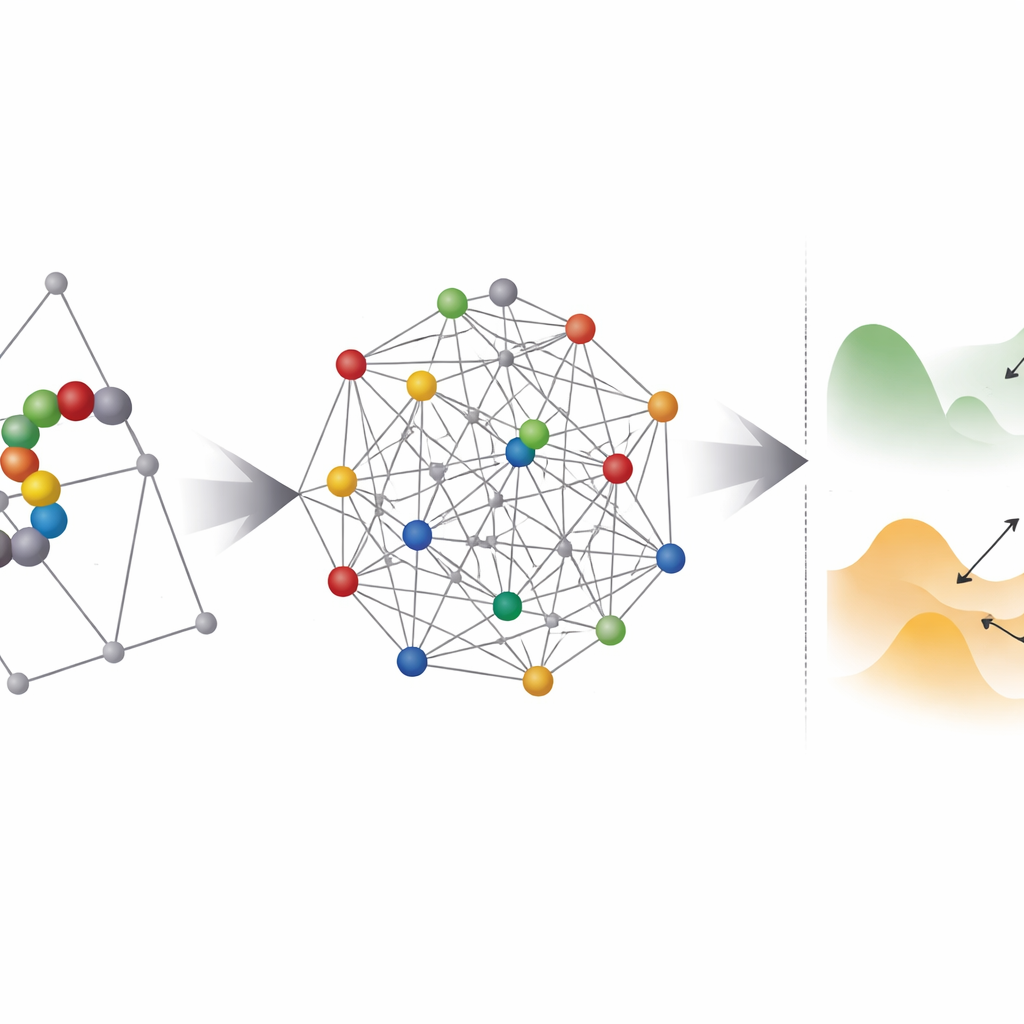
Kuantum donanımı nerede yardımcı oluyor—ve nerede zorlanıyor
Sonraki adımda ekip, bu kodlanmış problemlerin herhangi bir optimizör için—kuantum ya da klasik—ne kadar “engebeli” göründüğünü araştırıyor. Düşük enerjili durumların dağılımını incelemek ve aralarındaki bariyerlerin kalınlığını tahmin etmek için paralel temperleme adlı bir teknik kullanıyorlar. Koordinat-temelli örneklerin çoğu, prensipte kuantum tünellemenin yakın minimumlar arasında atlamada yardımcı olabileceği bir rejime giriyor. Ancak pratik bir engel göze çarpıyor: mevcut kuantum tavlayıcılar her qubiti her diğerine bağlayamıyor, bu nedenle her mantıksal değişken embedding olarak adlandırılan bir süreçte fiziksel qubit zincirine eşlenmek zorunda kalıyor. Bu, qubit sayısını dramatik biçimde artırıyor ve sıklıkla etkin enerji peyzajını daha engebeli ve çözmeyi daha zor hale getiriyor.
Kuantum ve klasik çözücülerin karşılaştırması
Son olarak yazarlar, kısa rastgele seçilmiş amino asit zincirleri için gerçek en düşük enerjili katlanmayı bulmanın farklı yöntemlerle ne kadar sürdüğünü karşılaştırıyorlar. En umut verici model olan yeni tetrahedral koordinat-temelli kodlamaya odaklanarak, yüksek düzeyde optimize edilmiş, GPU hızlandırmalı bir simüle tavlama kodunu iki nesil ticari kuantum tavlayıcıyla kıyaslıyorlar. Altı ila dokuz kalıntı uzunluğundaki küçük test proteinlerinde her iki yaklaşım da boyutla benzer ölçeklenme gösteriyor, ancak mutlak ölçekte klasik kod hâlâ orijinal problem üzerinde birkaç mertebe daha hızlı. Bununla birlikte her iki yöntem de tam olarak aynı, önceden embed edilmiş problem üzerinde çalıştırıldığında kuantum tavlayıcı onların klasik simüle tavlamasından daha iyi performans gösteriyor; bu, embedding artık ana darboğaz olmadığında potansiyel bir ölçeklenme avantajına işaret ediyor.
Gelecek için ne anlama geliyor
Genel okuyucu için çıkarım şudur: kuantum tavlama şu anda gerçekçi proteinlerin katlanması için bir kestirme yol değil, ancak tamamen çıkmaz da değil. Çalışma, seyrek tetrahedral kafeslerdeki koordinat-temelli modelleri en umut verici yol olarak belirliyor ve model tasarımının ortaya çıkan problemlerin herhangi bir çözücü için ne kadar zor olduğunu büyük ölçüde şekillendirdiğini gösteriyor. Bugünün kuantum donanımı, bağlılık ve hassasiyet eksikliği nedeniyle kanıt kavramı boyutlarının çok ötesindeki proteinlerle başa çıkamıyor ve bazı mevcut katlanma modelleri temel fiziği yanlış tanımlıyor. Yine de kuantum aygıtları daha iyi bağlı qubitler ve daha düşük hata oranları ekledikçe ve kodlamalar fizikdışı katlanmaları önleyecek ve embedding yükünü azaltacak şekilde iyileştirildikçe, kuantum tavlama özellikle klasik ve yapay zekâ tabanlı yöntemleri zorlayan engebeli protein katlanma zorluklarında rekabetçi—ve belki de sonunda üstün—hale gelebilir.
Atıf: Scheiber, T., Heller, M. & Giebel, A. Exploring quantum annealing for coarse-grained protein folding. Sci Rep 16, 12035 (2026). https://doi.org/10.1038/s41598-026-46916-w
Anahtar kelimeler: kuantum tavlama, protein katlanması, kaba taneli modeller, optimizasyon algoritmaları, kuantum hesaplama donanımı