Clear Sky Science · it
Esplorare l’annealing quantistico per il ripiegamento proteico a grana grossa
Perché questo è importante per i farmaci del futuro
Le forme in cui le proteine si ripiegano determinano il loro funzionamento nei nostri corpi, dal trasporto dell’ossigeno al riconoscimento dei virus. Predire queste forme è fondamentale per progettare farmaci, ma farlo con precisione per tutte le proteine rimane estremamente difficile. Questo articolo si chiede se un nuovo tipo di hardware di calcolo — gli annealer quantistici — potrebbe un giorno contribuire a risolvere problemi di ripiegamento particolarmente difficili, che mettono in crisi l’intelligenza artificiale odierna e i supercomputer classici.
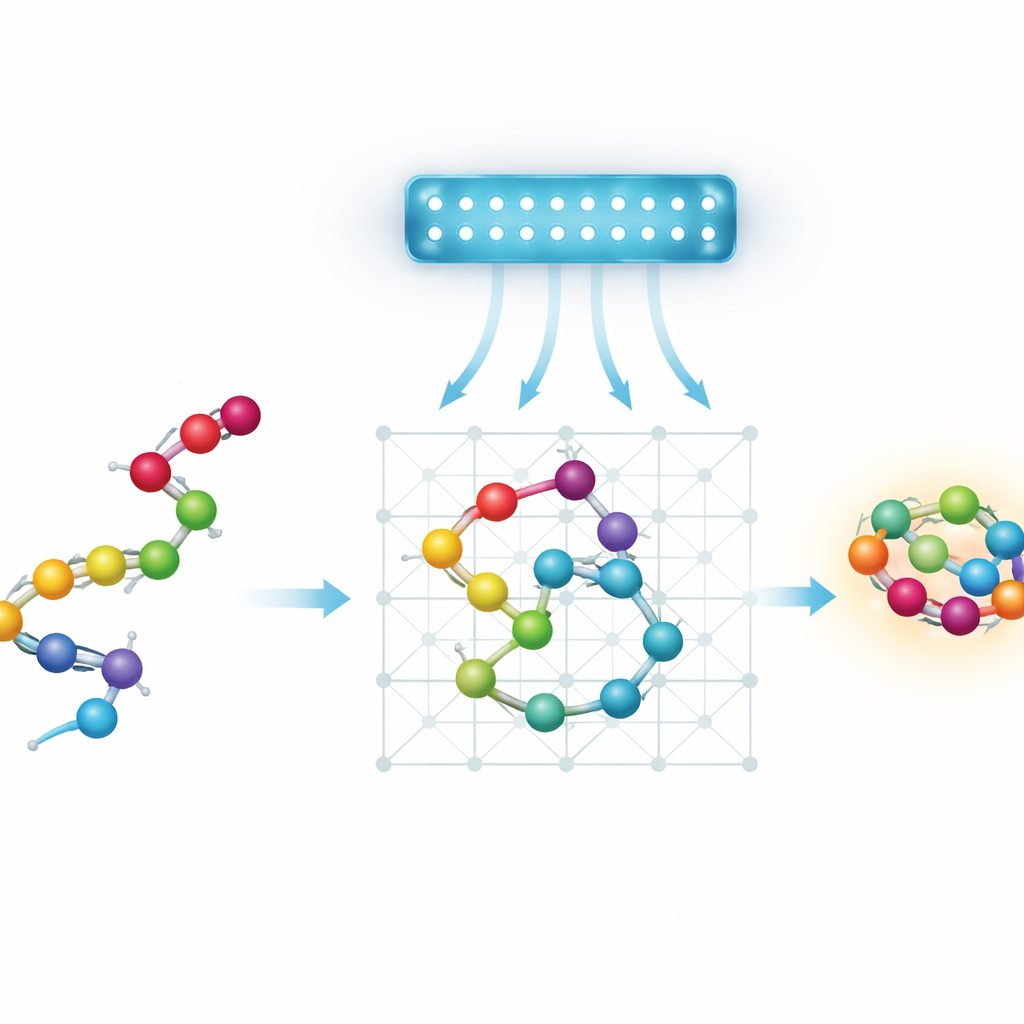
Proteine, paesaggi ed una ricerca di scorciatoie
In fondo, il ripiegamento delle proteine è un gigantesco problema di ricerca. Una catena di amminoacidi può ripiegarsi in un numero astronomico di forme, ognuna con una sua energia. La natura tende a scegliere le forme a bassa energia, ma il “paesaggio energetico” è frastagliato, pieno di valli profonde separate da colline ripide. I metodi di ottimizzazione standard e le simulazioni ispirate alla fisica spesso restano intrappolati in valli locali e perdono la soluzione migliore. L’annealing quantistico è interessante perché, in teoria, effetti quantistici come il tunneling potrebbero permettere a un sistema di attraversare alcune di queste colline invece di doverle sempre scalare, trovando potenzialmente buoni ripiegamenti più in fretta.
Semplificare le proteine per le macchine quantistiche
Gli annealer quantistici attuali sono limitati per dimensioni e connettività, quindi gli autori lavorano con modelli semplificati, o a grana grossa, delle proteine. Invece di seguire ogni atomo, rappresentano ciascun amminoacido come una sfera su una griglia discreta. Esaminano quattro modi per codificare questa configurazione come un problema matematico gestibile da un annealer quantistico. Due modelli “a svolta” descrivono la catena in base alla sequenza di passi compiuti sulla griglia. Due modelli “basati sulle coordinate” assegnano a ogni sfera una posizione specifica nella rete. Ciascuna variante può essere disposta su una griglia cubica standard o su una più economica griglia tetraedrica, dove ogni sfera ha meno vicini. Il gruppo introduce inoltre un nuovo schema basato su coordinate sulla rete tetraedrica, che usa due griglie intrecciate per rappresentare sfere alternate pur mantenendo semplici le interazioni.
Valutare la qualità del modello e la difficoltà del problema
Gli autori eseguono innanzitutto un dettagliato “audit delle risorse”: quanti bit binari (qubit), quante accoppiature a coppie e quanto ampia è la gamma di intensità delle interazioni richieste da ciascun modello al crescere della lunghezza della proteina. Dimostrano che alcune codifiche a svolta diventano rapidamente troppo dense e richiedono una precisione numerica molto elevata, entrambe caratteristiche poco compatibili con l’hardware attuale. Un precedente modello tetraedrico a svolta mostra un difetto più profondo: per sequenze più lunghe di circa dieci amminoacidi può considerare legittimi come soluzioni a energia minima ripiegamenti chiaramente non fisici con auto-intersezioni. Al contrario, gli schemi basati sulle coordinate sono naturalmente limitati a interazioni a coppie e usano penalità più regolari, il che mantiene la precisione numerica richiesta modesta e la mappatura sull’hardware più pulita, specialmente sulla griglia tetraedrica.
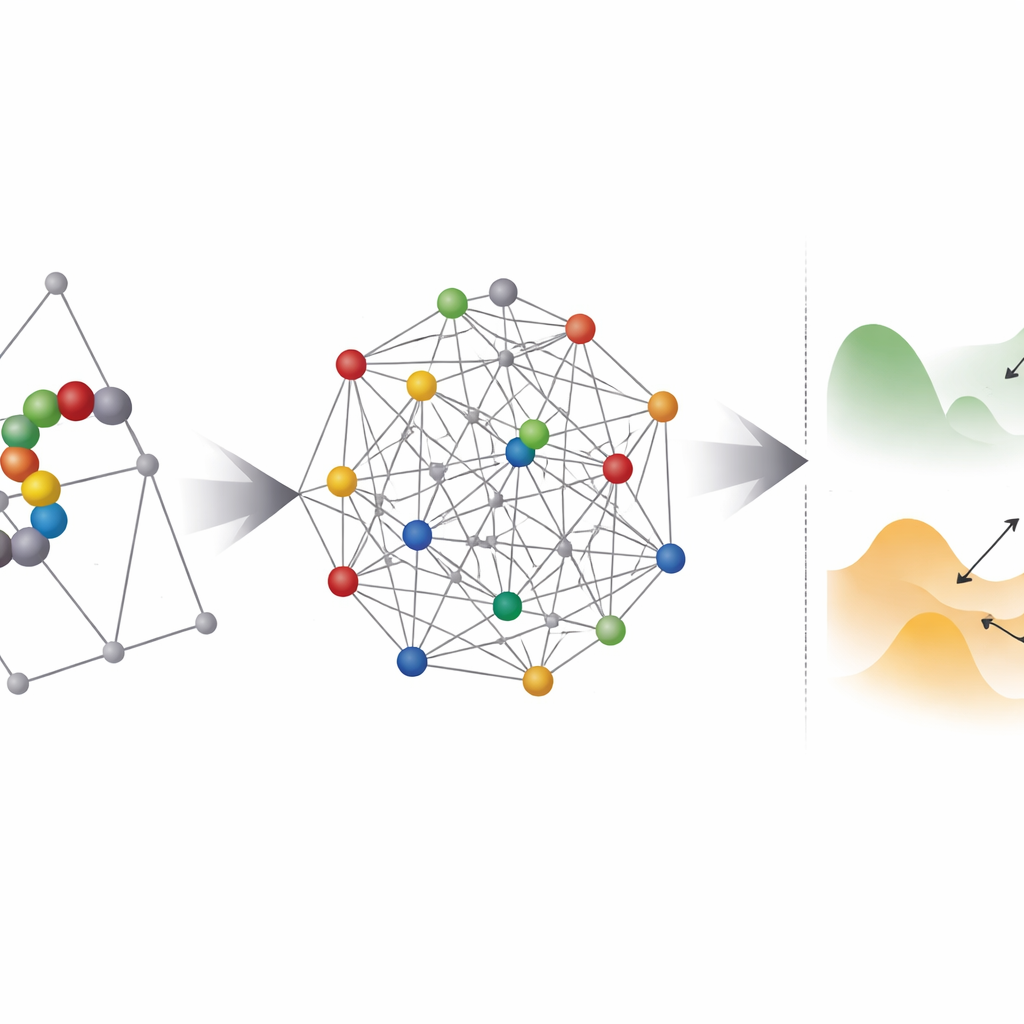
Dove l’hardware quantistico aiuta — e dove fatica
Successivamente il team indaga quanto questi problemi codificati appaiano “frastagliati” a qualunque ottimizzatore, quantistico o classico. Usano una tecnica chiamata parallel tempering per sondare la distribuzione di stati a bassa energia e stimare quanto spesse siano le barriere tra di essi. La maggior parte delle istanze basate sulle coordinate rientra in un regime in cui il tunneling quantistico potrebbe, in linea di principio, aiutare a saltare tra minimi vicini. Tuttavia, emerge un ostacolo pratico: gli annealer quantistici esistenti non possono collegare ogni qubit a tutti gli altri, quindi ogni variabile logica deve essere mappata su una catena di qubit fisici in un processo chiamato embedding. Questo gonfia drammaticamente il numero di qubit e spesso rende il paesaggio energetico effettivo più irregolare e più difficile da risolvere.
Scontro tra solver quantistici e classici
Infine, gli autori confrontano quanto tempo impiegano diversi metodi a trovare il vero ripiegamento a energia minima per catene di amminoacidi corte e scelte casualmente. Mettono a confronto un codice di simulated annealing altamente ottimizzato e accelerato su GPU con due generazioni di annealer quantistici commerciali, concentrandosi sul modello più promettente: la nuova codifica basata sulle coordinate sulla griglia tetraedrica. Per piccole proteine di prova da sei a nove residui, entrambi gli approcci mostrano una scala simile al crescere della dimensione, ma su una scala assoluta il codice classico è ancora molto più veloce — di diversi ordini di grandezza — quando lavora sul problema originario. Tuttavia, quando a entrambi i metodi viene chiesto di risolvere esattamente la stessa versione del problema già embeddata, l’annealer quantistico supera il loro simulated annealing classico, suggerendo un possibile vantaggio di scaling una volta che l’embedding non sarà più il collo di bottiglia principale.
Cosa significa per il futuro
Per il lettore generale, la conclusione è che l’annealing quantistico non è ancora una scorciatoia per ripiegare proteine realistiche, ma neanche un vicolo cieco. Lo studio identifica i modelli basati sulle coordinate su reticoli tetraedrici sparsi come la strada più promettente da percorrere e mostra che il design del modello influenza fortemente quanto i problemi risultino difficili per qualsiasi solver. L’hardware quantistico attuale manca di connettività e precisione per gestire proteine ben oltre dimensioni da prova di principio, e alcuni modelli di ripiegamento esistenti descrivono in modo errato anche fisica di base. Tuttavia, man mano che i dispositivi quantistici avranno qubit connessi meglio e tassi di errore più bassi, e man mano che le codifiche saranno affinate per evitare ripiegamenti non fisici e ridurre l’overhead di embedding, l’annealing quantistico potrebbe diventare competitivo — e forse infine superiore — per sfide di ripiegamento proteico particolarmente frastagliate che mettono sotto pressione i metodi classici e basati su IA.
Citazione: Scheiber, T., Heller, M. & Giebel, A. Exploring quantum annealing for coarse-grained protein folding. Sci Rep 16, 12035 (2026). https://doi.org/10.1038/s41598-026-46916-w
Parole chiave: annealing quantistico, ripiegamento delle proteine, modelli a grana grossa, algoritmi di ottimizzazione, hardware di calcolo quantistico