Clear Sky Science · de
Untersuchung von Quantum-Annealing für grobgespanntes Protein-Folding
Warum das für zukünftige Medikamente wichtig ist
Die Formen, in die Proteine sich falten, bestimmen ihre Funktion im Körper — vom Sauerstofftransport bis zur Erkennung von Viren. Diese Formen vorherzusagen ist für die Wirkstoffentwicklung entscheidend, aber für alle Proteine präzise Vorhersagen zu liefern, bleibt extrem schwierig. Dieser Artikel fragt, ob eine neue Art von Rechenhardware — Quantum-Annealer — eines Tages dabei helfen könnte, besonders hartnäckige Faltungsprobleme zu lösen, die heutige KI-Methoden und klassische Supercomputer vor große Herausforderungen stellen.
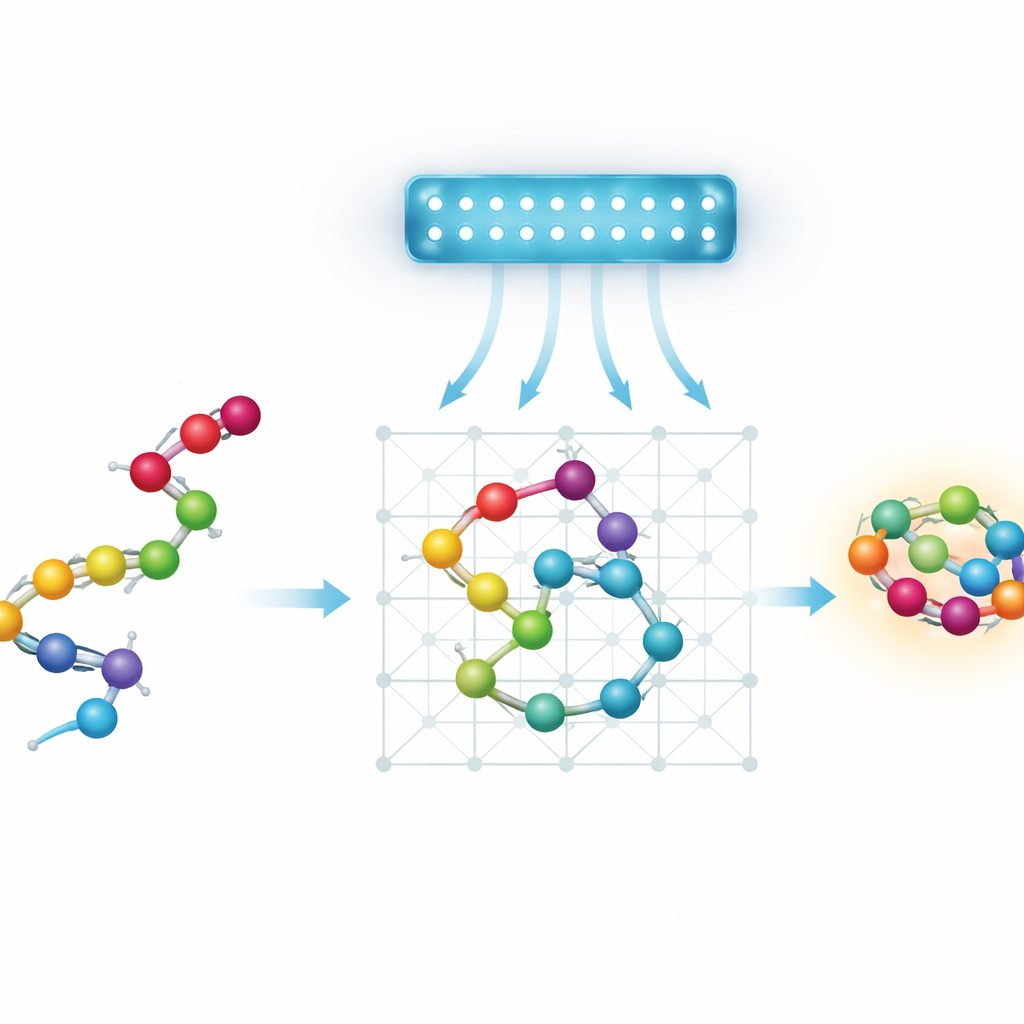
Proteine, Landschaften und die Suche nach Abkürzungen
Im Kern ist Protein-Folding ein gigantisches Suchproblem. Eine Kette von Aminosäuren kann in astronomisch viele Formen falten, jede mit einer eigenen Energie. Die Natur tendiert zu niedrigen Energiezuständen, doch die „Energielandschaft“ ist zerklüftet, voller tiefer Täler, getrennt durch steile Hügel. Standard-Optimierer und physikbasierte Simulationen bleiben oft in lokalen Tälern stecken und übersehen die beste Faltung. Quantum-Annealing erscheint attraktiv, weil quantenmechanische Effekte wie Tunneln einem System theoretisch erlauben könnten, durch einige dieser Hügel hindurchzufließen, statt sie immer hinaufklettern zu müssen — womit sich gute Faltungen potenziell schneller finden lassen.
Proteine für Quantenmaschinen vereinfachen
Die heutigen Quantum-Annealer sind in Größe und Konnektivität begrenzt, daher arbeiten die Autoren mit vereinfachten, also grobgespann-ten Modellen von Proteinen. Anstatt jedes Atom zu verfolgen, repräsentieren sie jede Aminosäure als Perle auf einem diskreten Gitter. Sie untersuchen vier Möglichkeiten, dieses Setup als mathematisches Problem zu kodieren, das ein Quantum-Annealer verarbeiten kann. Zwei „Winkel-basierte“ Modelle beschreiben die Kette durch die Abfolge der Schritte auf einem Gitter. Zwei „Koordinaten-basierte“ Modelle weisen jeder Perle eine spezifische Gitterposition zu. Jede Variante lässt sich entweder auf einem Standardkubikgitter oder auf einem platzsparenderen tetraedrischen Gitter anordnen, bei dem jede Perle weniger Nachbarn hat. Das Team stellt außerdem ein neues koordinatenbasiertes Schema auf dem tetraedrischen Gitter vor, das zwei ineinandergreifende Gitter nutzt, um abwechselnde Perlen darzustellen und gleichzeitig die Wechselwirkungen einfach zu halten.
Modellqualität und Problemhärte testen
Die Autoren führen zunächst eine detaillierte „Ressourcen-Bilanz“ durch: wie viele binäre Variablen (Qubits), wie viele paarweise Kopplungen und wie groß die Spannweite der Wechselwirkungsstärken jedes Modell mit wachsender Proteingröße benötigt. Sie zeigen, dass einige winkelbasierte Kodierungen sehr schnell zu dicht werden und extrem hohe numerische Präzision verlangen — beides schlechte Voraussetzungen für die heutige Hardware. Ein zuvor vorgeschlagenes winkelbasiertes tetraedrisches Modell offenbart einen gravierenderen Fehler: Für Sequenzen, die länger als etwa zehn Aminosäuren sind, kann es offensichtlich unphysikalische Selbstüberschneidungen als legitime Lösungen mit minimaler Energie betrachten. Im Gegensatz dazu sind die koordinatenbasierten Schemata naturgemäß auf paarweise Wechselwirkungen beschränkt und verwenden regelmäßigere Strafterme, was die erforderliche numerische Präzision überschaubar hält und die Abbildung auf Hardware insbesondere auf dem tetraedrischen Gitter sauberer macht.
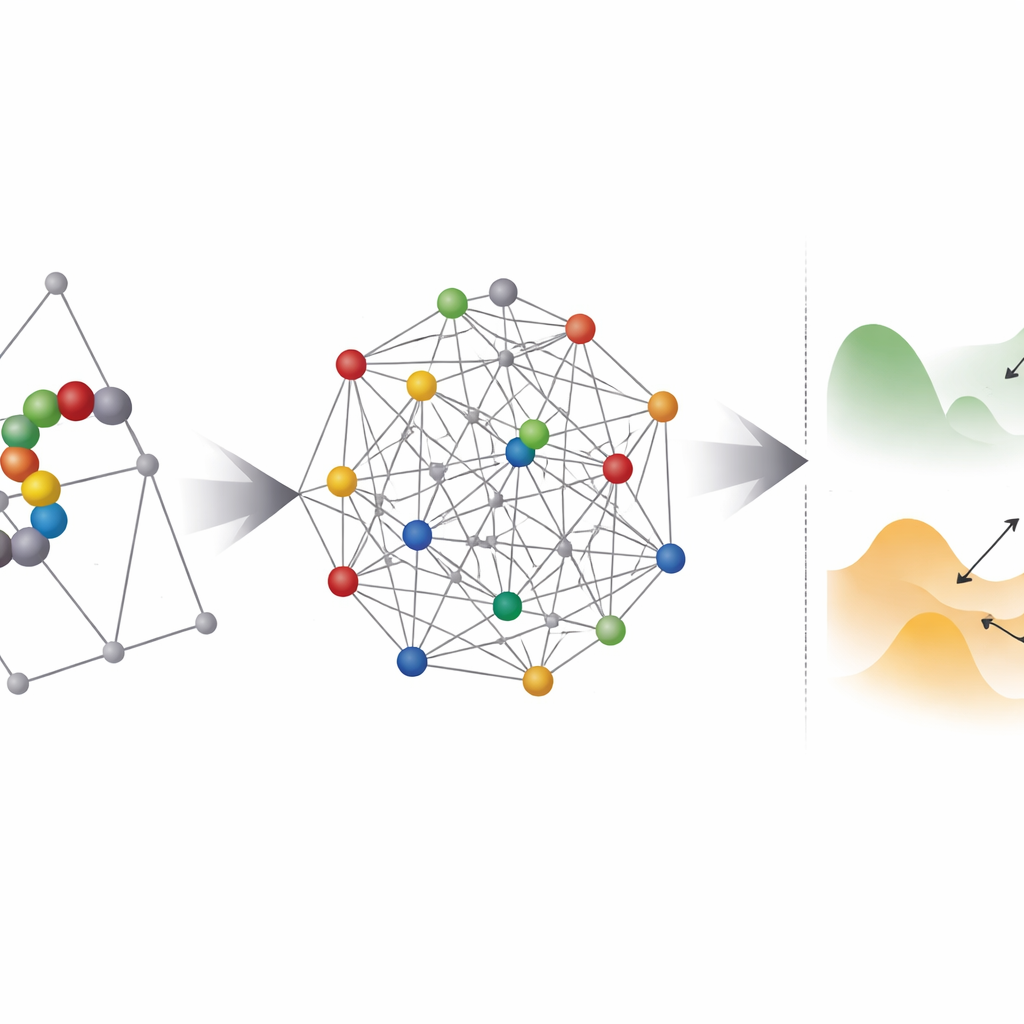
Wo Quantenhardware hilft — und wo sie kämpft
Als Nächstes untersuchen die Forschenden, wie „zerklüftet“ diese kodierten Probleme für beliebige Optimierer, quantum oder klassisch, erscheinen. Sie verwenden eine Technik namens Parallel Tempering, um die Verteilung niederenergetischer Zustände zu untersuchen und abzuschätzen, wie dick die Barrieren zwischen ihnen sind. Die meisten koordinatenbasierten Instanzen fallen in ein Regime, in dem Quanten-Tunneln prinzipiell helfen könnte, zwischen nahegelegenen Minima zu springen. Allerdings gibt es ein praktisches Hindernis: bestehende Quantum-Annealer können nicht jeden Qubit mit jedem anderen verbinden, sodass jede logische Variable in einem Einbettungsprozess auf eine Kette physischer Qubits abgebildet werden muss. Das treibt die benötigte Qubit-Anzahl stark in die Höhe und macht die effektive Energielandschaft oft rauer und schwerer lösbar.
Duell zwischen Quanten- und klassischen Lösern
Schließlich vergleichen die Autoren, wie lange verschiedene Methoden benötigen, um die tatsächliche energieärmste Faltung für kurze, zufällig gewählte Aminosäureketten zu finden. Sie benchmarken einen stark optimierten, GPU-beschleunigten Simulated-Annealing-Code gegen zwei Generationen kommerzieller Quantum-Annealer und konzentrieren sich auf das vielversprechendste Modell: die neue koordinatenbasierte Kodierung auf dem tetraedrischen Gitter. Bei kleinen Testproteinen mit sechs bis neun Resten zeigen beide Ansätze eine ähnliche Skalierung mit der Größe, aber in absoluten Laufzeiten ist der klassische Code beim Lösen des Ursprungsproblems noch um mehrere Größenordnungen schneller. Wenn jedoch beide Methoden die exakt gleiche, bereits eingebettete Version des Problems lösen sollen, schneidet der Quantum-Annealer besser ab als ihr klassisches Simulated-Annealing, was auf einen potenziellen Skalenvorteil hindeutet, sobald die Einbettung nicht mehr der dominierende Engpass ist.
Was das für den weiteren Weg bedeutet
Für eine allgemeine Leserschaft lautet die Quintessenz: Quantum-Annealing ist noch kein Abkürzungsweg zum Falten realistischer Proteine, aber auch kein Sackgasse. Die Studie identifiziert koordinatenbasierte Modelle auf sparsamen tetraedrischen Gittern als den vielversprechendsten Weg nach vorn und zeigt, dass das Modell-Design stark beeinflusst, wie schwierig die resultierenden Probleme für jeden Löser sind. Die heutige Quantenhardware fehlt es an Konnektivität und Präzision, um weit über Proof-of-Concept-Größen hinausgehende Proteine zu behandeln, und einige existierende Faltungsmodelle beschreiben sogar grundlegende Physik falsch. Doch sobald Quantengeräte besser vernetzte Qubits und geringere Fehlerquoten bieten und Kodierungen so verfeinert werden, dass unphysikalische Faltungen vermieden und Einbettungsaufwand reduziert wird, könnte Quantum-Annealing konkurrenzfähig — und vielleicht schließlich überlegen — werden für besonders zerklüftete Protein-Faltungsaufgaben, die klassische und KI-basierte Methoden stark beanspruchen.
Zitation: Scheiber, T., Heller, M. & Giebel, A. Exploring quantum annealing for coarse-grained protein folding. Sci Rep 16, 12035 (2026). https://doi.org/10.1038/s41598-026-46916-w
Schlüsselwörter: Quantum-Annealing, Protein-Faltung, grobe Modelle, Optimierungsalgorithmen, Quantencomputing-Hardware